유기질 퇴비 시비에 따른 토양 중 polychlorinated biphenyls의 작물 흡수 이행
초록
토양 환경 중 오염물질의 작물체로의 이행은 토양유기물함량, 광물조성, 기상 및 식생 등, 다양한 인자의 영향을 받으며, 이 가운데 유기물 함량은 본 연구의 대상물질인 PCBs를 비롯한 다양한 오염물질의 작물 흡수이행 및 축적에 지대한 영향을 미치는 것으로 알려져 있다. 한편 난분해성 오염물질의 식물이행을 포함한 생물농축현상은 오염지 토양 유래의 농산물의 안전성 등, 식품안전에 위해요인으로 고려되고 있다. 본 연구에서는 수종의 PCBs 및 관련 유사체를 합성하고, 토양 살포 후, 토양 및 작물 중, 해당 오염물의 농도 변화를 연구하였다. 재배 토양은 유기질 시비량을 무시비구, 저농도 및 고농도 시비구로 나누어 당근을 이식하여 재배하였으며, GC-MS를 이용, 분석을 수행하였다. 일반적으로 PCBs의 작물 흡수이행은 유기질 시비의 양이 증가함에 따라 감소하는 경향을 나타내었다. 3,3',4,4',5-pentachlorobiphenyl (PCB-126)의 경우 이행계수는 무시비, 저시비 및 고시비구에 대하여 0.17, 0.12 및 0.08로 나타났다. 다른 유사체의 경우에도 이와 같은 경향이 관찰되었으며, 소수성이 높은 유사체일수록 작물내의 축적농도가 낮아졌다. 한편 지용성이 매우 높은 유사체의 경우, 재배기간 중, 지속적 축적이 나타난 반면, biphenyl 등 지용성이 다소 낮은 물질의 경우 이식 후 40-60일 경과시까지 꾸준한 농도 증가를 나타내었으나 이후 완만한 속도의 감소를 보였다. 이와 같은 경향은 토양 교질물로서 지용성물질에 대한 흡착력이 큰 부식질 등의 형성에 의한 것으로 사료된다.
Abstract
Translocations of organic compounds from soil to crops are dependent on many physicochemical properties including soil organic compounds, mineralogy, climate, and plant species, among which the organic contents were one of the most important factors determining the transfer ratio of organic pollutants from agricultural soils to common crops. Bioaccumulation through translocation is an important process for the evaluation of crop safety cultivated in contaminated soils
Several PCB derivatives were prepared by chemical syntheses and applied on upland soils with different application rates of organic fertilizer. Concentrations of PCBs in soil and carrot were analyzed with GC-MS. In general, the translocation ratio of PCBs from soil to carrot was inversely related to the organic contents. For example, the ratios of PCB-126 in low-, medium-, and high-organic content soils were 0.17, 0.12, and 0.08, respectively. In addition, tranlocation ratios were also inversely related to the hydrophobicities of contaminants. Lipophilic PCBs were gradually accumulated in carrots till the end of experimental periods, while accumulation of polar analogues reached a maximum at 40-60 days of cultivation.
Translocation of organic pollutants were negatively correlated with the soil organic contents. Application of organic fertilizers inhibit the accumulation of PCBs on carrot, which were well coincided with literature results. Additionally, it was found that accumulations of lipophilic persistant contaminants including highly chlorinated PCB analogues were very slow.
Keywords:
Organic content, Polychlorinated biphenyl, translocation, bioaccumulation서 론
다양한 유기 및 무기질 화합물로 구성된 토양 교질물은 작물 생장에 필수적인 양분의 공급과 함께, 환경 중에 유입되는 오염물질의 동태를 결정하는 주요한 인자 중의 하나이다(Bollag et al., 1992). Polychlorinated biphenyls (PCBs)를 포함한 소수성 환경 오염물은 토양 유기물에 강하게 흡착되는 것이 일반적인데, humic acid, fulvic acid 등의 토양 부식질의 함량과 관련 유기물의 표면전하에 영향을 줄 수 있는 다양한 토성 요인에 따라 동일한 오염물질이라고 하더라도 상이한 흡착 경향을 나타낸다(Frankki et al., 2006; Persson et al., 2008; Zhu et al., 2004). 유기물의 토양 흡착과 관련된 연구는 주로 다핵방향족 탄화수소(polycyclic aromatic hydrocarbons, PAHs) 등과 같이 다양한 환경에 광범위한 분포를 나타내는 물질에 대하여 진행되어 왔으나, 농약을 비롯한 농경활동에 의하여 발생되는 오염에도 다수 연구가 수행되고 있다(Ahmad et al., 2001; Motoki et al., 2014). 오염물질의 토양 흡착 및 탈착 현상은 부식질을 포함한 토양 유기물은 해당 물질의 화학적 구조뿐만 아니라 pH, 점토 광물의 조성 및 강우 등에 의하여 달라 질 수 있다(Badea et al., 2014; Hiller et al., 2009). 또한 토양 유기물의 함량과 함께 세부 구조 역시 흡착에 영향을 주는 것이 알려져 있다. 예를 들어 Ahmad 등은 NMR을 이용, 부식질의 화학구조를 분석하고, 농약의 흡착특성과의 상관관계를 규명하였는데, 부식질 중 방향족 관능기의 함량이 증가함에 따라 농약의 흡착계수(Koc)가 증가하는 것을 보고하였다(Ahmad et al., 2001). 토양부식질은 식물 및 미생물의 잔사가 주요한 급원으로서 다양한 생물학적, 화학적 분해과정을 거쳐 생성되며, 화학적 조성 및 물리적 성질은 토양 무기질과 마찬가지로 지속적 변화를 거치게 된다. 따라서 환경오염물질의 토양에 대한 흡착 특성 역시 경과시간에 따라 다르게 나타날 수 있다. Motoki 등은 27종의 수용해도가 다른 농약을 대상으로 연구를 수행하여 대부분의 경우 처리후 경과일에 따라 식물체가 쉽게 가용한 농약의 용출 속도가 달라지는 것을 보고하였다(Motoki et al., 2016). 이와 같은 현상은 상기한 바와 같이 토양 입자의 물리화학적 성질의 지속적 변화와 이에 따른 농약 및 기타 유기물의 토양 중 동태의 시간에 따라 다르다는 점을 보여준다. 한편 토양 유기물은 미생물상에도 영향을 끼치며 일반적으로 적절한 유기물 함량의 토양에서 다량의 미생물군체가 발견되며, 오염물질의 분해를 촉진하는 경향이 있다(Briceno et al., 2007). 식물 또는 기타 유래의 유기물의 장기적 풍화에 의하여 형성되는 부식질이 유기오염물질의 토양 입자 흡착에 대하여 흡착량 및 속도의 증대를 초래하는 것과 비교하여, 농업에 일반적으로 사용되는 유기질 비료의 경우, 해당 소재의 발효 정도, 유래 등의 요인에 따라 다양한 다른 영향을 나타내는것으로 알려져 있다. 예를 들어 유기질 시비의 주요한 수단으로 사용되는 퇴비는 일부 농약에 대하여 농약의 용탈을 촉진하는 것으로 알려져 있다(Li et al., 2005). 이와 같은 현상은 퇴비 등에서 발생되는 다양한 가용성 유기물(dissolved organic matter, DOM)의 토양 용수중 이동과 이에 의하여 토양 입자중 흡착된 오염물질의 용해에 따른 현상으로서 농도에 따라 흡착 및 용탈의 상반된 효과를 나타내기도 한다(Gao et al., 2007, Huang and Lee, 2001).
농작물을 비롯한 다양한 식생이 존재하는 농경지 및 산림환경의 경우에는 이와 같은 다양한 유기물의 흡수-이행 및 이동 현상이 관련 산물의 안전성을 위협하는 요인으로 볼 수 있는데, 작물에 의한 토양 교질물 성상의 변화, 토양용수의 이동 등의 다양한 물리-화학적 현상에 따라 물질의 이동에 변화가 나타나게 된다(Juraske et al., 2009). PAHs, dioxins, 및 PCBs 등의 잔류성 환경오염물질의 경우, 낮은 분해속도, 토양 입자에 대한 강한 흡착 등의 영향으로 오염지의 농작물 및 동물 등에 대한 흡수/이행과 이에 따른 환경 위해성이 지속적으로 지적되고 있으며, 관련 연구의 필요성이 제기되고 있다.
본 연구에서는 PCBs와 관련 유사체를 토양 환경중 존재하는 대표적 난분해성 유기 오염물질로 선정하고, 국내 농작물 재배에 일반적으로 사용되는 유기질 퇴비를 밭토양에 시비한 후, 유기질 시비의 함량과 이에 따른 PCBs 및 구조 유사체의 작물로의 흡수-이행 경향을 검토하고, PCBs의 분해/소실에 미치는 토양 유기물 함량의 영향을 연구하였다.
재료 및 방법
재료 및 시약
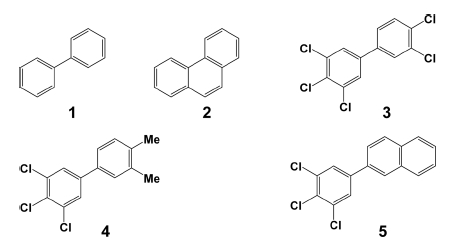
Biphenyl, phenanthrene 표준품(>98%) 및 유기용매는 HPLC급으로 Sigma-Aldrich Korea 및 Alfa Aesar (USA)에서 구입하여 사용하였다. 기타 시약으로 크로마토그래피용 silica gel은 Merck사의 제품을 사용하였으며, ethyl acetate 등 대사물 추출용 용매는 대정사의 (Korea) 제품을 구입, 사용하였다. PCB-126 및 관련 유도체는 전보의 방법을 참고하여 합성하고, column chromatography를 이용, 정제하여(순도 >99%) 사용하였다(Fig. 1) (Lim et al., 2016).
PCB 이성질체의 토양 처리 및 당근 재배
실험 토양은 경기도 남양주시 소재, 밭토양으로, 음건 후, 작물 잔사 등을 제거 후, 사용하였으며, 토성은 사질양토, pH 5.92, 유기물 함량, 2.5%, CEC 15.6 meq/100 g이었다. 해당 토양에 혼화 처리한 퇴비는 농협을 통하여 가축분 퇴비를 구매하여 사용하였으며, 토양 중량 기준, 무처리구, 저처리구(1%) 및 고처리구(5%)로 퇴비 함량을 조절하여 조제하였다. Biphenyl 및 PCBs 표준용액(acetone, 20 mL)을 토양(20 kg)에 가하여, 토양 중 농도를 biphenyl (1), phenanthrene (2), PCB-126 (3), 3,4,5-trichloro-3',4'-dimethylbiphenyl (4), 2-(3,4,5-trichlorophenyl)naphthalene (5)을 0.5-1.5 mg/kg으로 조절하였다. 혼합 시료는 48시간 실온 중 건조 후, 증류수(200 mL)을 가하여 혼화후, 실험용 pot (20*20*40 cm)에 가하여 1주일간 방치하였다. 실험용 당근으로는 미니당근(아시아베이비)를 아시아종묘에서 구매하여, 화합물 비처리구 토양에서 2주간 재배한 다음, pot별 3구 식재한 다음, 실온에서 0, 15, 30, 60 및 90일 후 채취하여 실험에 사용하였다. 재배 기간 중, 증류수를 이용하여 토양 수분 함량은 30-40% 내외로 조절하였다. 토양 시료는 채취 후, 실온에서 24시간 음건하여, 혼합한 다음, -20oC에서 보관하였다. 당근 시료는 증류수로 세척하여, 표면에 부착된 토양을 제거한 다음 -20oC에 보관하였다. 실험구는 PCBs 이성질체별로 3반복으로 수행하였다.
Biphenyl 및 PCB 추출 및 정제
시료(당근, 5 g)을 분취하여, acetone (100 mL)과 혼합 후, Waring blender로 5분간 마쇄하고, sonicator를 이용, 60분간 추출하였다. 감압여과 후, 잔사를 동일한 조건에서 2회 추출하여 여액을 합하였다. 여액을 건고한 다음, dichloromethane (50 mL)에 용해하여, 무수 Na2SO4로 통과한 다음 농축하여 10 mL로 조정하고, 아래와 같은 column chromatography를 수행하였다. 상기의 용액을 적층 황산 silica gel column (column 하단에서부터 silica gel, 0.1 g, 5% 황산-silica gel, 0.9 g, 및 무수 Na2SO4, 0.1 g)에 가하여 용출한 다음, dichloromethane (5 mL)을 추가, PCBs를 용리하였다. Column 분획을 감압 건고한 다음, dichloromethane (250 uL)에 용해한 다음, gas chromatography-mass spectrometry (GC-MS)에 주입하여 정량 분석을 수행하였다.
토양 시료의 경우, 동일량의 시료(5 g)를 acetone (150 mL)을 가한 다음, sonicator로 60분간 2회 추출하여 상기의 당근 시료와 동일한 방법으로 정제 및 분석을 수행하였다.
분석법의 회수율은 상기의 방법에 따라 고농도 시비구 토양 및 당근에 분석 대상물질의 농도가 0.1 및 0.5 mg/kg이 되도록 처리하여, 3반복으로 수행하였다.
분석기기 및 분석조건
Biphenyl 및 기타 PCBs의 분석은 Shimadzu GC-2010/SE GC-MS로 수행하였으며, Restek사의 Rtx-5MS (30 m, 0.25 mm i.d., 0.25 μm thickness) column을 사용하였다. Column 온도조건은 170oC로 10분간 유지 후, 2oC/분로 승온, 290oC에서 20분간 유지하였으며, injector 온도는 250oC, interface 온도는 275oC로 설정하였고, helium carrier gas는 1 mL/분으로 유지하였다. Biphenyl 및 phenenthrene의 정성 분석은 total ion chromatogram (m/z 100-500)에서 실시하였으며, 정량 분석은 selected ion monitoring (SIM) mode로 수행하였다. SIM 분석을 위한 정량 ion으로는, biphenyl, m/z 154; phenanthrane, m/z 178; PCB-126, m/z 324; 3,4,5-trichloro-3',4'-dimethylbiphenyl, m/z 284; 2-(3,4,5-trichlorophenyl)-naphthalene, m/z 306을 선정하여 분석을 수행하였다. TIC 및 SIM 분석 시 시료는 2 μL를 주입하였다.
PCB congener의 logP 측정 및 logKoc 예측
신규로 합성된 PCBs의 logP는 HPLC를 이용한 US-EPA 방법을 이용하여 구하였다(Lim et al., 2016). 토양흡착계수(logKoc)는 상기의 logP를 바탕으로 EPI Suite를 이용하여 예측값을 구하였다(EPI Suite ver. 4.11, US EPA).
결과 및 고찰
Biphenyl 및 PCB congener 분석법
당근 및 토양 중 PCB-126을 포함한 연구 화합물의 회수율은 70-95% 내외로 나타났으며, 대부분의 화합물에 대하여 저농도 처리구(0.1 mg/kg)의 회수률이 전반적으로 낮았고, 고농도 처리구의 회수율은 87-95%로 다소 높은 경향을 나타내었다(Table 1). 이와 같은 회수율은 전보에서 보고한 무시비구 밭토양의 결과와 비교하여 전반적으로 낮은 것으로 나타났다(무시비구 회수율: 80-110%) (Lim et al., 2016). 유기질 시비가 이루어진 토양에서 나타난 낮은 회수율은 토양 중 유기교질물의 흡착에 의한 것으로 사료되었다(Dean et al., 1996). SIM 방법을 이용한 분석법의 검출한계는 0.01-0.05 mg/kg이었다.
Biphenyl 및 PCB congener의 토양 중 소실
토양 중, 연구 대상물질의 소실 속도는 화학 구조에 따라 다르게 나타나 대략적으로 토양 반감기가 17-231일로 나타났다(Table 2). Biphenyl 및 방향족탄화수소의 일종인 phenanthrene은 빠른 속도로 소실되어 90일 경과 후, 초기 살포량의 2-10% 내외만 잔류된 반면, PCB-126을 비롯한 지용성 오염물의 경우, 90일 경과 후에도 초기 농도의 80-90%가 토양 중에 잔류함을 알 수 있었다(Fig. 2). 분석대상물의 토양 잔류량은 다른 유기 오염물질에서 일반적으로 보고되고 있는 일차반응 곡선에 따라 감소하는 것으로 사료되며, 이에 따른 개별 화합물의 토양 중 반감기는 17-231일이었다(Table 2). 토양 중 유기물질의 분해소실 속도에 영향을 미치는 요인으로는 토양 pH, 토성 등의 통기성 및 함수율 등, 유기물 함량, 미생물 군집의 밀도 등의 토양 고유의 인자와 함께, 물질의 토양 입자에 대한 흡착 특성, 화학적 안정성, Henry's constant 등의 물리적 성질 등, 물질 고유의 특성에 의존한다. 또한 화합물의 구조적 특성 중, 할로겐 등의 치환체의 존재 위치, 대사화학적 성질 등은 해당 물질의 생분해에 지대한 영향을 미치는 것이 알려져 있다(Abramowicz, 1990; Haritash and Kaushik, 2009). 일반적으로 logP 및 Koc 등의 물질의 지용성 정도의 지표로 사용되는 인자들은 미생물 분해, 토양 용수를 통한 이동, 작물로의 흡수-이행에 영향을 미치는 주요한 인자로 알려져 있다(Sabjic and Nakagawa 2014). 한편 토양흡착계수(Koc)는 일반적으로 토양 중 유기교질물, 특히 부식질의 함량과 높은 상관관계가 있는 것으로 알려져 있다(Niederer et al., 2007). 또한 부식질의 세부 화학구조에 따라 지용성 유기물의 흡착력에 차이가 있음이 보고되었다(Niederer et al., 2007). 토양 흡착계수(logKoc)는 logP를 이용하여 예측되기도 하는 데, 이는 토양 교질물에 의한 흡착이 용질의 지용성과 직접적 상관관계를 나타내기 때문이다(Allen-King et al., 2002; Gawlik et al., 1997; Seth et al., 1999). 본 연구에 신규로 합성하여 사용한 물질의 logP는 전보의 방법에 따라, HPLC법으로 측정하였으며, logKoc는 EPI Suite를 이용하여 예측하였다(Lim et al., 2016). 본 연구에 사용한 화합물의 logKoc는 biphenyl, phenanthrene, PCB-126, 3,4,5-trichloro-3',4'-dimethylbiphenyl, 2-(3,4,5-trichlorophenyl)-naphthalene에 대하여 각 2.82, 3.58, 4.16, 4.27 및 5.15이었다.
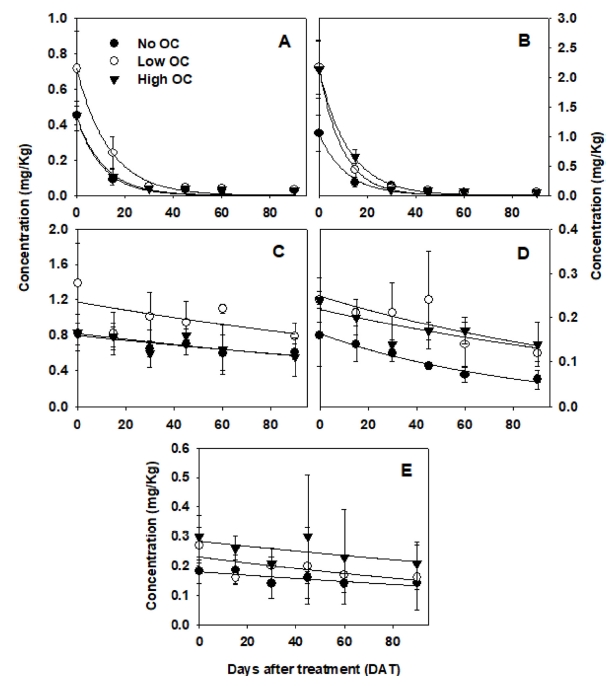
Dissipation of test chemicals (A) biphenyl, (B) phenanthrene, (C) PCB-126, (D) 3,4,5-trichloro-3',4'-dimethylbiphenyl and (E) 2-(3,4,5-trichlorophenyl)naphthalene in soil with no (no OC), low (low OC), and high amount of amendments (high OC) of organic fertilizer.
토양 중 농약을 비롯한 오염물질의 생물학적 분해는 주로 세균 및 진균류에 의하여 일어나는 데, 일부 세균의 경우, 토양입자에 흡착된 유기물을 용리할 수 있는 biosurfactant를 분비하여 강하게 흡착된 오염물질의 분해를 촉진한다고 보고되었다(Awasthi et al., 1999; Sachdev and Cameotra, 2013). 한편 이와 같은 미생물의 활동은 토양 산화-환원 전위의 변화를 초래하여 PAHs의 토양흡착 특성에 변화를 일으키기도 한다(Kim and Pfaender, 2005). 따라서 다양한 미생물의 군집밀도가 높은 유기질 시비는 무시비구와비교하여 오염물질의 분해에 다른 영향을 미칠 것으로 예측되었다. 본 연구 결과에 따르면 biphenyl 및 phenanthrene 등 비교적 지용성이 낮은 물질의 경우, 시비량의 증가는 물질분해에 영향이 없거나, 촉진하는 것으로 나타났다(Table 2). 한편 PCB-126을 비롯한 높은 지용성의 물질에서는 시비량이 증가하는 경우, 분해소실이 지연되는 경향을 나타내었다. 본 연구에 사용한 물질 중, PCB-126과 유사체인 3,4,5-trichloro-3',4'-dimethylbiphenyl의 토양 잔류 특성을 비교한 결과, 유사체의 잔류 반감기가 짧은 것으로 나타났는 다. PCBs의 미생물 대사는 치환된 염소의 수효가 증가할수록 감소하며, meta- 또는 para-치환체일수록 대사속도가 감소하게 된다(Furukawa and Matsumura, 1976). 한편 염소와 비교하여 3,4,5-trichloro-3',4'-dimethylbiphenyl에 존재하는 methyl기는 일반적으로 산화적 대사가 용이한 관능기로 알려져 있다. 따라서 PCB-126의 dimethyl 유사체의 빠른 분해속도는 이와 같은 치환체의 대사 가능성의 차이 때문으로 사료된다.
Biphenyl 및 PCB congener의 당근 시료 중 동태
당근 중, biphenyl을 비롯한 처리물질의 농축 경향은 화합물의 종류와 시비량에 따라 다르게 나타났다(Fig. 3). Biphenyl과 phenanthrene 처리 구의 경우 대략 15-30일 경과시까지 급격한 농도 증가를 나타내었으나, 이후에는 완만하게 감소되는 경향을 보였다. Biphenyl의 경우, 저농도 시비구, 15일 경과시 당근 중 축적량이 최대치를 나타내어 0.12 mg/kg를 나타내었으며, 다소 높은 지용성을 지닌 phenanthrene의 경우, 저농도 시비구, 15일차 시료에서 0.17 mg/kg의 잔류량을 보였다. 한편 높은 Koc 값을 지닌 PCB-126을 비롯한 다른 유사체의 축적 경향은 상기한 화합물과 다르게 나타났는 데, 예를 들어 PCB-126의 경우, 대략적으로 처리 후 60일 내외까지 급격한 농도증가를 나타내었고 이 후 완만한 상승 또는 감소하는 현상을 보였다. 또한 가장 높은 Koc (logKoc, 5.15)를 나타낸 2-(3,4,5-trichlorophenyl)-naphthalene은 실험 종료시까지 지속적으로 농도가 증가하였다. 반면 개별 당근에 흡수된 PCBs의 총량은 모든 처리구에 대하여 계속적으로 증대되었다. 이와 같은 경향은 당근 등의 작물은 일반적으로 재배기간 중 지속적 비대생장을 하여 축적된 오염물의 희석효과를 나타낸다는 기존 연구와 일치하였다(Low et al., 2009).
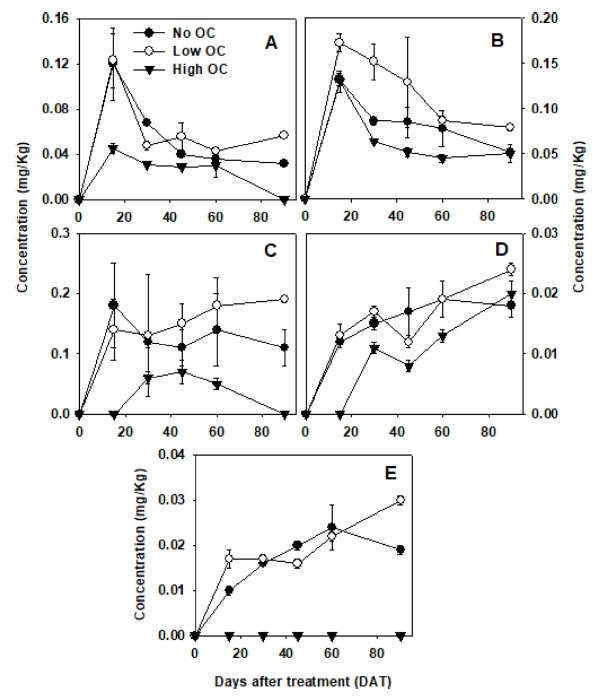
Accumulation of test chemicals (A) biphenyl, (B) phenanthrene, (C) PCB-126, (D) 3,4,5-trichloro-3',4'-dimethylbiphenyl and (E) 2-(3,4,5-trichlorophenyl)naphthalene in carrot from the soil with no (no OC), low (low OC), and high amount of amendments (high OC) of organic fertilizer.
한편 재배토양 중 유기질 시비의 함량과 당근 중 농도간 상관관계는 토양과는 상이한 경향을 나타내었다. 토양의 경우, 유기질 시비가 오염물질의 분해/소실을 촉진하거나 낮은 유의성의 상관관계를 나타낸 반면, 당근의 경우, 저농도 시비에서는 무시비구와 비교하여 오염물질의 축적을 촉진한 반면, 고농도 처리구의 경우 일반적으로 당근 중 축적되는 농도가 낮은 것으로 나타났다(Figs. 2 and 3). 유기질 비료의 시비에 의한 농약의 토양중 이행성은 상반된 결과를 나타내는 경우가 있는데, 토양입자에 대한 흡착의 증가와 생분해의 지연을 예로 들 수 있다(Briceno et al., 2007). 그러나 한편으로 유기물의 증가에 의하여 토양입자의 응결과 통기성 및 이행성에 큰 영향을 주는 대형 공극의 감소를 수반하여 농약 등의 오염물이 표토에 잔류하는 시간이 증대되고 이에 따라 미생물 분해가 촉진되는 경우도 보고되고 있다(Cox et al., 2001). 유기질 비료에 존재하는 유기물은 분해가 완전히 진행되지 않은 다량의 불용성 물질과 부식질 및 토양 용수의 성질에 따라 용리 가능한 가용성유기물(dissolved organic matter, DOM)으로 나눌 수 있다. 토양 중 DOM 함량이 증가하면 일반적으로 유기물의 용탈속도 역시 증가한다고 알려져 있다(Li et al., 2005). 이와 같은 현상은 DOM에 의하여 토양입자에 흡착된 유기물이 공극수 등 토양 수분에 용리되기 때문이며 해당물질의 작물 흡수를 촉진할 수 있다. 본 연구 중, 저농도 시비구 당근의 화합물 농도가 높은 것은 이와 같은 원인에 따른 것으로 해석할 수 있다. 한편 연구대상물질 중 비교적 높은 Koc를 지닌 PCB-126 등의 화합물의 경우, 당근 중 초기 농도는 시비량과 유의성 있는 상관관계를 나타내지 않았으나 재배일수의 경과에 따라 고농도 시비구 당근의 축적량이 저농도 시비구 및 무비구와 비교하여 낮게 나타났다(Fig. 3). 이와 같은 현상은 처리된 유기질 비료 중의 DOM이 재배 초기에는 다량 존재하여 토양입자 중 화합물의 가용화를 촉진하였지만 경과시간에 따라 DOM의 함량이 감소하고 불용성 유기잔사 또는 humin 등의 부식질이 축적됨에 따라 처리물질의 토양 흡착이 다시 촉진된 것이 원인으로 보인다.
Biphenyl 및 PCB congener의 당근-토양간 이행
당근-토양 중 biphenyl 및 PCB-126 등 처리물질의 농도비(농축계수, bioconcentration factors, BCFs)는 실험 기간 중 지속적으로 증가하였다(Fig. 4). 그러나 시비량과 화합물의 종류에 따라 예외적인 반응을 나타내는 경우도 관찰되었다. Biphenyl 및 phenanthrene 등의 Koc 값이 비교적 낮은 물질의 경우, 90일 경과 시료의 경우, BCFs는 1.2-1.5 내외로 상기한 바와 같이 경과시간에 따라 지속적으로 완만한 상승을 나타내었다. 한편 매우 큰 Koc를 지닌 2-(3,4,5-trichlorophenyl)naphthalene은 고농도 시비구의 경우, 당근으로의 이행이 관찰되지 않아 농축계수가 낮게 나타났다(BCF=0). PCB congener 중 독성계수(toxicity equivalent, TEQ)가 가장 큰 PCB-126의 경우, 시비량에 따라 BCF는 0-0.25로 나타났다. 이와 같은 값은 Aroclor를 이용한 Iwata 등의 연구에서 보고된 0.04-0.8 과 잘 일치하는 것이었다(Iwata and Gunther, 1976). 한편 PAHs의 일종인 phenanthrene의 경우 0.8-1.2의 BCF 값을 나타내었으며, 다른 작물을 대상으로 한 기존 연구와 유사한 결과를 나타내었다(Jeelani et al., 2017; Khan et al., 2008). Aroclor중에 함유된 concenger의 작물 흡수이행계수는 congener의 logP와 양의 상관관계를 나타내지만, 이와 같은 관계가 성립되지 않는 사례도 보고되고 있다(Javorska et al., 2011). 또한 흡수된 PCB의 작물 심층부로의 이행성에 있어서도 상반된 연구결과가 관찰된 바 있다(Javorska et al., 2011).
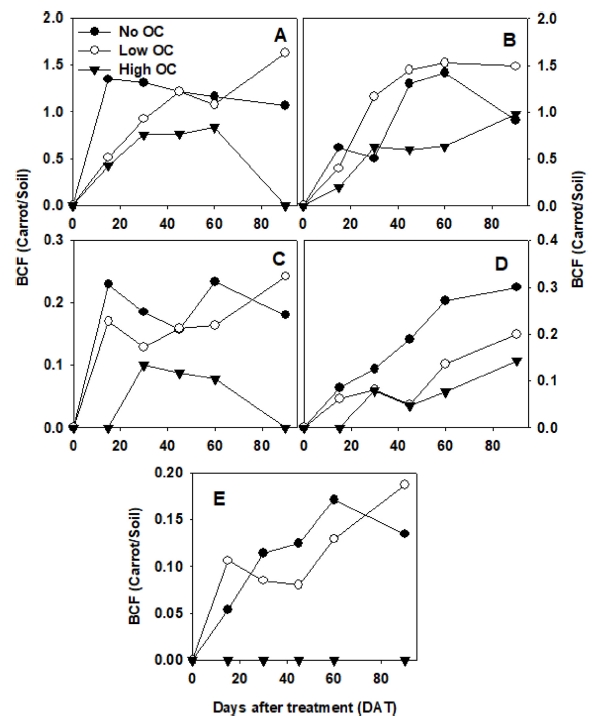
Bioconcentration factors (BCFs) of test chemicals (A) biphenyl, (B) phenanthrene, (C) PCB-126, (D) 3,4,5-trichloro-3',4'-dimethylbiphenyl and (E) 2-(3,4,5-trichlorophenyl)naphthalene between carrot and soils with no (no OC), low (low OC), and high amount of amendments (high OC) of organic fertilizer. BCFs = (Concentration (mg/kg) in carrot / concentration (mg/kg) in soil).
작물 중 오염물질의 농도는 본 연구 진행 중, 완만한 증대 또는 일부의 경우 감소하는 경우도 나타났지만 흡수물질의 총량은 전보와 동일하게 지속적으로 증가하였다(Lim et al., 2016). 90일 경과 후 당근의 평균 무게는 대략 180-300 g 내외로 측정되었으며, 이를 기준으로 측정한 오염물질의 총잔류량은 biphenyl (9-20 μg), phenanthrene (13-21 μg), PCB-126 (0-45 μg), 3,4,5-trichloro-3',4'-dimethylbiphenyl (5.4-7.2 μg) 및 2-(3,4,5-trichlorophe-nyl)naphthalene (0-7.2 μg)으로 나타났다. 이와 같은 흡수량은 토양처리 화합물의 총량기준 0-0.1%이었다.
본 연구 결과를 종합하면 작물 재배 중 유기질 퇴비의 시비는 시비량에 따라 매우 상이한 결과를 나타내어 저농도 시비의 경우, 가용성 유기물의 함량 증대와 이에 따른 토양용액 중 오염물의 농도를 증대하고, 작물 중 흡수를 촉진하는 반면, 고농도 시비의 경우, 토양 흡착 등의 생분해 및 이행을 저해하는 효과가 관찰되었다. 따라서 오염 토양에서의 작물 재배에 있어 유기질 시비는 시비량, 유기질 시비의 화학적 특성 등의 사항을 세부적으로 고려하여 실시되어야 할 것으로 사료된다.
Acknowledgments
본 연구는 농촌진흥청의 연구개발비(작물 재배환경 중 유해화학물질의 안전관리기준 설정 연구, 과제번호 PJ011435)로 수행되었으며 이에 감사드립니다.
Literature Cited
-
Abramowicz, D. A., (1995), Aerobic and anaerobic PCB biodegradation in the environment, Environ. Health. Perspect, 103, p97-99.
[https://doi.org/10.2307/3432489]

- Ahmad, R., Kookana, R. S., A. M. Alston, and J. O. Skjemstad, (2001), The nature of soil organic matter affects sorption of pesticides, 1. relationships with carbon chemistry as determined by 13C CPMAS NMR spectroscopy. Environ. Sci. Technol, 35, p878-884.
-
Allen-King, R. M., P. Grathwohl, and W. P. Ball, (2002), New modeling paradigms for the sorption of hydrophobic organic chemicals to heterogeneous carbonaceous matter in soils, sediments, and rocks, Adv. Water Resour, 25, p985-1016.
[https://doi.org/10.1016/s0309-1708(02)00045-3]

-
Awasthi, N., Kumar, A., R. Makkar, and S. S. Cameotra, (1999), Biodegradation of soil.applied endosulfan in the presence of a biosurfactant, J. Environ. Sci. Health B, 34, p793-803.
[https://doi.org/10.1080/03601239909373226]

-
Badea, S. L., Mustafa, M., S. Lundstedt, and M. Tysklind, (2014), Leachability and desorption of PCBs from soil and their dependency on pH and dissolved organic matter, Sci. Total. Environ, 499, p220-227.
[https://doi.org/10.1016/j.scitotenv.2014.08.031]

- Bollag, J. M., C. J. Myers, and R. D. Minard, (1992), Biological and chemical interactions of pesticides with soil organic matter, Sci. Total Environ, 123-124, p205-217.
- Briceno, G., G. Palma, and N. Duran, (2007), Influence of organic amendment on the biodegradation and movement of pesticides, Crit. Rev. Environ. Sci. Technol, 37, p233-271.
-
Cox, L., Cecchi, A., Celis, R., Hermosin, M., W. Koskinen, and J. Cornejo, (2001), Effect of exogenous carbon on movement of simazine and 2,4-D in soils, Soil Sci. Soc. Am. J, 65, p1688-1695.
[https://doi.org/10.2136/sssaj2001.1688]

-
Dean, J. R., I. J. Barnabas, and S. P. Owen, (1996), Influence of pesticide-soil interactions on the recovery of pesticides using supercritical fluid extraction, Analyst, 121, p465-468.
[https://doi.org/10.1039/an9962100465]

-
Frankki, S., Persson, Y., M. Tysklind, and U. Skyllberg, (2006), Partitioning of CPs, PCDEs, and PCDD/Fs between particulate and experimentally enhanced dissolved natural organic matter in a contaminated soil, Environ. Sci. Technol, 40, p6668-6673.
[https://doi.org/10.1021/es0608850]

-
Furukawa, K., and F. Matsumura, (1976), Microbial metabolism of polychlorinated biphenyls. Relative degradability of polychlorinated biphenyl components by Alkaligenes species, J. Agric. Food Chem, 24, p251-256.
[https://doi.org/10.1021/jf60204a002]

-
Gao, Y., Xiong, W., Ling, W., X. Wang, and Q. Li, (2007), Impact of exotic and inherent dissolved organic matter on sorption of phenanthrene by soils, J. Hazard. Mater, 140, p138-144.
[https://doi.org/10.1016/j.jhazmat.2006.06.053]

-
Gawlik, B. M., Sotiriou, N., Feicht, E. A., S. Schulte-Hostede, and S. A. Kettrup, (1997), Alternatives for the determination of the soil adsorption coefficient, KOC, of non-ionicorganic compounds - a review, Chemosphere, 34, p2525-2551.
[https://doi.org/10.1016/s0045-6535(97)00098-2]

-
Haritash, A. K., and C. P. Kaushik, (2009), Biodegradation aspects of polycyclic aromatic hydrocarbons (PAHs): A review, J. Hazard. Mater, 169, p1-15.
[https://doi.org/10.1016/j.jhazmat.2009.03.137]

-
Hiller, E., Cernansky, S., Z. Krascsenits, and J. Milicka, (2009), Effect of soil and sediment composition on acetochlor sorption and desorption, Environ. Sci. Pollut. Res, 16, p546-554.
[https://doi.org/10.1007/s11356-009-0113-9]

-
Huang, X., and L. S. Lee, (2001), Effects of dissolved organic matter from animal waste effluent on chlorpyrifos sorption by soils, J. Environ. Qual, 30, p1258-1265.
[https://doi.org/10.2134/jeq2001.3041258x]

-
Iwata, Y., and F. A. Gunther, (1976), Translocation of the polychlorinated biphenyl Aroclor 1254 from soil into carrots under field conditions, Arch. Environ. Contam. Toxicol, 4, p44-59.
[https://doi.org/10.1007/bf02221014]

- Javorska, H., P. Tlustos, and R. Kaliszova, (2011), Distribution of polychlorinated biphenyl congeners in root vegetables, Pol. J. Environ. Stud, 20, p93-99.
-
Jeelani, N., Yang, W., Xu, Li, Qiao, Y., A. Shuqing, and X. Leng, (2017), Phytoremediation potential of Acorus calamus in soils co-contaminated with cadmium and polycyclic aromatic hydrocarbons, Sci. Rep, 7, p8028.
[https://doi.org/10.1038/s41598-017-07831-3]

-
Juraske, R., Castells, F., Vijay, A., P. Munoz, and A. Anton, (2009), Uptake and persistence of pesticides in plants: measurements and model estimates for imidacloprid after foliar and soil application, J. Hazard. Mater, 165, p683-689.
[https://doi.org/10.1016/j.jhazmat.2008.10.043]

-
Khan, S., Aijun, L., Zhang, S., Q. Hu, and Y. G. Zhu, (2008), Accumulation of polycyclic aromatic hydrocarbons and heavy metals in lettuce grown in the soils contaminated with long-term wastewater irrigation, J. Hazard. Mater, 152, p506-515.
[https://doi.org/10.1016/j.jhazmat.2007.07.014]

- Kim, H. S., and F. K. Pfaender, (2005), Effects of microbially mediated redox conditions on PAH-soil interactions. Environ, Sci. Techn, 39, p9189-9196.
-
Li, K., B. Xing, and W. A. Torello, (2005), Effect of organic fertilizers derived dissolved organic matter on pesticide sorption and leaching, Environ. Pollut, 134, p187-194.
[https://doi.org/10.1016/j.envpol.2004.08.011]

-
Lim, D. H., D. S. Lim, and Y. S. Keum, (2016), Translocation of polychlorinated biphenyls in carrot-soil systems, Kor. J. Pestic. Sci, 20, p203-210.
[https://doi.org/10.7585/kjps.2016.20.3.203]

- Low, J. E., A. M. L. Whitfield, A. Rutter, and B. A. Zeeb, (2009), Effect of plant age on PCB accumulation by Cucurbita pepo ssp. pepo, J. Environ. Qual, 39, p245-250.
-
Motoki, Y., Iwafune, T., Seike, N., T. Otani, and M. Asano, (2014), Effects of organic carbon quality on the sorption behavior of pesticides in Japanese soils, J. Pestic. Sci, 39, p105-114.
[https://doi.org/10.1584/jpestics.d13-067]

-
Motoki, Y., T. Iwafune, N. Seike, K. Inao, and T. Otani, (2016), Effect of time-dependent sorption on the dissipation of water-extractable pesticides in soils, J. Agric. Food Chem, 64, p4478-4486.
[https://doi.org/10.1021/acs.jafc.6b01028]

-
Niederer, C., R. P. Schwarzenbach, and K. U. Goss, (2007), Elucidating differences in the sorption properties of 10 humic and fulvic acids for polar and nonpolar organic chemicals, Environ. Sci. Technol, 41, p6711-6717.
[https://doi.org/10.1021/es0709932]

-
Persson, Y., K. Hemstrom, L. Oberg, M. Tysklind, and A. Enell, (2008), Use of a column leaching test to study the mobility of chlorinated HOCs from a contaminated soil and the distribution of compounds between soluble and colloid phases, Chemosphere, 71, p1035-1042.
[https://doi.org/10.1016/j.chemosphere.2007.12.008]

- Sabljic, A., and Y. Nakagawa, (2014), Biodegradation and quantitative structure-activity relationship (QSAR), In Chen, W., Sabljic, A., Cryer, S.A., Kookana, R.S. (eds), ACS symposium series vol 1174 Non-first order degradation and time-dependent sorption of organic chemicals in soil, Washington DC,, American Chemical Society, p57-84.
-
Sachdev, D. P., and S. S. Cameotra, (2013), Biosurfactants in agriculture, Appl. Microbiol. Biotechnol, 97, p1005-1016.
[https://doi.org/10.1007/s00253-012-4641-8]

-
Seth, R., D. Mackay, and J. Muncke, (1999), Estimating the organic carbon partition coefficient and its variability for hydrophobic chemicals, Environ. Sci. Technol, 33, p2390-2394.
[https://doi.org/10.1021/es980893j]

-
Zhu, D., S. Hyun, J. J. Pignatello, and L. S. Lee, (2004), Evidence for π-π electron donor-acceptor interactions between π-donor aromatic compounds and π-acceptor sites in soil organic matter through pH effects on sorption, Environ. Sci. Technol, 38, p4361-4368.
[https://doi.org/10.1021/es035379e]