LC-MS/MS를 이용한 살충제 톨펜피라드의 잔류시험법 개발 및 검증
초록
살충제 톨펜피라드는 2018년 잔류허용기준이 신설될 예정이므로 안전성 확보를 위해 잔류물의 정의를 모화합물로 규정하여 LC-MS/MS를 이용한 공정시험법을 개발하였다. 본 연구에서는 톨펜피라드를 대표농산물 6종(감귤, 감자, 고추, 현미, 대두, 아몬드)에 적용하여 시료의 침투성을 높이기 위해 아세토니트릴을 사용하여 추출하고, 디클로로메탄을 이용해 극성 간섭물질을 분리하였다. 현미와 대두는 헥산/아세토니트릴 분배법을 추가 적용하여 유지와 비극성 간섭물질을 제거하였다. 플로리실 카트리지를 이용해 정제를 최적화하여 시험법을 확립하였다. 확립된 시험법은 검출한계, 정량한계, 선택성, 직선성 및 회수율 시험을 통해 실험실내 및 실험실간 검증을 수행하여 공정시험법으로 유효성을 입증하였다. 개발된 시험법의 검출한계와 정량한계가 각각 0.001, 0.005 mg/kg이었고, 회수율은 77.4-104.5%, 변이계수(CV)는 7.9% 이하였다. 이는 잔류물 분석에 관한 CODEX 가이드라인(CAC/GL 40)과 식품의약품안전평가원의 가이드라인(2016)에 만족하여 국내에 유통되는 농산물 중 톨펜피라드의 안전관리를 위한 공정시험법으로 사용되기에 적합할 것으로 판단된다.
Abstract
The analytical method developed for the determination of tolfenpyrad in alomond, walnut, pistachio. The tolfenpyrad residues in samples extracted by using acetonitrile and partitioned with dichloromethane, and then purified with Florisil solid phase extraction (SPE) cartridge to clean up. The analytes quantified and confirmed by using liquid chromatograph-tandem mass spectrometer (LC-MS/MS) in positive ion mode using multiple reaction monitoring (MRM). Matrix matched calibration curves were linear over the calibration rages (0.001-0.25 μg/mL) into a blank extract with r2 > 0.99. For validation, recovery studies carried out at three different concentration levels (LOQ, 10LOQ, and 50LOQ), performing five replicates at each level. The recoveries ranged between 72.7 to 100.2%, with relative standard deviations (RSDs) less than 9.7% for all analytes. All values were consistent with the criteria ranges requested in the Codex guidelines (CAC/GL40, 2003) and NIFDS (national institute of food and drug safety evaluation) guideline (2016). The proposed analytical method was accurate, effective and sensitive for tolfenpyrad determination in agricultural commodities.
Keywords:
Agricultural commodity, analytical method, insecticide, LC-MS/MS, tolfenpyrad키워드:
농산물, 분석법, 살충제, 톨펜피라드, 잔류농약서론
농약은 농작물의 재배기간 동안 발생하는 해충, 병, 식물 생장 조절 및 잡초 방제로부터 농작물을 보호하고 농산물의 품질 향상 등 다양한 용도로 인류의 생활 여건에 광범위하게 사용되는 중요한 농업용 자재이다. 그러나 농약은 식물의 생리활성 작용을 저해하는 역할을 하므로 독성을 가질 가능성이 있다. 또한 농작물에 살포되었을 때, 살포된 농약의 특성과 환경에 따라 독성이 잔류 될 가능성이 있으며, 잔류되는 양이 많고 계속 섭취할 경우, 체내에 축적되어 만성독성을 유발할 수 있는 위해성에 대한 불안감을 갖는 소비자들이 증가하고 있어 잔류하는 농약에 대한 섭취량과 기준에 대한 관리가 필요하다(Lee et al., 2010; Kim et al., 2014; Kim et al., 2010; Lee et al., 2008). 이에 따라 세계 각국에서는 각국의 농산물 및 식품에 대한 잔류농약의 안전성을 평가하고, 잔류허용기준(maximum residue limit, MRL)을 설정하여 규제를 하고 있다. 우리나라 또한 안전성 확보를 위해 잔류물의 정의와 잔류허용기준을 설정하고 잔류농약 시험법을 매년 제·개정하고 있으며, 2018년 3월 현재 농산물 중 466종의 농약과 축산물 중 84종의 농약에 대한 잔류허용기준을 설정하여 관리하고 있다(Ministry of Food and Drug Safety, 2018).
톨펜피라드(Tolfenpyrad)는 국내에 수입되는 농산물인 아몬드, 피스타치오, 호두에 대하여 2017년에 잔류허용기준 신설이 요청된 농약이다. 1991년 일본 미츠비시화학 주식회사(Mitsubishi Chemical Corporation)에서 개발한 살충제로 채소, 교목성 과일 및 기타 작물의 응애, 총채벌레, 나방 등의 살충하기 어려운 해충에 살충효과가 크며, 알, 유충, 애벌레 및 성층 단계의 해충에 직접 접촉 작용하고 기존의 살충제와 교차 저항을 보이지 않는다(Song et al., 2012; Okada et al., 1999). 톨펜피라드의 물질대사 연구 결과에 따르면 주요 대사산물로 OH-PT가 생성되나 작물잔류성시험을 통해 농산물 중 잔류 가능성이 없는 것으로 확인되어 국내에서는 잔류물의 정의를 모화합물로만으로 규정하고자 하였다(Ministry of Food and Drug Safety, 2016). 국제식품규격위원회(CODEX Alimentarius Commission, CAC), 미국(EPA) 및 일본(FSC)에서도 잔류물의 정의를 모화합물로 정하여 관리하고 있으며, 잔류허용기준은 0.01-70.0 mg/kg으로 설정하여 관리하고 있다(CAC., 2015; EPA., 2016; MHLW., 2016). 톨펜피라드 시험법은 GC-MS/MS를 이용한 다성분시험법과 LC 분석법 등이 보고된 바가 있으나 국내의 경우 수입되는 견과류(아몬드, 피스타치오, 호두)에 대한 시험법이 마련되지 않아 톨펜피라드의 안전관리를 위한 시험법 개발이 필요하다(Yamaguchi K., 2012; Zou N., 2016; Wang J., 2012).
따라서 본 연구에서는 견과류 외에도 향후 곡류, 채소류 등 다른 농산물에 잔류할 가능성을 고려하여 모든 농산물에서 잔류량을 확인할 수 있도록 대표 농산물 6종(감귤, 감자, 고추, 대두, 현미, 아몬드)에 대하여 선택성 및 감도가 우수한 LC-MS/MS를 이용하여 톨펜피라드의 공정시험법을 개발하고자 하였다.
재료 및 방법
시약 및 재료
톨펜피라드(순도 98%) 표준품은 Wako(Osaka, Japan)에서 구입하여 사용하였고, 아세토니트릴(acetonitrile), 디클로로메탄(dichloromethane), 헥산(hexane) 등은 HPLC 등급으로 Merck(Darmstadt, Germany)에서 구입하여 사용하였다. 염화나트륨은 Wako(Osaka, Japan), 무수황산나트륨은 Merck(Darmstadt, Germany)에서 구입하여 사용하였다. 또한 SPE 카트리지(1 g, 6 cc)는 Waters(Milford, USA) 제품을 구입하여 사용하였다. 검체는 식물성 원료로 분류된 대표농산물 5종인 감귤(과일류, mandarin), 감자(서류, potato), 고추(채소류, green and red pepper), 대두(두류, soybean), 현미(곡류, hulled rice)와 기준 신설 예정인 아몬드(견과류, almond)를 포함하여 모두 무농약 농산물을 구입하여 균질화한 후 밀봉된 용기에 담아 -50℃에 보관하여 실험에 사용하였다.
표준원액 및 표준용액의 조제
톨펜피라드(순도 98%) 표준품 20.41 mg을 20 mL의 아세토니트릴에 용해하여 1,000 μg/mL의 표준원액을 조제하였다. 이를 시료 무처리 추출물로 희석하여 0.001, 0.005, 0.01, 0.05, 0.1 및 0.25 μg/mL로 조제하여 90% 이상의 무처리 추출물이 첨가된 표준용액을 조제하였다. 표준원액과 표준용액은 모두 갈색병에 담아 4℃에 보관하여 실험에 사용하였다.
추출 및 액액분배
검체를 분쇄하여 균질화한 후 10 g (과일류, 채소류, 서류 및 견과류는 약 1 kg을 분쇄한 후 10 g, 곡류 및 두류는 약 1 kg을 혼합하여 표준체 420 μm를 통과하도록 분쇄한 후 10 g)을 정밀히 달아 균질기 용기에 넣고 아세토니트릴 50 mL을 가하여 진탕기에서 10분간 진탕하였다. 여과지가 깔려있는 부흐너깔때기로 흡인여과한 뒤 아세토니트릴 20 mL로 잔사 및 용기를 씻어내려 앞의 여액과 합친 뒤 이를 40℃ 이하 수욕 상에서 감압 농축하였다. 농축 후 잔류물에 증류수 100 mL를 가하여 녹인 후 500 mL 용량의 분액여두에 옮긴 후 포화식염수 20 mL를 더한 뒤 디클로로메탄 30 mL를 차례로 가하고 심하게 흔들어 층이 완전히 분리될 때까지 정치시킨 후 디클로로메탄 층을 무수황산나트륨에 통과시켜 감압농축플라스크에 받는 과정을 2회 반복하였다. 이를 40℃ 이하의 수욕 상에서 감압하여 용매를 모두 날려버린 후, 잔류물에 디클로로메탄 10 mL를 가하여 최종부피를 10 mL가 되게 하였다. 다만, 지방성 검체(대두, 현미)의 경우 헥산 30 mL를 잔류물에 가하여 녹인 후 250 mL 분량의 분액여두에 옮기고 아세토니트릴 30 mL으로 2회 분배하여 추출하였다. 합친 아세토니트릴 층을 40℃에서 감압 농축한 후 잔류물에 디클로로메탄을 가하여 최종부피를 10 mL가 되게 하였다.
카트리지 정제
플로리실(Florisil) 카트리지에 디클로로메탄 10 mL를 2~3 방울/초의 속도로 유출하여 버린다. 이어서 고정상 상단이 노출되기 전에 추출액 중 5 mL를 카트리지 상단에 넣고 1~2 방울/초의 속도로 유출시켜 씻어 버린다. 디클로로메탄을 고정상 상단이 노출되기 전에 5 mL를 유출시켜 버린 뒤 아세톤/디클로로메탄 혼합용액(5/95, v/v) 10 mL를 용출시켜 받은 시험액을 감압농축플라스크에 취하였다. 이를 40℃ 이하 수욕상에서 감압농축하고 아세토니트릴을 가하여 최종 부피 5 mL가 되게 한 뒤 멤브레인 필터(nylon, 0.2 μm)로 여과한 후 시험용액으로 사용하였다.
LC-MS/MS 분석조건
톨펜피라드 분석을 위해 액체크로마토그래프-질량분석기(Liquid Chromatograph-Tandem Mass Spectrometer, Xevo TQ-S (Waters, MA, USA))를 사용하였다. 분석용 칼럼은 역상 칼럼으로 C18 칼럼을 선택하였고, 기울기 용리 방식은 0.1% 포름산 함유 아세토니트릴과 0.1% 포름산 수용액을 이동상으로 사용하였다. 분석성분의 이온화법으로는 electro-spray ionization(ESI)법의 positive-ion mode를 사용하였으며, LC-MS/MS의 분석조건은 Table 1과 같다.
시험법의 검증
본 연구는 ‘CODEX 가이드라인(CAC/GL 40)’과 식품의 약품안전처 식품의약품안전평가원의 ‘식품등 시험법 마련 표준절차에 관한 가이드라인(2016)’을 적용하여 시험법의 직선성(linearity), 검출한계(limit of detection, LOD), 정량한계(limit of quantification, LOQ), 회수율(recovery) 및 재현성(reproducibility)에 대한 유효성을 검증하였다(CAC., 2003; NIFDS., 2016). 직선성 확인을 위하여 톨펜피라드를 무처리 시료 시험용액으로 희석하여 조제한 표준 용액 0.001-0.25 μL의 농도범위에 대한 각각의 피크 면적을 이용하여 검량선을 작성하였고, 검량선의 결정계수(r2)를 구하였다. 또한 검출한계와 정량한계는 크로마토그램 상에서 신호대 잡음비(S/N ratio)를 각각 3, 10 이상으로 하였다. 시험법의 정확도 및 정밀도를 확인하기 위하여 무처리 시료에 톨펜피라드의 표준용액을 첨가한 후 분석하여 회수율을 확인하였다. 회수율 실험의 처리 농도는 정량한계, 정량한계 10배, 정량한계의 50배에 해당하는 농도로 수행하였으며, 각 농산물 검체의 처리구는 5반복으로 수행하여 평균과 상대표준편차(RSD, relative standard deviation)를 계산하여 시험법의 정확도 및 정밀도를 평가하였다.
결과 및 고찰
기기선정 및 분석조건 확립
톨펜피라드의 화학식은 C21H22ClN3O2로 분자 구조 내에 질소(nitrogen, N)를 포함하고 있어 질소를 선택적으로 검출할 수 있는 GC-NPD 분석이 가능할 것으로 판단되었다. 하지만 끓는점이 539.98℃ (760 mmHg)로 높으나 분해온도가 250℃이므로 톨펜피라드를 휘발시키기 전에 분해될 가능성이 있어 재현성이 낮아질 것으로 사료되었다. 따라서 톨펜피라드는 비공유 전자쌍과 이중결합의 전자 전이에 의해 UV-Vis에서 강한 흡광성을 나타내는 conjugation 결합이 있어 LC-UVD를 이용한 분석이 용이할 것으로 판단되었다. 이에 따라 특정 파장대를 흡수하는 특성을 이용하여 PDA(Photodiode Array)로 스캔(210~360 nm)한 결과 최적 파장인 232 nm를 확인할수 있었으므로, 이 파장에 대한 감도를 근거로 정량한계를 확인하였다. 확인한 농도 수준은 0.1 mg/kg으로 감도가 낮은 편으로 높은 감도를 요구하는 톨펜피라드의 정량한계를 만족시킬 수가 없어 기기상의 감도를 높이고, 시료에 존재하는 간섭물질로부터 선택적인 분리를 위해 액체크로마토그래프-질량분석기(LC-MS/MS)를 분석기기로 선정하였다(Lee, 2013). 분석용 칼럼은 톨펜피라드의 비극성(Log Pow=5.61)인 특성을 고려하여 비극성 물질과 극성물질 모두 분리가 가능한 C18 칼럼을 선택하였다. 이동상은 0.1% 포름산 함유 아세토니트릴과 0.1% 포름산 수용액을 이용한 기울기 용리 방식으로 분석하였다. 이동상에 쓰인 포름산은 톨펜피라드 분자의 [M+H]+ 이온 생성에 용이한 protonation enhancer로 작용하였다. 각 대상성분은 electro-spray ionization (ESI)법의 positive-ion mode를 사용하여 최적 특성이온을 선정하여 selected-ion monitoring(SIM)으로 분석하였다. Total ion chromatogram (TIC)과 mass spectrum을 통해 최적 특성이온을 선정하였다. 평균질량 383.9 (exact mass: 383.1403)인 톨펜피라드의 표준용액(0.1 μg/mL)을 일정한 속도(10 μL/min)로 질량검출기에 직접 주입한 결과 질량이 [M+H]+ 형태인 384.4 m/z 값을 확인하였다. 이 때 cone voltage의 변경(10-70 V)을 통해 40 V에서 최대의 peak 강도가 나타남을 확인하였다. 최적화된 cone voltage 상태에서 분석의 선택성과 검출강도를 극대화시키기 위하여 MS/MS 분석 시 MRM (multiple reaction monitoring) mode로 분석하였다. Collision cell에서 collision energy를 조절하여 최적의 precursor/product ion pair를 선정하였고, 가장 높은 감도를 보이는 product ion을 정량이온(quantification ion)으로, 다음으로 크게 검출되는 product ion을 정성이온(qualification ion)으로 설정하였다. 최적 기기분석 조건은 Table 1에 나타내었고, 분석조건에서 선정된 특성 이온과 머무름 시간은 Table 2에 나타내었다.
추출 및 분배조건 확립
톨펜피라드는 Log Pow 값이 5.61이며, pH 1.32-13.15 범위에서 비해리 상태로 존재하는 비극성 화합물이다. 대상 성분을 비극성 유기용매를 이용하여 추출과 분배를 할 수 있으나 시료 입자 표면이나 내부에 톨펜피라드가 존재할 수 있기 때문에 비극성 유기용매로 추출 시 시료 내부 침투성이 낮아 추출 효율이 낮을 것으로 사료되었다. 따라서 대표 농산물 6종에 대한 추출 용매는 수용성 유기용매를 이용하여 내부 침투성을 용이하게 하고 추출 효율을 높일 수 있는 추출조건을 확립하였다. 수용성 유기용매인 아세토니트릴은 다른 수용성 유기용매인 아세톤과 비교했을 때, 비극성 간섭물질의 추출률이 낮은 특성을 갖고 있으며, chlorophyll과 같은 고추, 대두 등의 색소 추출 효율이 낮아 추출용매로 적합한 것으로 판단되었다(Kown, 2008). 추출이 끝난 시료 추출액에 극성 간섭물질과 톨펜피라드 분리를 위한 액-액 분배법을 적용하였다. 액-액 분배 용매를 선정하기 위해 톨펜피라드의 물리·화학적 특성, 용매의 극성지수 및 용매에 대한 용해도를 고려하여 디클로로메탄을 선정하였다. 디클로로메탄은 비교적 비극성 유기용매이며, 디클로로메탄에 대한 용해도(> 500 g/L, 25℃)가 다른 비극성 유기용매에 비해 높아 분배 효율이 높을 것으로 판단되었다. 또한 액-액 분배과정에 포화식염수를 첨가하여 명확한 층 분리를 통해 분배효과를 증대시키고, 극성 간섭물질이 디클로로메탄 층으로 전이되는 것을 최소화하였다. 다만 유지함량이 2% 이상인 곡류, 두류 및 견과류는 헥산/아세토니트릴 분배법을 추가로 적용하여 유지와 비극성 불순물 제거를 통해 matrix effect를 최소화 할 수 있을 것으로 판단하여 회수율을 확인하였다. 그 결과 대표농산물 6종에 대한 회수율이 72.7% 이상의 높은 효율을 나타내었다(Table 5).
카트리지 정제법 확립
분배 과정이 끝난 분배액은 톨펜피라드의 손실을 줄이고, 보다 우수한 정제효과를 얻기 위하여 고체상 추출법(Solid phase extraction, SPE) 중 흡착제에 대한 친화도의 차이를 이용하는 흡착 카트리지 중 Silica, Florisil 및 HLB 카트리지를 사용하여 회수율을 비교하였다. 정제에 사용된 Silica 카트리지는 극성 순상 흡착제로서 탄화수소나 염소, 플루오르가 치환된 탄화수소와 같이 비극성 용매 또는 극성이 덜한 에스테르 및 에테르로부터 분석물질을 용출하며, 아세토니트릴 또는 물과 같은 극성이 더 강한 용매로 분석물질을 용출하는 특성을 갖고 있다. Florisil 카트리지는 주로 유기용매로부터 극성부터 중간 극성물질의 분석에 주로 사용되며, AOAC 및 EPA의 분석법을 이용한 농약분석을 위해 많이 사용 되는 카트리지이다(Park, 2011). Silica 카트리지와 Florisil 카트리지는 이와 같이 순상 카트리지로 극성 물질을 분리하는 특성이 있으나 용출하는 유기용매의 특성을 이용하여 용매를 조합할 경우 비극성 분석 물질을 분리할 수 있다. HLB 카트리지는 hydrophilic N-vinylpyrrolidone과 lipophilic divinylbenzene을 함유하는 역상 카트리지로서, 친수성이 강한 성분들은 카트리지에서 쉽게 용출되지만, 방향족 고리나 탄소수가 4개 이상인 카르복실 산을 함유하는 화합물은 흡착되는 원리를 이용한 카트리지이다(Son, 2015).
톨펜피라드는 Log Pow값이 5.61로 비극성 물질로써 이 점을 고려하여 에틸아세테이트/헥산, 디클로로메탄/헥산 및 아세톤/디클로로메탄의 혼합액으로 정제효율을 비교하였다. 에틸아세테이트/헥산과 디클로로메탄/헥산의 혼합액에서 Florisil, Silica, HLB 카트리지 모두 회수율이 26.1-75.7%로 낮은 회수율을 보여 정제 용매로 사용할 수 없었다. 두 용매조합에서 비극성 용매로 사용된 헥산은 비극성인 톨펜피라드를 용출시키기에 적합할 것으로 판단하였으나, 톨펜피라드는 헥산에 대한 용해도(7.41 g/L)가 상대적으로 낮기 때문에 흡착카트리지의 활성기에 흡착된 톨펜피라드가 용매와의 경쟁적 친화력이 낮아 용출이 모두 되지 않은 것으로 판단하였다. 반면, 아세톤/디클로로메탄의 혼합액에서의 각 카트리지별 회수율을 확인한 결과 Florisil 카트리지에서 97%, Silica 카트리지에서 89.6%, HLB 카트리지에서 91.5%의 회수율이 확인되었다(Table 3). 그 중 가장 높은 회수율이 확인 된 Florisil 카트리지를 정제 카트리지로 우선 적용하였고, 정제조건을 최적화하기 위해 용매 조성을 세분화하여 추가 실험을 하였다. 아세톤/디클로로메탄 혼합액(100, 5/95, 90/10/ 80/20, v/v)을 세분화하여 각 용매 조성에 대해 5 mL씩 4개의 분획을 받아 확인한 결과, 아세톤/디클로로메탄 혼합액(5/95, v/v) 10 mL에서 가장 높은 회수율을 보여 최적의 정제용매로 선정하였다. 따라서 최종 정제법은 디클로로메탄으로 재용해한 추출액 10 mL 중 간섭물질 최소화를 위해 5 mL를 카트리지에 유출시킨 후 디클로로메탄 5 mL로 씻어버리고 아세톤/디클로로메탄 혼합액(5/95, v/v) 10 mL로 용출시키는 방법으로 정제 효율을 높여 적용하였다(Table 4).
시험법의 검증
선택성 및 직선성
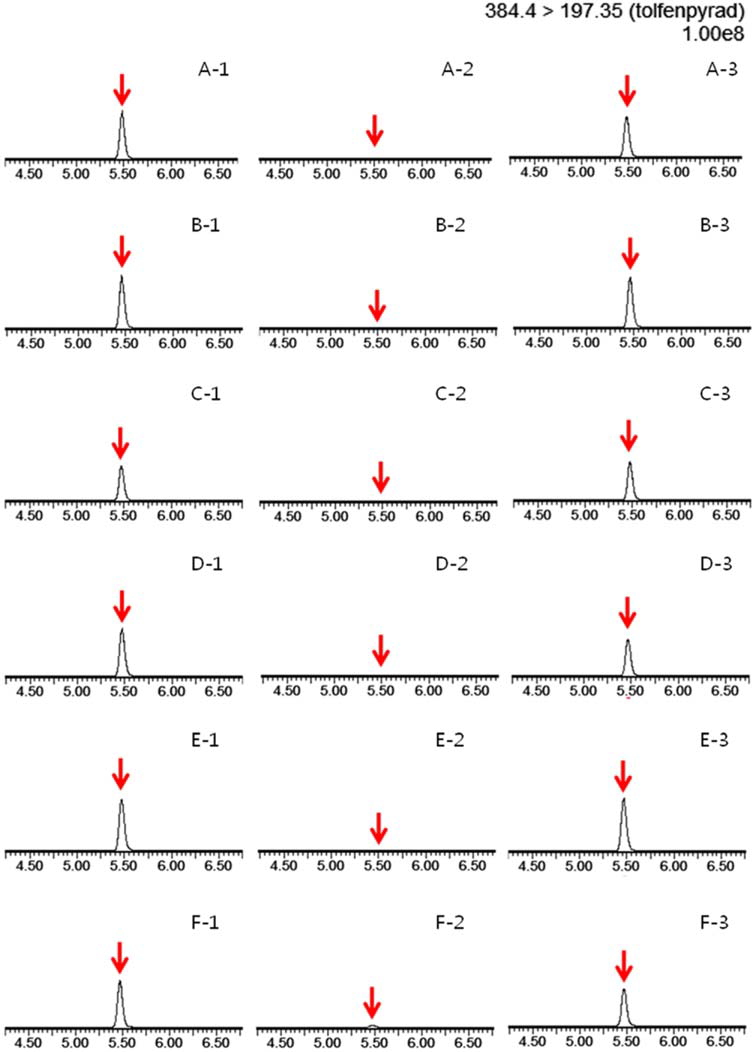
톨펜피라드는 표준용액, 무처리 시료, 표준용액을 첨가한 회수율 시료의 크로마토그램을 서로 비교, 평가하여 선택성(selectivity)을 확인하였다. 무처리 시료 중 톨펜피라드의 머무름 시간과 질량 대 전하비(m/z)가 같은 간섭물질은 검출되지 않아 본 시험법은 대상물질을 분석하는 것에 있어 높은 분리능과 선택성(selectivity)을 확보하였다.
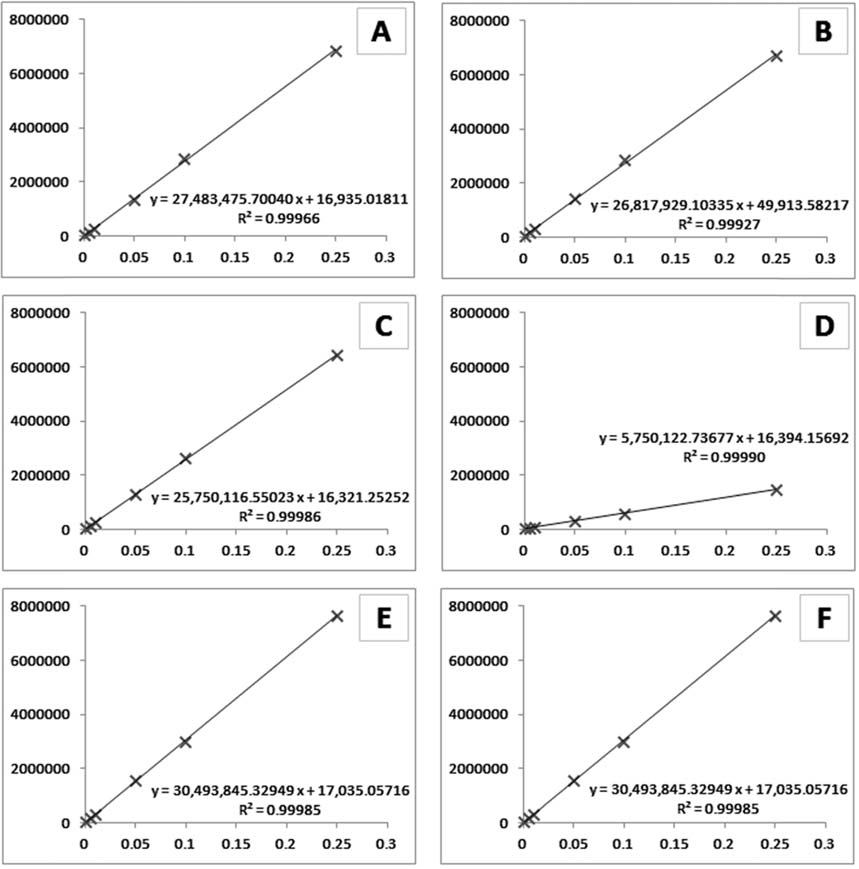
개발된 시험법의 직선성(linearity)을 확인하기 위해 표준원액을 무처리 추출물로 희석하여 0.001, 0.005, 0.01, 0.05, 0.1 및 0.25 μg/mL 1 μL를 LC-MS/MS에 주입하여 분석한 결과, 모든 농산물 시료 표준용액에서 결정계수(r2) 0.99 이상으로 높은 직선성을 보여주었다(Fig. 1).
검출한계와 정량한계
톨펜피라드의 검출한계는 기기의 크로마토그램 상에서 신호 대 잡음비(S/N ratio)를 3 이상으로 결정하였다. 농산물 시료 6종의 경우 분석기기의 최소검출량은 0.001 ng으로 아래의 계산식에 따라 검출한계는 0.001 mg/kg이었고, 정량한계는 신호 대 잡음비(S/N ratio)가 10 이상인 0.005 mg/kg으로 아래의 계산식에 나타내었다.
- *희석배수 = 총 용량(mL)/취한 용량(mL)
실험실내 검증
시험법의 정확도 및 정밀도를 평가하기 위하여 감귤, 고추, 감자, 대두, 현미 및 아몬드에 LOQ, 10 × LOQ, 50 × LOQ 농도 수준인 0.005, 0.05 및 0.25 mg/kg의 농도로 5회 반복하여 회수율 실험을 진행하였다. 그 결과 각 농도에서 톨펜피라드의 평균 회수율은 72.7~100.2%였고, 상대표준편차는 9.6% 이하로 조사되었다. 이 결과는 잔류물 분석에 관한 CODEX 가이드라인(CAC/GL 40, 2003)과 식약처 식품의약품안전평가원의 ‘식품등 시험법 마련 표준절차에 관한 가이드라인(2016)을 통해 처리농도 >1 μg/kg, ≤10 μg/kg일때, 회수율 범위 60~120%, 변이계수(CV)는 32%, >10 μg/kg, ≤100 μg/kg일 때, 회수율 범위 70~120%, CV값 22%, >100 μg/kg, ≤1000 μg/kg일 때, 회수율 범위 70~120%, CV값 18%로 두 기관의 잔류농약 분석 기준에 부합한 것으로 확인되었다. 따라서 본 연구에서 개발한 추출 및 정제 방법이 농산물 중 잔류하는 톨펜피라드를 분석하기에 두 가이드라인에 부합하는 것을 확인하였다(Table 5). LC-MS/MS를 이용한 농산물 시료 중 톨펜피라드의 회수율 크로마토그램을 Fig. 2에 제시하였다.
실험실간 검증
본 연구에서 개발한 시험법은 시험법의 유효성을 검증하기 위하여 서울지방식품의약품안전청 수입식품분석과와 실험실간 검증을 수행하였다. 개발한 시험법을 서울지방식품의약품안전청에 동일하게 제공하여 분석한 회수율 및 표준편차를 비교하여 확인한 결과 각 농도에서 회수율은 71.4~120.0%, 표준편차는 10.0% 이하였다. 두 실험실간의 평균회수율은 77.4~104.5%이고, 변이계수(CV %)는 7.9% 이하로 확인하였다. 따라서, CODEX 가이드라인(2003)과 식품의약품안전평가원의 가이드라인(2016)에서 제시한 실험실간 검증 기준은 처리농도 1 μg/kg, ≤10 μg/kg의 46%, >10 μg/kg, ≤100 μg/kg의 34%, >100 μg/kg, ≤1000 μg/kg의 25%에 만족하여 모든 처리농도에서 두 가이드라인에 부합한 것을 확인하였다(Table 5). 따라서 본 연구에서 확립한 시험법은 식품공전에 수록하여 잔류허용기준을 통한 안전관리를 위한 시험법으로 적합할 것으로 확인된다.
Acknowledgments
본 연구는 식품의약품안전평가원 “2017년 식품 중 잔류농약 안전관리를 위한 위해평가 및 신규 시험법 확립 연구(17161식위안001)”의 연구개발비 지원에 의해 수행되었으며, 이에 감사드립니다.
Literature cited
- CAC (Codex Alimentarius Commission), (2003), Guidelines on good laboratory practice in residue analysis, CAC/GL 40-1993.
- CAC (Codex Alimentarius Commission), (2015), Pesticide residue in food and feed, http://www.fao.org/fao-sho-codexalimentarius/standards/pestres/pesticide/en.
- EPA, (2016), United states Environmental Protection Agency. http://www.ecfr.gov/cgibin/retrieveECFR?gp=&SID=596ee9062eb78954e2206dcb840d28fd&mc=true&n=pt40.26.180&r=PART&ty=HTML#se40.26.180_1675.
-
Kim, J. Y., S. M. Lee, H. J. Lee, M. I. Chang, N. S. Kang, N. S. Kim, H. J. Kim, Y. J. Cho, J. Y. Jeong, M. K. Kim, and G. S. Rhee, (2014), Monitoring and risk assessment of pesticide residues for circulated agriculutral commodities in korea-2013, J. Korean Soc. Appl. Biol. Chem., 57(3), p235-242.
[https://doi.org/10.3839/jabc.2014.037]

- Kim, M. O., H. S. Hwang, M. S. Lim, J. E. Hong, S. S. Kim, J. A. Do, D. M. Choi, and D. H. Cho, (2010), Monitoring of residueal pesticides in agricultural products by LC/MS/MS, Korean J. Food Sci. Technol., 42(6), p664-675.
- Kwon, C. H., M. I. Chang, M. H. Im, H. Choi, D. I. Jung, S. C. Lee, J. Y. Yu, Y. D. Lee, J. O. Lee, and M. K. Hong, (2008), Determination of mandipropamid residues in agricultural commodities using high-performance liquid chromatography with mass spectrometry, J. Anal. Sci. Technol., 21(6), p518-525.
- Lee, J. H., H. W. Park, Y. S. Keun, C. H. Kwon, Y. D. Lee, and J. H. Kim, (2008), Dissipation pattern of boscalid in cucumber under greenhouse condition, Korean J. Pestic. Sci., 12(1), p67-73.
- Lee, J. Y., W. J. Choe, H. J. Lee, Y. W. Shin, J. A. Do, W. S. Kim, D. M. Choi, K. R. Chae, and C. S. Kang, (2010), Research on pesticides residue in commercial agricultural products in 2009, J. Food Hyg. Saf., 25(2), p192-202.
- Lee, Y. D., (2013), Practical book of Korea Food Code pesticide residue analysis method, 4th ed, MFDS, Cheongju, Korea, p78-79.
- Ministry of Food and Drug Safety (MFDS), (2016), MFDS notice 2017-57.
- Ministry of Food and Drug Safety (MFDS), (2016), Tolfenpyrad safety evaluation report.
- Ministry of Health, Labour and Welfare(MHLW), (2016), The Japan food chemical research foundation, http://www.m5.ws001.squarestart.ne.jp/foundation/agrdtl.php?a_inq=46800.
- National Institute of Food and Drug Safety Evaluation (NIFDS), (2016), Guidelines on standard procedures for preparing analysis method.
-
Okada, I., S. Okui, T. Fukuchi, and K. Yoshiya, (1999), Synthesis and insecticidal activity of N-(Tolyloxybenzyl)-pyrazolecarboxamide derivatives, J. Pestic. Sci., 24(4), p393-396.
[https://doi.org/10.1584/jpestics.24.393]

-
Park, M. S., J. J. Lee, and S. W. Myung, (2011), Analysis of phoxim residue in animal food production (cattle and pig) by LC/ESI-MS/MS, J. Korean Chem. Soc., 55(4), p626-632.
[https://doi.org/10.5012/jkcs.2011.55.4.626]

- Song, H., Y. Liu, L. Xiong, Y. Li, N. Yang, and Q. Wang, (2012), Design, synthesis, and insecticidal activity of novel pyrazole derivatives containing α-chloromethyl-N-benzyl carboxamide, and 4,5-dihydrooxazole moieties, J. Agric. Food Chem., 60(6), p1470-1479.
- Son, S. C., M. S. Bae, and S. S. Park, (2015), Chemical characteristics and formation pathways of humic like substances (JULIS) in PM2.5 in an urban area, J. Korean Soc. Atmos. Environ., 31(3), p239-254.
-
Yamaguchi, K., W. Hikiji, M. Takino, K. Saka, M. Hayashida, T. Fukunaga, and Y. Ohno, (2012), Analysis of tolfenpyrad and its metabolites in plasma in a tolfenpyrad poisoning case, Journal of Analytical Toxicology, 36(7), p529-537.
[https://doi.org/10.1093/jat/bks060]

-
Zou, N., Y. Han, Y. Li, Y. Qin, K. Gu, J. Zhang, C. Pan, and X. LI, (2016), Multiresidue method for determination of 183 pesticide residues in leeks by rapid multiplug filtration cleanup and gas chromatoraphy-tandem mass spectrometry, J. Agric. Food Chem., 64(31), p6061-6070.
[https://doi.org/10.1021/acs.jafc.5b05132]

-
Wang, J., W. Chow, D. Leung, and J. Chang, (2012), Application of ultrahigh-performance liquid chromatography and electrospray ionization quadrupole orbitrap high-resolution mass spectrometry for determination of 166 pesticides in fruits and vegetables, J. Agric. Food Chem., 60(49), p12088-12104.
[https://doi.org/10.1021/jf303939s]