1-Aryl ethanolamine유도체로부터 식물 유근생장 억제제 발굴
초록
Pectin methylesterase (PME)는 최근 새롭게 밝혀진 식물생장 조절인자로 이를 작용점으로 하는 저해 물질 탐색을 통한 식물 생장억제제 개발 연구가 활발히 진행되고 있다. 본 연구에서는 aryl ethanamine을 기본 골격으로 하는 다양한 유도체를 1-aryl-1-ethanolamine (Group I)과 2-aryl-ethanamine (Group II)으로 구분하여 PME 효소 활성 억제 효능을 시험하였고, 이로부터 epinephrine (Ki= 51.0 μM)과 fenoterol (Ki= 55.1 μM)의 PME 효소 저해활성을 확인하였다. 특히 1-aryl ethanolamine의 구조에서 1-hydroxy의 치환 여부에 따라 PME 저해활성이 크게 달라짐을 확인할 수 있었고, 1-aryl-1-ethaolamine 구조의 중요성을 확인하였다. 뿐만 아니라, Group I의 물질 중 aryl 기내 meta-hydroxyl 기를 갖는 물질인 epinephrine, fenoterol, phenylephrine이 높은 PME 저해활성을 나타내어, meta-hydroxy기의 중요성을 실험적으로 입증하였다. 또한, PME 저해효과가 확인된 epinephrine과 fenoterol 모두 배추 유근생장 억제능 (IC50 216 - 354 μM)이 확인되어, meta-hydroxylated 1-aryl-1-ethaolamine 유도체로부터 유용한 식물생장억제제 개발이 가능할 것으로 기대하였다.
Abstract
Pectin methylesterase (PME) regulation has been highlighted a new mode-of-action for plant growth, and the inhibitor screening was an issue to develop a new class plant growth regulators (PGR). Recently phenylephrine had been reported their PME inhibition and PGR activity. In here, aryl ethanamines can be divided into 1-aryl-1-ethanolamine (Group I) and 2-aryl ethanamine (Group II), and the chemicals were tested PME inhibition assay. Among them, epinephrine and fenoterol showed potent PME inhibition activity and the Kis were 51.0 and 55.1 μM, respectively. In comparison with Group I and II, the chemicals from Group I based on 1-aryl-1-ethanolamine showed more potent PME inhibition activity than Group II. In addition, meta-hydroxylated 1-aryl-1-ethanolamines like epinephrine, fenoterol, and phenylephrine showed strong PME inhibition with the root growth inhibition in Brassica campestris (IC50 216 - 354 μM).
Keywords:
Pectin methylesterase, plant growth inhibition, aryl ethanolamine, epinephrine, fenoterol키워드:
펙틴메틸에스터라아제, 식물생장조절, 아릴에탄올아민, 에피네프린, 페노테롤서 론
현대 농업의 주요 관심사는 적절한 병해충 방제를 통한 안정적 작물 생산과 함께 작물의 수확 시기를 적절히 조절하여, 고품질 농산물을 생산하며 노동력 수요를 최소화 할 수 있는 재배기술 개발과 이에 맞춘 농약 공급에 있다(Pyo et al., 2014; Jang et al., 2015; Jang et al., 2016; Shin et al., 2017). 특히 최근에는 이를 목적으로 작물의 생장을 조절하기 위한 다양한 생장조절제가 개발되어 활용되고 있다. 최근까지 알려진 식물 생장 조절 물질로는 식물 호르몬에서 유래한 auxin, cytokinin, gibberellin, abscisic acid와 식물 생장호르몬의 생합성 혹은 작용점을 교란하는 물질로 알려진 ancymidol, flurprimidol과 triazole계 성분인 paclobutrazole, uniconazole이 알려져 있다(Kim and Lee 2013; Zhao Y 2010; Kataoka et al., 2008; Rademacher, 2000). 하지만, 호르몬계 물질과 호르몬 교란을 통한 생장억제제의 작물재배 적용에는 많은 제약이 따르고 있어, 비호르몬 조절작용을 갖는 새로운 작물 생장조절제를 찾기 위한 연구가 꾸준히 진행되고 있다. 특히, 최근에는 화학 물질 은행 및 식물 추출물을 활용한 식물생장조절제 탐색 연구가 활발히 진행되고 있으며, 이들 중 essential oil에서 유래한 geraniol을 활용한 생장촉진연구(Choi et al., 2015)와 hydroxyl benzaldehyde계 물질의 유근생장억제 연구(Choi et al., 2016)등이 보고된 바 있다. 또한, 새로운 생장억제 조절점이 될 수 있는 호르몬 비의존형 조절물질 개발연구를 통해 pectin methylesterase(PME) 활성 조절을 통한 식물의 생장조절 연구결과가 최근 보고된 바 있다(Cheong et al., 2019).
Pectin은 식물 세포벽을 구성하는 주요 구성 성분 중 하나로 D-galacturonic acid methyl ester가 α-1,4-glycosidic 결합으로 연결된 다당류이며, pectin의 methylation 정도에 따라 세포벽의 다양한 생리학적 기능이 연구되고 있다. 특히, pectin의 구조 변화는 세포벽 내의 pectin-cellulose 상호작용 및 microfibril과의 상호작용, Ca2+ 등 2가 양이온과의 결합에 의한 세포벽 물리성 조절 등의 생리학적 조절 작용을 갖는 것으로 보고되었다(Carpita and Gibeaut 1993; Kohli et al., 2015; Lionetti et al., 2012). 이러한 pectin에 대한 대사 조절은 pectinase에 의한 pectin 구조 내 glycosidic 결합 가수분해 작용과 PME에 의한 methylation 조절 작용이 알려져 있으며, PME 기능 조절은 식물의 병 저항성 증가와 식물 생장조절 작용이 있는 것으로 최근 보고되고 있다(Dai et al., 2018; Fan et al., 2017; Muller et al., 2013; Volpi et al., 2011; Weraduwage et al., 2016). 특히, PME 조절을 통한 식물 생장조절 연구는 식물체 내 PME inhibitor 단백질의 과발현을 통한 접근과 외래 저분자 물질 처리에 의한 PME 저해제 개발 탐색 연구가 진행되어 왔으며, 이들 중 catechin과 phenylephrine을 활용한 PME저해와 식물 생장 조절 연구가 진행된 바 있다(Cheong et al., 2019; L'Enfant et al., 2019; Muller et al., 2013; Weraduwage et al., 2016).
PME 관련 연구는 식물 생장 조절 인자로서 작용점이 되는 단백질의 기능 규명을 중심으로 그 동안 연구가 진행되어 왔고, PME 저해물질 탐색을 통한 본격적인 생장 조절제 개발 연구는 아직 시작 단계에 머물러 있다. 따라서, 본 연구에서는 PME의 저해 물질로 알려진 phenylephrine의 기본 골격인 aryl ethanamine을 활용하여 다양한 유도체로부터 PME 저해 활성을 평가하고, PME 저해활성을 갖는 aryl ethanamine의 핵심 기본 골격을 확인하고, 이를 통한 식물 생장 억제제 개발 가능성을 검토하였다.
재료 및 방법
시약 및 물질
저해 시험에 사용된 물질인 aryl ethanolamine 유도체는 모두 TCI Co. Ltd (Tokyo, Japan)에서 reagents 등급을 구매하였으며, stereochemistry를 갖는 물질은 stereoisomer mixture인 시약을 구매하여 시험에 사용하였다. Acetic acid, acetylacetone, ammonium acetate, dimetylsulfoxide (DMSO), pectin (from citrus peel), sodium chloride, sodium phosphate는 Sigma-Aldrich Co. Ltd. 사 (MO, USA)에서 구매하여 사용하였다.
PME 저해활성 시험
PME활성 측정은 alcohol oxidase (AO from pichia pastoris, Sigma-Aldrich Co. Ltd., MO, USA)를 사용하는 coupled reaction으로 PME 반응으로 생성된 methanol을 formaldehyde로 산화시킨 뒤, acetylacetone으로 발색시켜 흡광도를 측정하는 stopped assay법으로 Cheong 등(2019)의 방법에 따라 3반복 수행되었다. 시험에 사용된 PME (from organge peel, Sigma-Aldrich Co. Ltd. MO, USA)는 1.7 M NaCl로 희석 후 시험에 사용하였다. 기질인 pectin은 0.15 M phosphate buffer (pH 7.5) 에 녹여 제조하였다. PME 저해활성은 96-well plate에 DMSO로 녹여진 시험용 물질 5 μL, phosphate buffer 25 μL와 0.2% pectin 50 μL를 넣어 섞어준 뒤 1.0 munit AO와 0.1 munit PME를 ice bath에서 첨가한 후 30oC에서 40분간 반응 시켰다. 반응물은 acetylacetone 발색시약 80 μL를 넣어 효소 반응을 종결시키고, 60oC에서 30분간 발색 후 412 nm 파장에서 흡광도를 측정하였다(Sunrise, Tecan Austria-GMBH Ltd., Switzerland). 저해활성 탐색 시 초기 화합물의 농도는 250 μM이었다.
배추 유근생장 억제시험
배추 종자는 ㈜아시아종묘에서 구매하여 사용하였으며, 발아율과 유근생장 억제능은 Kim 등(2014)이 수행한 방법과 같이 처리구 당 50립의 종자를 사용하여 시험하였다. 배추 발아율은 23oC에서 2일간 항온 보관 후 발아율을 측정하였으며, 균일하게 발아된 종자를 취하여 동일 온도조건에서 3일간 보관 후 유근 생장 억제 여부를 평가하였다.
결과 및 고찰
Aryl ethanamine의 PME 저해활성
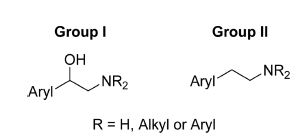
Cheong 등(2019)은 phenylephrine을 대상으로 한 PME 저해제 탐색연구에서 in silico 연구를 통해 aryl기와 ethanamine을 저해물질의 핵심구조로 제안하였으며, 특히 amino기는 enzyme active site의 carboxylate domain (D138)과 charge-to-charge interaction을 갖는 것으로 보고하였다. 따라서, 본 연구에서는 phenylephrine과 유사구조를 갖는 aryl ethanamine 중 1-aryl ethanolamine (Group I)과 2-aryl ethanamine (Group II) 유도체들을 확보하여 각각의 그룹으로 분류하고 이들에 대한 PME 저해활성을 평가하였다(Fig. 1).
Group I은 positive control로 사용된 phenylephrine과 함께 1-aryl ethanolamine 구조를 갖는 epinephrine, fenoterol이 포함되어 있으며, 이들 화합물의 PME에 대한 IC50은 156 - 164 μM이었다. 이러한 결과는 phenylephrine과 유사한 저해 활성으로 확인되었다. 특히, Group I에서 amino기에 치환된 N-alkyl group이 isopropyl 혹은 tert-butyl 등과 같이 methyl 보다 hydrophobicity가 증가하는 치환기가 치환된 경우 PME 저해 활성이 낮아지는 것을 확인할 수 있었다. 또한 aryl기에 위치한 hydroxy 위치가 meta-인 phenylephrine이 para-에 위치한 synephrine보다 PME 저해활성이 증가한 것과 높은 저해활성을 나타낸 epinephrine과 fenoterol 모두 meta-hydroxy기를 갖는 것으로 볼 때 aryl 기에 치환된 meta-hydroxy의 구조적 중요성을 확인할 수 있었다. 이는 Cheong 등(2019)이 예측한 것과 같이 meta-hydroxy가 enzyme과 hydrogen-bond를 형성함으로서 Enzyme-Inhibitor(EI) complex를 보다 강하게 형성한 결과로 판단된다. 반면, Group II에 속한 2-aryl ethanamine 계열 물질은 PME에 대한 IC50이 모두 >250 μM로 PME 효소 활성을 효율적으로 저해하지 못하는 것으로 확인되었다. Cheong 등(2019)은 in silico 시뮬레이션에서 1-aryl ethanolamine 중 hydroxy기의 중요성을 정확하게 분석하지 못하였지만, 본 연구에서는 실험적 증명을 통해 그 중요성을 확인할 수 있었다.
1-Aryl ethanolamine의 PME inhibition kinetics
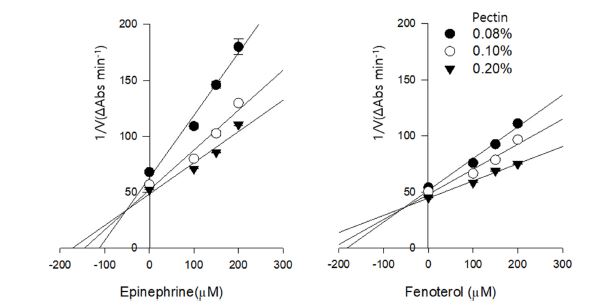
Epinephrine과 fenoterol의 PME에 대한 저해 활성은 기질인 pectin농도와 저해제 농도에 의존하는 competitive inhibition model로 예측되었으며, 이는 phenylephrine의 저해 작용 모형과 같은 것으로 확인되었다(Fig. 2). 이들 물질의 Ki 는 각각 epinephrine 51.0 μM과 fenoterol 55.1 μM로 phenylephrine의 Ki 보다 3배 가량 높은 것으로 나타났다. 특히, 본 시험 결과 epinephrine의 phenyl기에 치환된 para-hydroxy기는 PME 효소와의 강한 결합에 있어 큰 역할이 없는 functional group으로 판단되었다.
Epinephrine과 fenoterol의 배추 유근 생장 억제능
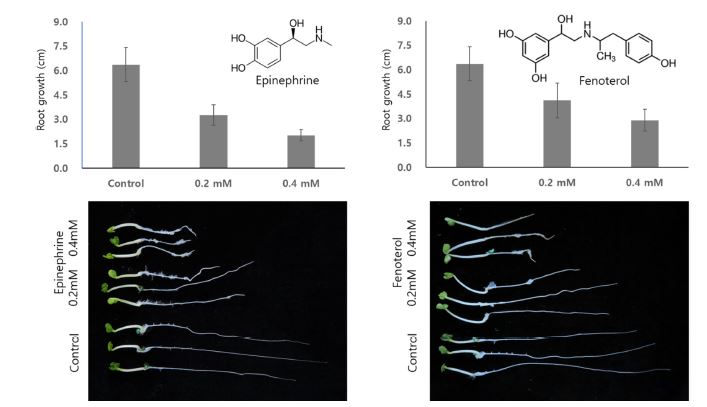
PME에 대한 우수한 저해활성을 보여준 epinephrine과 fenoterol의 배추 생장에 대한 영향평가는 발아율 시험과 유근생장 시험으로 나누어 진행되었다. 먼저, 발아율은 0.8 M 수용액에서 진행한 결과 두 화합물 모두 배추 종자의 발아에는 영향을 주지 않음을 확인할 수 있었고, 이는 phenylephrine의 결과와 동일하였다(Cheong et al. 2019). Phenylephrine 유도체인 epinephrine과 fenoterol의 배추 유근에 대한 IC50은 216 μM과 354 μM로 이번 시험결과 밝혀졌으며, 이는 phenylephrine과 유사한 저해 활성(IC50 385 μM)으로 확인되었다(Fig. 3). 특히, 이들 두 화합물이 Cheong 등(2019)이 보고한 phenylephrine과 유사한 저해활성과 유사한 구조를 갖는 것으로 볼 때 배추의 유근 생장 조절이 root hair 발달 조절에 의한 결과로 판단된다.
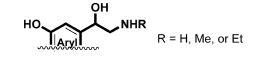
Epinephrine과 fenoterol은 동물 신경계에 작용하는 호르몬계 물질(Boudreau et al., 1993)로 이들 물질을 활용한 작물 생장조절제 개발에는 많은 한계를 갖는 것으로 보여진다. 하지만, 다양한 meta-hydroxylated 1-aryl-1-ethaolamine 유도체로부터 PME를 신규 작용점으로 하는 high-throughput screening (HTS) 연구가 추후 보완 된다면(Fig. 4), 작물 재배에 사용 가능한 신규 식물 생장 억제제 개발이 가능할 것으로 예상된다.
Acknowledgments
본 연구는 연구재단에서 집행하는 교육부 이공학개인기초 연구지원사업 지역대학우수과학자(No. No. 2016R1D1A3B03930535) 지원에 의해 수행되었습니다.
References
-
Boudreau, G., F. Peronnet, J. De Champlain, and R. Nadeau, (1993), Presynaptic effects of epinephrine on norepinephrine release from cardiac sympathetic nerves in dogs, Am. J. Physiol. Heart Circ. Physiol, 265(1), pH205-H211.
[https://doi.org/10.1152/ajpheart.1993.265.1.h205]

-
Carpita, N. C., and D. M. Gibeaut, (1993), Structural Models of Primary Cell Walls in Flowering Plant: Consistency of Molecular Structure with the Physical Properties of the Wall during Growth, Plant J, 3(1), p1-30.
[https://doi.org/10.1111/j.1365-313x.1993.tb00007.x]

-
Cheong, M.S., D. Y. Lee, K. H. Seo, G. H. Choi, Y. H. Song, K. H. Park, and J. H. Kim, (2019), Phenylephrine, a small molecule, inhibits pectin methylesterases, Biochem. Biophys. Res. Commun, 508(1), p320-325.
[https://doi.org/10.1016/j.bbrc.2018.11.117]

- Choi, G. H., D.K. Jeong, B. J. Park, N. J. Cho, J. H. Hong, and J. H. Kim, (2015), Promotive Effects of Geraniol on Radicle Growth of Several Veges and Leaf Growth of Brassica campestris, Korean. J. Pestic. Sci, 19(4), p399-401.
-
Choi, G. H., J. H. Rho, B. J. Park, D. Y. Lee, M. S. Cheong, D. Y. Lee, W. D. Seo, and J. H. Kim, (2016), Benzaldehyde as a new class plant growth regulator on Brassica campestris, J. Appl. Biol. Chem, 59(2), p159-164.
[https://doi.org/10.3839/jabc.2016.029]

-
Dai, X. Y., L. M. Kong, X. L. Wang, Q. Zhu, K. Chen, and T. Zhou, (2018), Prepation, Characterization and Catalytic Behavior of Pectinase Covalently Immobilized onto Sodium Alginate/graphene Oxide Composite beads, Food Chem, 253, p185-193.
[https://doi.org/10.1016/j.foodchem.2018.01.157]

-
Fan, H., H. Dong, C. Xu, J. Liu, J. Ye, G. Mai, and H. Li, (2017), Pectin methylesterases Contribute the Pathogenic Differences between Races 1 and 4 of Fusarium oxysporum f. sp. cubense, Sci. Rep, 7(1), p13140.
[https://doi.org/10.1038/s41598-017-13625-4]

- Jang, I. B., J. Yu, K. B. Kweon, and S. J. Suh, (2016), Effect of Controlled Light Environment on the Growth and Ginsenoside Content of Panax ginseng C, A. Meyer. Kor. J. Med. Crop Sci, 24(4), p277-283.
-
Jang, J., H. J. Kim, A. Y. Ko, E. H. Lee, Y. J. Ju, M. I. Chang, G. S. Rhee, and S. J. Suh, (2015), Development of a Simultaneous Analytical Method for Determination of Trienxapac-ethyl and Trinexapac in Agricultural Products Using LC-MS/MS, Kor. J. Environ. Agric, 34(4), p318-327.
[https://doi.org/10.5338/kjea.2015.34.4.48]

-
Kataoka, K., T. Sakakibara, K. Nishikawa, K Kusumi, and S. Yazawa, (2008), Seed Formation is Affected by Uniconazole, an Inhibitior of Giberellin Biosynthesis, in a Parthenocarpic Cultivar Severianin of Tomato (Lycopersicon esculentum Mill.), J. Jpn. Soc. Hortic. Sci, 77(3), p283-288.
[https://doi.org/10.2503/jjshs1.77.283]

-
Kim, J. H., G. H. Choi, and B. J. Park, (2014), Effect of cinnamyl derivatives on crop growth inhibition of Brassica campestris, Kor. J. Pestic. Sci, 18(4), p439-442.
[https://doi.org/10.7585/kjps.2014.18.4.439]

-
Kim, Y. H., and I. J. Lee, (2013), Influence of Plant Growth Regulator Application on Seed Germination of Dandelion (Taraxacum officinale), Weed Turfgr. Sci, 2(2), p152-158.
[https://doi.org/10.5660/wts.2013.2.2.152]

- Kohli, P., M. Kalia, and R. Gupta, (2015), Pectin Methylesterase: A Review, . Bioprocess. Biotech, 5(5), p227.
- L'Enfant, M., P. Kutudila, C. Rayon, J. Domon, W.H. Shin, D. Kihara, A. Wadouachi, J. Pelloux, G. Pourceau, and C. Pau-Roblot, (2019), Lactose derivatives as potential inhibitors of pectin methylesterases, Int. J. Biol. Macromol, 132, p1140-1146.
-
Lionetti, V., F. Cervone, and D. Bellincampi, (2012), Methyl Esterificaition of Pectin Plays a Role during Plant-Pathogen Interactions and Affects Plant Resistance to Diseases, J. Plant Physiol, 169(16), p1623-1630.
[https://doi.org/10.1016/j.jplph.2012.05.006]

- Müller, K., G. Levesque-Tremblay, A. Fernades, A. Wormit, S. Bartels, B. Usadel, and A. Kermode, (2013), Overexpression of a Pectin Methylesterase Inhibitor in Arabidopsis thaliana Leads to Altered Growth Morphology of the Stem and Defective Organ Separation, Plant Signal. Behav, 8(12), pe26464.
-
Pyo, J. S., S. A. Shrestha, S. H. Park, and J. S. Kang, (2014), Biological Control of Plant Growth Using the Plant Growth-Promoting Rhizobacterium Bacillus mojavensis KJS-3, J. Life Sci, 24(12), p1308-1315.
[https://doi.org/10.5352/jls.2014.24.12.1308]

- Rademacher, W., (2000), Growth Retardants: Effects on Gibberellin Biosynthesis and Other Metabolic Pathways. Annu. Rev. Plant Physiol, Plant Mol. Biol, 51(1), p501-531.
-
Shin, Y. S., J. E. Lee, S. W. Oh, J. D. Cheung, H. R. Sohn, H. W. Do, and M. K. Kim, (2017), Beneficial effect of heat fans on quality and yield of Korean melon cultivated in greenhouse at winter season, Protec. Horticul. Plant Fact, 26(3), p188-193.
[https://doi.org/10.12791/ksbec.2017.26.3.188]

-
Volpi, C., M. Janni, V. Lionetti, D. Bellincampi, F. Favaron, and R. D. Ovidio, (2011), The Ectopic Expression of a Pectin Methylesterase Inhibitor Increases Pectin Methyl Esterification and Limits Fungal Diseases in Wheat, Mol. Plant Microbe Interact, 24(9), p1012-1019.
[https://doi.org/10.1094/mpmi-01-11-0021]

- Weraduwage, S. M., S. J. Kim, L. Renna, F. C. Anozie, T. D. Sharkey, and F. Brandizzi, (2016), Pectin Methylesterification Impacts the Relationship between Photosynthesis and Plant Growth, Plant Physiol, 171, p833-848.
-
Zhao, Y., (2010), Auxin Biosynthesis and its Role in Plant Development, Annu. Rev. Plant Biol, 61(1), p49-64.
[https://doi.org/10.1146/annurev-arplant-042809-112308]