
사과 및 들깻잎 중 이산화염소수를 활용한 농약 저감화 연구
초록
본 연구에서는 친환경적 식품첨가제인 이산화염소수를 이용하여 농산물 잔류농약 저감효과 구명 연구를 수행하였다. 시험방법은 상이한 농도 및 시간 조건을 설정하여 실험을 진행하였다. 이산화염소수 농도 0, 10, 25, 50, 100 mg/L(사과), 0, 5, 10, 25, 50 mg/L(깻잎)와 처리시간 0, 1, 5, 10, 20분 처리하여 저감효과를 확인하였다. 실험결과 시간 및 농도에 따라 저감효과가 증가하는 양상을 보였다. 사과에서의 이산화염소 처리에 따른 잔류양상은 acetamiprid와 dinotefuran에서 최대 저감률이 이산화염소 농도 100 mg/L, 처리시간 20분에서 80.5%, 90.6%로 다른 농약에 비하여 높았다. 두 농약의 낮은 log P와 높은 solubility in water 화학적 특성 때문에 다른 농약에 비하여 저감효율이 높은 것으로 판단된다. 또한, 깻잎에서는 azoxystrobin과 carbendazim에서 최대 저감률이 91%, 90.4%로 높게 나타났는데, 두 농약은 산화반응 쉽게 일어날 수 있는 결합이 존재하여 다른 농약에 비하여 높은 저감률을 얻을 수 있을 것으로 판단된다. 이번 연구의 결과를 통해 이산화염소가 신선농산물의 잔류농약 저감효과 기술로 활용할 수 있을 것으로 판단되어 진다.
Abstract
Chlorine dioxide (ClO2) known as an eco-friendly food additive was used to reduce pesticide residues from the apple and perilla leaf. The experimental conditions were established with treatment concentrations of aqueous ClO2 at 0, 10, 25, 50, 100 mg/L (apple), 0, 5, 10 25, 50 mg/L (perilla leaf) and treatment time for 0, 1, 5, 10, 20 min. As a result, effects of reduction for pesticides residues were improved as increase of treatment time and concentration on ClO2. Especially, the rate of reduction on apple for acetamiprid and dinotefuran at apple were 80.5%, 90.6% and higher rate of degradation than other pesticides, because, two pesticides have the chemical properties of low log P and high solubility in water. On the perilla leaf, the reduction of azoxystrobin and carbendazim, which have the bonds that were easy to oxidize were greatest at 91.0% and 90.4% respectively. These results showed that ClO2 treatments is available method to reduce the pesticide residues on fresh fruits and vegetables.
Keywords:
apple, chlorine dioxide(ClO2), perilla leaf, residual pesticide키워드:
사과, 들깻잎, 이산화염소수, 잔류농약서 론
2019년부터 농약허용물질목록관리제도(Positive List System, PLS)가 시행되면서 농산물 중 농약에 대한 안전성은 강화되었다. PLS제도는 잔류허용기준이(Maximum Residue Level, MRL) 설정되지 않은 농약에 대하여 0.01 mg/kg의 일률적인 기준을 적용하는 제도이다(RDA., 2019). PLS 시행 전에는 MRL이 설정되지 않은 농약에 대해서는 Codex 및 유사 농산물의 MRL을 적용하였다. 그러나, PLS가 시행되면서 MRL 설정이 되지 않은 농약은 일률적인 기준 0.01 mg/kg을 적용하면서 농약안전기준이 강화되어 부적합 농산물이 상승될 것으로 예상된다. 이에 따라 소비자의 농산물 안전에 대한 불안감은 더 높아질 것으로 예상되어 진다. 한 예시로는, 2017년 살충제 달걀 파동으로 인하여 동물복지 달걀에 대한 소비가 증가하였다는(RDA., 2018) 보고를 통해서 일부 식품의 안전성 문제는 해당식품 전체에 대한 소비자 인식에 영향력을 미치며, 소비자들은 더 안전하고, 고품질 식품을 선호하는 경향이 나타나는 것을 확인할 수 있었다.
PLS가 시행되면 부적합 농산물 상승이 예상됨에 따라 안전한 농산물을 구매하고자 하는 소비자는 더욱더 증가할 것으로 판단된다. 이에 따라, GAP(Good Agricultural Practice) 농산물 같은 안전 농산물의 수요가 증가할 것으로 예상되면서, 농산물 생산의 전 과정에서 농약안전관리가 필요할 것으로 판단된다. 그러나, 현재 우리나라는 생산단계에서 농약안전관리가 잘 이루어지고 있지만 수확 후 단계에서는 안전관리방안은 부족한 실정이다. 이번 연구에서는 수확 후 단계에서 농약안전관리방안 마련을 위해서 이산화염소를 이용한 농산물 중 잔류농약 저감화 연구를 진행하였다.그 동안 수확 후 과정에서의 잔류농약 저감연구는 단순세척(Miyahara and Saito., 1994), 오존(Ikeura et al., 2013) 등 제한적으로 진행되어 왔다. 이번 연구에서는 이산화염소(Chlorince dioxide, ClO2)를 이용하여 신선농산물 중 잔류농약 저감화 연구를 실시하였다.
이산화염소(Chlorine dioxide, ClO2)는 강력한 산화제로서 농약과 반응하여 산화반응을 일으켜 농약 분해를 촉진하는 작용을 하는 것으로 알려져 있고(Agüera and Fernández-Alba., 1998; Jia et al., 2017), 염소계소독제와 달리 유기물질과 반응하여 발암성물질인 트리할로메탄(THM)을 형성하지 않아 환경에 안전한 물질로 알려져 있고, 빛 및 온도 등에 민감하여 대기 중에 쉽게 분해되는 특징이 있어서 환경 중에서 안전한 것으로 보고 되어진다(Lee et al., 2015). 또한 이산화염소는 신선농산물 잔류농약 저감기술로의 장점으로 기존의 다양한 연구를 통해 적정한 농도 및 처리시간을 적용할 때 부패균을 저감시켜서 농산물 품질 및 저장기간 향상에 도움을 주는 것으로 나타났다(Aday et al., 2013; Fu et al., 2007; Jin and Lee, 2007; Jin et al., 2007). 그러나 이산화염소는 식품 중 병원성 미생물 제어 연구가 주로 이루어져 왔다. 이산화염소 가스형태로 사과(Sy et al., 2005), 블루베리(Popa et al., 2007), 당근(Gomez-Lopez et al., 2007), 딸기(Mahmoud et al., 2007), 토마토(Trinetta et al., 2013)에서 Escherichia coli, Listeria monocytogenes 및 Salmonella 등의 저감화 연구가 진행되었고, 액체형태로 엽채류(Kim et al., 2008; Lopez-Galvez et al., 2010; Lee and Baek, 2008) 및 과채류 (Jin et al., 2007; Wu and Kim, 2007; Chun et al., 2013) 등 다양한 작물에서 연구가 진행되었다. 현재 신선농산물 중 이산화염소를 이용한 잔류농약 저감연구는 상추(Chen et al., 2014) 및 포도(Wei et al., 2018) 등 에서 일부 실행되었다.
이번 연구에서는 기존에 수행되지 않은 신선농산물의 이산화염소의 잔류농약 저감기술 도입 가능성을 확인하기 위해 이산화염소수를 이용하여 실험을 실시하였다. 시험작물 선정은 다음의 기준을 적용하여 선정하였다. ① 신선농산물 형태로 섭취하고, ② 우리나라 소비자가 많이 섭취하는 다소비 농산물 ③ ‘14~’17 국립농산물품질관리원 잔류농약 실태조사에서 부적합 농약 검출사례가 많고, 농약이 많이 검출되는 작물을 선정하였다. 위의 조건을 충족하는 작물로 과일에서는 사과, 엽채류에서는 깻잎을 선택하여 실험을 진행하였다.
이번 연구에서는 선정된 시험작물에 이산화염소수를 처리하여 잔류농약 저감효과를 확인하였고, 처리조건 중 농약 저감률이 가장 높은 이산화염소수 처리 조건을 산출하였다.
재료 및 방법
시험농약 선정 및 시약
시험 농약은 국립농산물품질관리원에서 발표한 자료 중 ’14-’17동안 사과와 깻잎에서 검출빈도수가 높고, 비의도적 오염으로 잔류할 수 있는 농약과 12종을 선정하였다(Table 1). 분석에 사용한 표준품은 1,000 mg/L stock solution은 Kemidas(Korea, Suwon)에서 구매하여 사용하였고, 각 농약은 acetonitrile(ACN)로 희석하여 10 mg/L의 혼합 working solution을 제조하였다. 분석에 사용한 용매 acetonitrile, acetic acid (100%) 및 formic acide (>98% purity)는 Merck사 (Darmstadt, Germany)의 HPLC Grade를 사용하였고, ammonium acetate (99% purity)는 Sigma Aldrich (St, Louis, MS, USA)에서 구입하여 사용하였다. 3차 증류수는 Millipore사의 Milli-Q-system (Bedford, USA)을 사용하여 제조하였다. QuEChERS 전처리 시약 및 제품은 Sigma Aldrich (St. Louis, USA)에서 구매하였다.
사과 및 들깻잎 중 농약 처리
시험작물 사과(품종: 부사)와 들깻잎(품명: 추부깻잎)을 군산 농수산물 시장에서 구매 후 사과는 상처가 없고 150-200 g 사이의 시료를 선별하였고, 들깻잎은 잎이 무르거나 찢어짐이 없는 작물을 선별하여 실험에 이용하였다. 물 20 L에 제품으로 판매되는 시험농약을 Table 2의 조건대로 용해하여 작물을 집어넣은 후 농약이 충분히 묻을 수 있게 1분간 흔들어 주고 꺼낸 후 상온조건(20oC)에서 2시간 동안 건조시켰다. 농약이 건조된 작물에 농약이 분해되지 않고 충분히 흡착될 수 있도록 냉장조건(4oC)에서 36시간 보관하였다.
이산화염소수의 제조 및 처리
이산화염소수 제조는 이산화염소 발생시약을 MCS 로직스(Seoul, Korea)에서 구매하여 1차 증류수에 용해시켜 제조하였다. 이산화염소수 농도 측정은 N,N-diethyl-p-phenylenediamine(DPD) 방법(Saengnil et al., 2014)을 이용하였다. 이산화염소와 반응하여 발색하는 DPD 용매를 첨가하여 색깔의 진함을 측정하여 농도를 산출하는 방법이다. 위의 방법을 통하여 800-1000 mg/L 수준의 이산화염소수를 측정하였다.
사과 및 깻잎의 처리방법은 각 농도별로(사과: 0, 10, 25, 50, 100 mg/L, 깻잎 0, 5, 10, 25, 50 mg/L) 제조한 이산화염소수에 작물을 침지한 후 1, 5, 10, 20분에 각 시료를 채취하여 2시간 동안 상온에서 (20oC) 건조시켰다. 사용된 시료의 양은 사과 10 kg, 깻잎 5 kg을 사용하였다. 이산화염소수의 각 농도별 처리물량은 사과 8 L 깻잎 20 L를 사용하였고, 각 농도별로 제조한 이산화염소수에 사과 및 깻잎을 2 kg, 1 kg씩 집어넣은 후 침지시켰다. 침지된 시료를 처리시간별로 사과 500 g, 깻잎 250 g을 건조대 위에 올린 후 채취한 후 2시간 동안 상온조건(20oC)에서 표면에 뭍은 이산화염소수를 건조시켰다. 잔류농약 분석을 위해서 사과는 꼭지와 씨를 제거한 가식부위, 들깻잎은 전체부위를 드라이아이스와 함께 분쇄하여 분석할 때까지 냉동조건(-18oC)에서 보관하였다.
잔류농약 분석방법
시료 10 g과 15 mL의 1% acetic acid를 포함한 ACN을 혼합하여 QuEChERS 추출기(1600 MiniG, SPEX sample Prep, Metuchen, USA)를 이용하여 1300 rpm에서 2분간 추출하였다. 여기에 EN Extraction kit (4 g MgSO4, 1 g NaCl, 1 g NaCitrate, 0.5 g disodiumcitratesesquihydrate)을 첨가하였고 QuEChERS 추출기를 이용해 1300 rpm에서 30초간 흔들어준 후 3,500 rpm, 5분(4oC)동안 원심분리 하였다. 상등액 8 mL를 취하여 15 mL EN-General kit (900 mg MgSO4, 150 mg primary secondary amine (PSA))에 첨가한 후 1분간 흔들어준 후 3500 rpm, 5분 조건에서 원심분리 하였다. 0.2 μm syringe filter에 통과시킨 상등액 500 μL와 ACN 500 μL를 혼합한 후 LC-MS/MS로 기기분석 하였다(Table 3).
표준검량선 작성 및 회수율 시험
제조한 working solution과 시험농약이 첨가되지 않은 무처리 시료를 이용해 0.005, 0.01, 0.05, 0.1, 0.2, 0.5 mg/L 수준으로 matrix matched 표준희석용액을 만들었다. 이 표준희석용액들을 Table 3의 기기분석조건에서 분석하여 나타난 chromatography상의 peak 면적을 기준으로 검량선을 작성하고 그 직선성을 평가하였다. 위의 농도의 peak 면적 값을 이용해 검량선의 직선성을 평가하였다. 기기의 정량한계는 PLS 제도에서 MRL이 미설정된 농약에 대해 설정하는 0.01 mg/kg을 보고한계(Roportin Limit)로 설정 후 0.01 mg/kg이하 농도는 불검출로 설정하였다.
시험농약의 회수율 시험을 위해 표준용액 10 mg/kg을 이용하여 무처리 시료에0.1 및 0.5 mg/kg 수준으로 첨가하였다(n=3). 표준용액 첨가 후 30분간 방치한 후 상기의 방법으로 회수율을 산출하였다.
결과 및 고찰
사과 및 깻잎 시험농약 회수율 결과
사과 및 깻잎의 회수율 결과는 Table 5, 6와 같다. 사과에서는 0.1 mg/kg (70.1-113.9%), 0.5 mg/kg (72.3-96.1%)이었다. 들깻잎에서는 0.1mg/kg (83.4-118.2%), 0.5 mg/kg (91.5-112.0%)이었다. RSD 값은 모두 20% 이내로 적정 수준의 결과를 나타냈다.
이산화염소수를 이용한 사과 중 잔류농약 저감효과 구명
사과 중 시험농약의 초기농도는 0.36-1.36 mg/kg이었다. 시험결과 모든 시험농약에서 이산화염소수를 처리할 때 시간 및 농도 증가에 따라 저감률이 높아졌다. 사과 중 시험농약의 이산화염소수 처리에 따른 저감효과는 다음 Fig. 1과 같다. 세척공정에 의한 농산물 중 잔류농약 저감효과에서는 solubility in water와 log P값이 많은 영향을 주기 때문에(Kong et al., 2012), log P값으로 그룹을 나누어서 결과를 해석하였다.
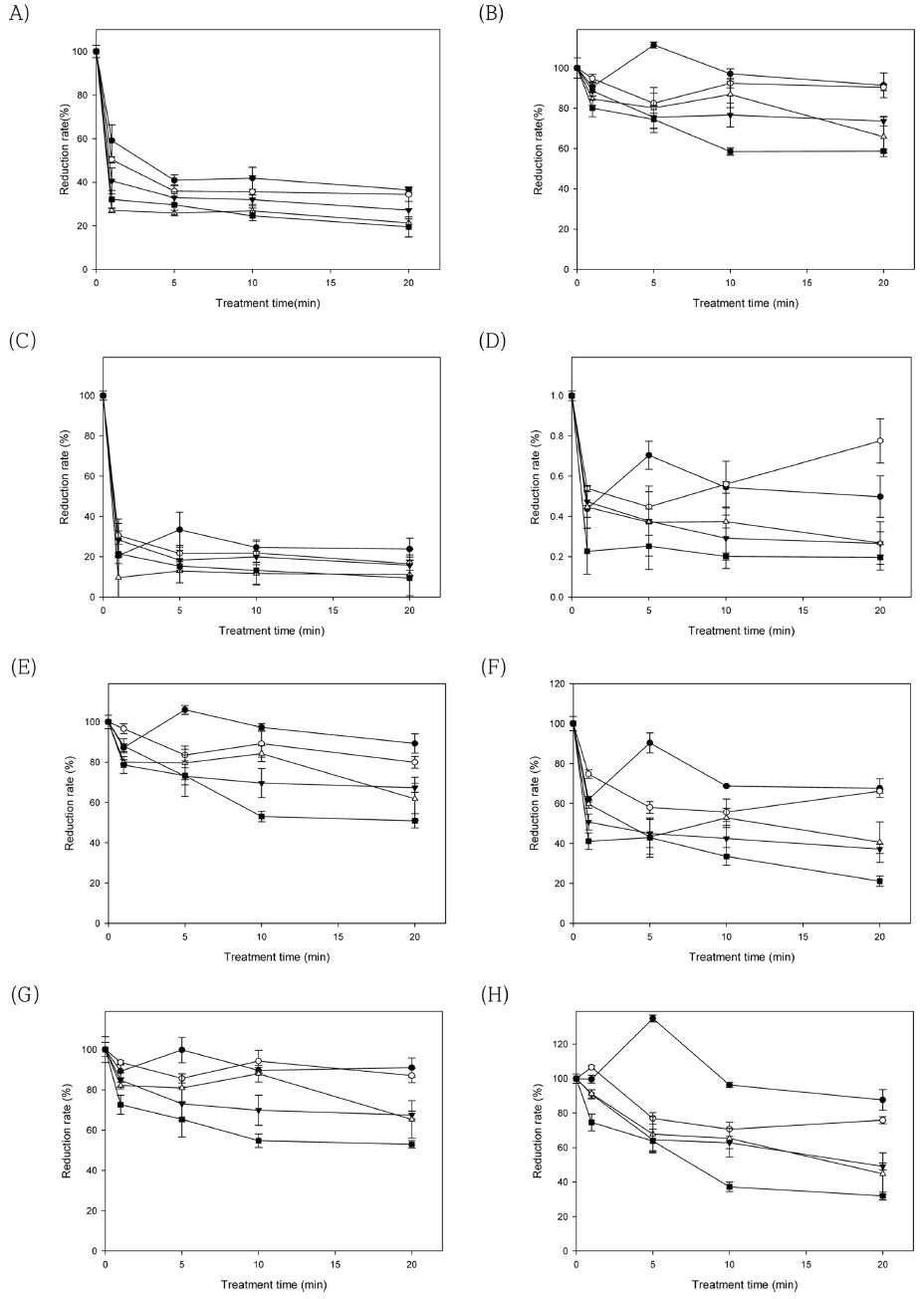
Reduction effects of (A) acetamiprid, (B) difenoconazole, (C) dinotefuran, (D) etofenprox, (E) fludioxonil, (F) isoprothiolane, (G) pyraclostrobin and (H) tebuconazole by different condition according to time (0, 1, 5, 10, 20 min) and concentration (●: 0 mg/L, ○: 10 mg/L, ▼: 25 mg/L, △: 50 mg/L, ■: 100 mg/L) in apples.
사과의 시험농약 중 그룹1인 acetamiprid 및 dinotefuran의 이산화염소수 처리에 따른 저감률은 acetamiprid에서는 모든 처리시간에서 무처리구와 이산화염소수 처리구 사이에서 유의적인 차이가 있었고(p<0.05), dinotefuran은 처리시간 1분에는 무처리구와 이산화염소수 10 mg/L에서는 유의적인 차이가 없었지만(p>0.05), 5분 이후부터는 무처리구와 모든 이산화염소수 처리구에서 유의적인 차이가 있었다(p<0.05). Acetamiprid와 dinotefuran의 무처리구에서 시간별(1, 5, 10, 20분) 저감효과는 40.9-63.5%, 66.6-79.4%이었고, 이산화염소수 100 mg/L 처리에서 시간별 저감효과는 67.9-80.5%, 78.5-90.6%이었다. 그룹 1 농약은 solubility in water가 높고 log P의 값이 낮은 특징을 가져 물과 친화성이 높아 물 처리에서도 저감효과가 상대적으로 높게 나타났다. 세척을 이용한 저감기술은 농약의 log P와 solubility in water와 상관관계가 높게 나타나기 때문이다(Zhao et al., 2014). Lozowicka et al. (2016)의 연구에서도 딸기에 acetamiprid를 수돗물 및 오존수로 처리하고 5분 이상 세척하였을 때 50%이상 농약이 저감되어 본 연구의 60.1%와 비슷한 수준을 나타냈다.
Log P값이 1 초과 4 이하인(그룹 2) 시험농약 중 isoprothiolane 및 tebuconazole의 무처리구와 이산화염소수 처리구 사이에서 유의적인 차이가 있었고(p<0.05), pyraclostrobin은 모든 처리시간에서 이산화염소수 25 mg/L 이상 처리할 때 무처리구와 유의적인 차이가 있었다(p<0.05). 그룹 2 농약 isoprothiolane, pyraclostrobin 및 tebuconazole의 처리시간 20분에서 무처리구와 이산화염소수 100 mg/L의 저감률을 비교하였을 때, 무처리구에서 32.3%, 9.0%, 12.4%이고 이산화염소수 100 mg/L 처리구에서는 78.9%, 47.0%, 68.1%로 두 처리구간 저감률 차이는 46.6%, 38.0%, 55.7%이었다(p<0.05). 그룹 2의 농약은 그룹 1에 비해 무처리구와 이산화염소수 처리간의 저감률 차이가 높게 나타났는데, 이러한 이유는 solubility in water가 48.5, 1.9, 36 mg/L로 용해도가 매우 낮아서 물만 처리하였을 때 사과에 흡착된 농약이 그룹 1 농약에 비해 낮은 비율로 세척되어 이산화염소수와 무처리구간의 저감률 차이가 높게 나타난 것으로 판단된다. Calvo et al. (2019)의 연구내용 중 복숭아, 자두, 살구에서 tebuconazole을 침지한 후 수돗물과 이산화염소수를 처리하여 잔류농약 경감효과를 비교하였을 때, 물을 25분간 처리하였을 때는 40% 저감률이 있었고, 이산화염소수 20 mg/L에서 25분간 처리하였을 때 60% 이상 저감률로 두 처리구간에 20% 이상 저감률 차이가 있다고 보고하였다. 또한 Franka et al. (2010)의 오존을 훈증처리하여 포도 중 잔류농약 저감효과 구명연구에서는 pyraclostrobin을 오존 10,000 μL/L에서 1시간 동안 처리하였을 때, 농약 저감률이 100%로 다른 boscalid등 5종의 다른 시험농약보다 저감률이 높게 나타난 것으로 보고하였다. Franka et al. (2010)는 이러한 이유로 pyraclostrobin 같은 strobilurin계 농약은 ① 에테르결합의 가수분해 및 산화 ② 벤젠고리의 수산화 ③ 이중결합의 산화 및 탈카르복실화 등이 용이하게 나타나는 특징이 있다고 설명하였다. 이산화염소는 오존처럼 산화제 역할을 하는 화합물로서 위의 3가지 반응이 pyraclostrobin과 반응할 때 일어날 것으로 판단되기 때문에 무처리구 대비 이산화염소수 처리구에서 높은 저감률을 나타낸 것으로 판단된다.
시험농약 중 log P값이 4를 초과(그룹 3)하는 difenoconazole 및 fludioxonil은 모든 처리시간에서 이산화염소수 25 mg/L 이상 부터 무처리구 대비 유의적인 차이가 있었고(p<0.05), etofenprox는 처리시간 10분을 제외하고 모든 이산화염소수 처리구와 무처리구 사이에 유의적인 차이가 있었다(p<0.05). 시험농약 3종의 처리시간 20분에서 모든 이산화염소수 농도(0, 10, 25, 50, 100 mg/L) 저감률은 difenoconazole 8.6%, 9.7%, 26.4%, 34.2%, 41.3%, etofenprox 50.2%, 22.5%, 73.4%, 73.2%, 80.3%, fludioxonil 10.7%, 20.0%, 32.7%, 38.2%, 49.1%로 처리농도가 증가하는 경향을 나타냈다. Chen et al. (2014)의 상추 중 이산화염소수 10 mg/L, 20 mg/L을 이용하여 diazinon 및 phorate의 저감효과 구명 연구결과에서도 농도 및 처리시간 증가에 따라 저감률이 높아지는 경향을 보이므로 본 연구와 유사한 양상을 나타냈다. 세척에 의한 저감효과는 log P가 영향을 미치는 것으로 알려져 있는데 이번 연구에서 etopenfrox는 그룹 3 농약이지만 무처리구, 처리시간 20분에서 50% 이상의 저감률로 그룹 1 농약과 비슷한 수준으로 나타났다. 이러한 이유는 etofenprox는 비침투성 농약으로 대부분 표면에 잔류되기 때문에 세척에 의한 저감효율이 높게 나타난 것으로 판단된다. 세척에 의한 농약 저감효과에서는 log P와 solubility in water과 중요한 요소이지만, 농약이 잔류하는 위치도 세척에 의해 저감효과를 결정하는 중요한 요인이므로(Lozowicka et al., 2016), etofenprox는 무처리구에서도 저감률이 높게 나타난 것으로 판단된다. Hwang et al. (2015)이 수행한 양파에 잔류한 etofenprox를 수돗물 침지, 1분간 흐르는 물 세척 및 1% 중성세제를 첨가한 용액을 이용한 침지조건에서 저감효과를 비교한 결과 21.6%, 43.9% 및 28.5%로 나타났다. 본 연구의 무처리구, 처리시간 20분에서의 저감률 50.2%보다 낮은 저감률을 나타냈는데, 이러한 차이는 시험작물 및 농약을 살포하는 방법이 다르기 때문이다. (Hwang et al., 2015)은 농약을 스프레이 방식으로 살포한 후 12일된 양파를 세척실험을 실시하였기 때문에, 상대적으로 농약이 오랫동안 잔류하면서 작물 체내 및 표면에 강하게 흡착되어서 저감률이 낮게 나타난 것으로 사료된디. 그룹 3의 비침투성 농약 중 fludioxonil은 무처리구에서 10% 이내의 저감률로 etofenprox 보다 낮게 나타났다. 두 농약의 제형은 fludioxonil은 액상수화제, etofenprox는 수화제로서 제형에 따른 작물의 흡착력 차이로 인해 저감률이 다르게 나타난 것으로 판단된다. 추후 제형에 따른 농약 흡착력 비교 데이터 생성 및 저감효과 차이구명에 대한 연구가 필요할 것으로 판단된다. Difenoconazole은 그룹 3 농약 중 가장 낮은 저감률을 보였는데, 화학적 특성 중 solubility in water가 낮고 log P값이 높아 물에 잘 세척되지 않으며, 침투이행성 특성 때문에 작물체내 잔류되기 때문이다. 그러나 difenoconazole의 이산화염소수 처리구 및 무처리구 사이 최대 저감률은 38.6% 이었다. (Lauana Pellanda et al., 2018)의 당근 중 오존수를 이용한 difenoconazole의 저감효과 구명연구에서 오존수 0-10 mg/L, 9.5-110.5분간 처리하였을 때 95% 이상의 저감률이 있다고 보고하였다. 오존은 강력한 산화제로서 수용액상에서 오존으로부터 생성된 산소 라디칼 원자에 의해 수산화 이온이 생성되고, 이 수산화 이온이 농약과 산화반응을 한다(Chiron et al., 2000). Difenoconazole에 존재하는 이중결합은 산화반응이 쉽게 일어날 수 있기 때문에, 산화제인 이산화염소에 의해 산화반응하여 저감률이 물만 처리할 때보다 높게 나타난 것으로 판단된다.
사과 중 이산화염소수를 처리할 때 농도 및 처리시간 증가에 따라 농약 저감률이 높아졌다. 본 연구의 결과를 통해 사과 중 이산화염소수 100 mg/L, 20분 처리할 때, 저감효과가 가장 높았고 통계적으로도 다른 처리구와 유의적인 차이가 있었다(p<0.05). 수확 후 과정에서 이산화염소수를 위의 조건으로 처리하면 안전 농산물 생산에 도움을 줄 수 있을 것으로 판단된다.
이산화염소수를 이용한 들깻잎 중 잔류농약 저감효과
들깻잎 중 시험농약 6종의 초기농도는 23.2-71.4 mg/kg이었고, 사과에 비하여 초기농도가 높게 나타났다. 들깻잎은 잎이 수평으로 펼쳐져 있고, 표면에는 융모가 있어서, 과수 및 다른 채소에 비하여 농약 흡착이 용이하여 본 연구에서 침지법을 이용하여 농약을 흡착시킬 때 사과에 비하여 높은 농도로 잔류된 것으로 판단된다. 들깻잎에 이산화염소수를 처리하였을 때 잔류농약 저감효과는 수돗물만 처리한 무처리구 대비 모든 이산화염소수 처리구에서 유의적인 차이가 있었다(p<0.05).
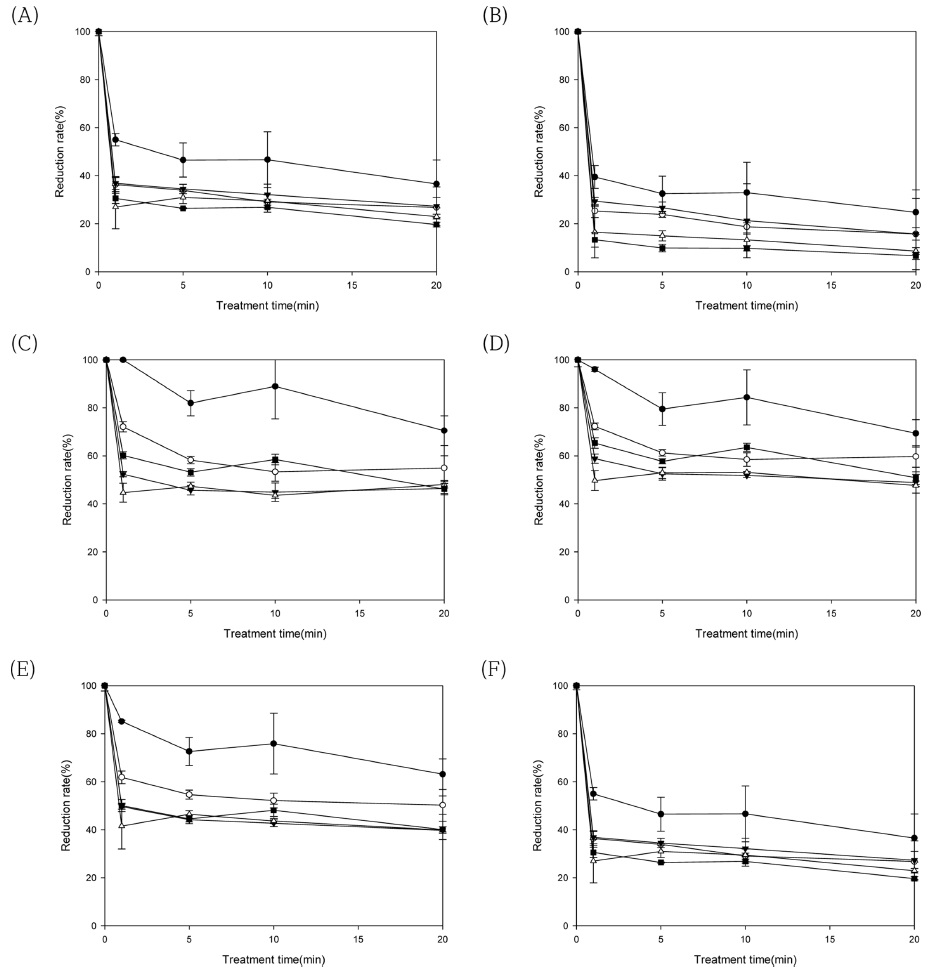
Reduction effects (A) azoxystrobin, (B) carbendazime, (C) clothianidin, (D) imidacloprid, (E) isoprothiolane and (F) pyraclostrobin by different condition according to time (0, 1, 5, 10, 20 min) and concentration (●: 0 mg/L, ○: 5 mg/L, ▼: 10 mg/L, △: 25 mg/L, ■: 50 mg/L) in perillia leaves.
그룹 1 농약인 clothianidin과 imidacloprid의 무처리구 및 이산화염소수 50 mg/L를 처리하였을 때, 처리시간별(1, 5, 10, 20분) 농약 저감률은 clothianidin에서 0.0-29.5%, 39.8-53.8%이고 imidacloprid는 4.0-30.6%, 34.7-49.1%로 두 농약 모두 무처리구와 이산화염소수 처리구 사이에 유의적인 차이가 있었다(p<0.05). Yakup et al. (2017)의 연구에서 clothianidin을 수돗물에서 5-10분간 처리했을 때 저감효과가 없었지만 오존수로 2-5분 동안 처리했을 때 88~98% 이상 저감효과가 있다고 보고하였다. 본 연구에서 clothianidin에서 무처리구와 이산화염소 처리구 사이에 최대 저감률 차이가 29.5%로 유의적인 차이가 있다는(p<0.05) 결과와 유사한 양상을 나타냈다. 그러나 본 연구의 이산화염소수 처리와 Yakup et al. (2017) 오존수 처리의 저감률 차이가 40% 이상 났는데, 이러한 이유로 Yakup et al. (2017)의 실험은 물에 용해된 농약을 대상으로 실험을 하였고, 본 연구에서는 깻잎을 대상으로 실험을 하였기 때문에, 시험대상의 차이가 다음과 같은 차이를 나타낸 것으로 판단된다. 이산화염소도 오존과 같은 산화제로서 충분히 농약과 반응을 시킨다면 clothianidin에서 더 높은 저감률을 나타낼 것으로 사료된다. Bourgin et al. (2011)의 연구에서 imidacloprid 표준품을 훈증실에 넣고 오존가스를 처리하였을 때, 오존가스 100 g/m3에서 45분간 처리할 때 imidacloprid가 99.8% 저감률이 나타났다고 보고하였고, imidacloprid의 분해경로는 2개의 아민그룹을 가지는 imidazolidine 고리의 α-carbon이 수산기에 의해 산화되면서 저감된다고 보고하였다. 본 연구에서는 최고 저감률이 52.3%로 Bourgin et al. (2011)의 연구결과와 비교하여 47% 정도 낮게 나타났지만, 작물에 잔류하는 농약은 모두 이산화염소에 노출되는 것이 아닌 작물 체내 및 깻잎의 융모 사이 흡착하여 산화반응이 원활하게 일어나지 못하기 때문에 표준품을 처리한 Bourgin et al. (2011)의 연구에 비해 낮은 저감률이 나타난 것으로 판단된다.
그룹 2 농약 azoxystrobin, carbendazim 및 isoprothiolane에서 모든 이산화염소수 처리구에서 무처리구와 비교하였을 때 유의적인 차이가 있었다(p<0.05). 처리시간 20분, 모든 이산화염소수 처리농도 (0, 5, 10, 25, 50 mg/L)에서 저감률은 azoxystrobin 78.4%, 86.2%, 82.0%, 87.4%, 91.0%, carbendazim 75.2%, 84.3%, 84.3%, 91.4%, 93.4%이고, isoprothiolane 36.8%, 49.7%, 60.2%, 60.1%, 59.9%로 처리 농도 증가에 따라 저감효과가 증가하는 양상을 보였다. 그러나 그룹 2의 농약 중 azoxystrobin과 carbendazim은 최대 저감효율이 90% 이상으로 그룹 1 농약보다 높게 나타나서 log P와 solubility in water와 관계없이 저감률이 높게 나타났다. 이러한 이유로는 첫째, 공통적으로 초기농도가 azoxystroin 71.4 mg/kg, carbendazim 61.9 mg/kg로 다른 농약에 비하여 높기 때문이다. 둘째로는, 두 농약의 작물 잔류 위치 때문으로, azoxystrobin은 침투이행성 농약이지만 대부분 작물의 표면에 축적되어서(Nadide et al. 2015) 세척에 의해 저감이 잘되는 것으로 판단된다. 또한 Jung et al. (2008)의 연구에 의하면 carbendaizm의 구조에는 C=O 이중결합을 가지고 있어 오존수에서 발생한 수산화기 및 산소 라디칼 원자에 의한 반응으로 분해가 잘 일어난다고 보고하였다. 본 연구에서 이산화염소 처리시 carbendazim에서 높은 저감률을 나타낸 것은 Jung et al. (2008)에 연구내용에서 언급된 C=O 이중결합과 이산화염소의 산소 라디칼 원자와 반응하여 90% 이상의 높은 저감률 결과를 얻은 것으로 판단된다. Isoprothiolane은 그룹 2에서 가장 낮은 저감률을 나타냈는데, isoprothiolane의 경우 세 개의 농약 중 log P 값이 가장 높고, 들깻잎에 침투이행력 및 흡착 능력이 다른 농약보다 높을 것으로 추정되기 때문에 같은 그룹의 다른 농약보다 저감률이 낮게 나타난 것으로 판단된다.
그룹 3의 pyraclostrobin도 모든 이산화염소수 처리구에서 무처리구와 비교할 때 유의적인 차이가 있었다(p<0.05). Pyraclostrobin은 처리시간별 저감률은 무처리구에서 45.0-63.4%이고, 이산화염소수 50 mg/L에서 69.4-80.3%로 두 처리구간에 16.9-35.3%의 저감률 차이가 있었다(p<0.05). 그러나 pyraclostrobin은 들깻잎에서 사과보다 높은 저감률을 보였는데, 들깻잎과 같이 융모가 있는 엽채류에서 사과와 같이 표면이 매끄러운 과수보다 농약 저감률이 낮을 것으로 예상되었지만, 오히려 깻잎에서 최고 저감률이 80.3%로 사과의 최고 저감률보다 33.3% 높게 나타났다. 이러한 이유로 첫 번째로는, 들깻잎의 초기잔류량은 31.1 mg/kg, 사과는 0.45 mg/kg으로 두 작물간 초기 잔류량이 69배가 차이 나기 때문이고, 두 번째는 들깻잎은 면적이 넓고 얇은 작물이라서 농약이 침투하여 작물체내로 들어가는데 한계가 있고, 사과는 둥글고 들깻잎에 비해 굵은 작물이라 더 많은 농약이 작물체내 침투하여 잔류하기 때문인 것으로 사료된다.
들깻잎에서도 이산화염소수 농도와 처리시간 증가에 따라 잔류효율이 높아지는 것으로 나타나는데, 통계적으로는 최장시간(20분)에서 이산화염소수 25, 50 mg/L을 처리할 때 일부를 제외하고는 두 처리구 사이의 저감률이 통계적으로 유의적인 차이가 없었기 때문에(p>0.05), 처리농도 25 mg/L, 처리시간 20분을 최적조건으로 설정하여 들깻잎의 수확 후 단계과정 중 적용하는 것이 적절할 것으로 사료된다. 위의 언급된 기술을 깻잎 의 수확 후 과정에 적용한다면 PLS를 대비하여 더욱더 안전한 농산물 생산에 도움을 줄 것으로 생각된다.
Acknowledgments
본 연구는 농촌진흥청 공동연구사업(과제번호: PJ012510012019) 및 국립농업과학원 농업과학기술 연구개발사업(과제번호: PJ012510012019)의 지원에 의해 이루어진 것임
References
-
Aday, M. S., M. B. Buyukcan and C. Caner (2013) Maintaining the quality of strawberries by combined effect of aqueous chlorine dioxide with modified atmosphere packaging. J. Food Process. Preserv. 97(6):568-581.
[https://doi.org/10.1111/j.1745-4549.2012.00697.x]

-
Agüera, A. and A. R. Fernández-Alba (1998) GC–MS and LC-MS evaluation of pesticide degradation products generated through advanced oxidation processes: an overview. Analusis. 26(6):123-130.
[https://doi.org/10.1051/analusis:199826060123]

-
Bourgin, M., F. Violleau, L. Debrauwer and J. Albet (2011) Ozonation of imidacloprid in aqueous solutions: Reaction monitoring and identification of degradation products. Journal of Hazardous Materials. 190(1-3):60-68.
[https://doi.org/10.1016/j.jhazmat.2011.02.065]

-
Calvo, H., D. Redondo, S. Remon, M. E. Venturini and E. Arias (2019) Efficacy of electrolyzed water, chlorine dioxide and photocatalysis for disinfection and removal of pesticide residues from stone fruit. Postharvest Biology and Technology. 148:22-31.
[https://doi.org/10.1016/j.postharvbio.2018.10.009]

-
Chen, J. Y., Y. J. Lin and W. C. Kuo (2013) Pesticide Residue Removal from Vegetables by Ozonation. Journal of Food Engineering. 114(3):404-411.
[https://doi.org/10.1016/j.jfoodeng.2012.08.033]

-
Chiron, S., A. Fernandez-Alba, A. Rodriguez and E. Garcia-Calvo (2000) Pesticide chemical oxidation: state-of-the-art. Water Research. 34(2):366-377.
[https://doi.org/10.1016/S0043-1354(99)00173-6]

-
Chun H. H., Kang J. H. and K. B. Song (2013) Effects of aqueous chlorine dioxide treatment and cold storage on microbial growth and quality of blueberries. J. Korean Soc. Appl. Biol. Chem. 56(3):309-315.
[https://doi.org/10.1007/s13765-013-3017-9]

-
Franka Mlikota Gabler, Joseph L. Smilanick, Monir F. Mansour, Hakan Karaca (2010) Influence of fumigation with high concentrations of ozone gas on postharvest gray mold and fungicide residues on table grapes. Postharvest Biology and Technology. 55(2):85-90.
[https://doi.org/10.1016/j.postharvbio.2009.09.004]

-
Fu, Y. C., K. L. Zhang, N. Y. Wang and J. H. Du (2007) Effects of aqueous chlorine dioxide treatment on polyphenol oxidases from golden delicious apple. LWT - Food Sci. Technol. 40(8): 1362-1368.
[https://doi.org/10.1016/j.lwt.2006.11.001]

-
Geetanjali Kaushik, Santosh Satya and S. N. Naik (2009) Food processing a tool to pesticide residue dissipation - A review. Food Research International, 42(1):26-40.
[https://doi.org/10.1016/j.foodres.2008.09.009]

-
Gomez-Lopez, V. M., F. Devlieghere, P. Ragaert, and J. Debevere (2007). Shelf-life extension of minimally processed carrots by gaseous chlorine dioxide. International Journal of Food Microbiology, 116(2):221-227.
[https://doi.org/10.1016/j.ijfoodmicro.2006.12.008]

-
Kim, Y. J., S. H. Lee, J. Y. Park, J. H. Park, M. S. Chung, K. S. Kwon, K. S. Chung, M. S. Won and K. B. Song (2008) Inactivation of Escherichia coli O157: H7, Salmonella typhimurium, and Listeria monocytogenes on stored iceberg lettuce by aqueous chlorine dioxide treatment. J. Food Sci. 73(9):M418–M422.
[https://doi.org/10.1111/j.1750-3841.2008.00940.x]

-
Kong, Z. Q., F. S. Dong, J. Xu, X. G. Liu, J. Li and Y. B. Li (2012) Degradation of acephate and its metabolite methamidophos in rice during processing and storage. Food Control, 23(1):149-153.
[https://doi.org/10.1016/j.foodcont.2011.07.001]

-
Hwang K. W., W. S. Bang, H. W. Jo and J. K. Moon (2015) Dissipation and removal of the etofenprox residue during processing in spring onion. Agricultural Ane Food Chemistry, 63(30):6675-6680.
[https://doi.org/10.1021/acs.jafc.5b02345]

-
Ikeura, H., S. Hamasaki and M. Tamaki (2013) Effects of ozone microbubble treatment on removal of residual pesticides and quality of persimmon leaves. Food Chemistry. 138(1):366-371.
[https://doi.org/10.1016/j.foodchem.2012.09.139]

-
Lauana, P. S., L. R. D. Faronia, F. F. Helenoa, F. G. Pintob, M. E. L. R. Queirozc and H. F. P. Lucas (2018) Ozone treatment for pesticide removal from carrots: Optimization by response surface methodology. J. Food Chemistry. 243:435-441.
[https://doi.org/10.1016/j.foodchem.2017.09.134]

-
Lee S. Y. and S. Y., Baek (2008) Effect of chemical sanitizer combined with modified atmosphere packaging on inhibiting Escherichia coli O157:H7 in commercial spinach. Food Microbiol. 25(4):582-587.
[https://doi.org/10.1016/j.fm.2008.02.003]

-
Lee, Y. S., G. Burgess, M. Rubino and R. Auras (2015) Reaction and diffusion of chlorine dioxide gas under dark and light conditions at different temperatures. Journal of Food Engineering, 144: 20-28.
[https://doi.org/10.1016/j.jfoodeng.2014.07.008]

-
Lopez-Galvez, F., A. Allende, P. Truchado, A. Martinez-Sanchez, J. A. Tudela, M. V. Selma and M. I. Gil (2010) Suitability of aqueous chlorine dioxide versus sodium hypochlorite as an effective sanitizer for preserving quality of fresh-cut lettuce while avoiding by-product formation. Postharvest Biol. Technol. 55(1):53-60.
[https://doi.org/10.1016/j.postharvbio.2009.08.001]

-
Lozowicka B., Jankowska M., Hrynko I., Kaczynski (2016) Removal of 16 pesticide residues fromstrawberries by washing with tap and ozone water, ultrasonic cleaning and boiling. Environ. Monit. Assess. 188(51):1-19.
[https://doi.org/10.1007/s10661-015-4850-6]

-
Mahmoud, B. S. M., A. R. Bhagat and R. H. Linton (2007) Inactivation kinetics of inoculated Escherichia coli O157: H7, Listeria monocytogenes and Salmonella enterica on strawberries by chlorine dioxide gas. Food Microbiology, 24(7-8):736-744.
[https://doi.org/10.1016/j.fm.2007.03.006]

-
Miyahara, M. and Y. Saito (1994) Effects of the processing steps in tofu production on pesticide residues. Journal of Agricultural and Food Chemistry, 42(2):369-373.
[https://doi.org/10.1021/jf00038a026]

-
Nadide T. and K. Hakan (2015) Enhanced Degradation of Azoxystrobin in Grapes and model systems by ozone fumigation during storage. Science&Engineering, 37: 479-488.
[https://doi.org/10.1080/01919512.2015.1064763]

-
Jia, X. H., L. Feng, Y. Z. Liu and L. Q. Zhang (2017) Oxidation of antipyrine by chlorine dioxide: reaction kinetics and degradation pathway. Chem. Eng. J., 309:646-654.
[https://doi.org/10.1016/j.cej.2016.10.062]

- Jin, Y. Y., Y. J. Kim, K. S. Chung, M. Won and K. B. Song (2007) Effect of aqueous chlorine dioxide treatment on the microbial growth and qualities of strawberries during storage. Food Sci. Biotechnol. 16(6):1018-1022.
-
Jin, H. H. and S. Y. Lee (2007) Combined effect of aqueous chlorine dioxide and modified atmosphere packaging on inhibiting Salmonella typhimurium and Listeria monocytogenes in mungbean sprouts. J. Food Sci. 72(9):M441-M445.
[https://doi.org/10.1111/j.1750-3841.2007.00555.x]

-
Popa, I., E. J. Hanson, E. C. D. Todd, A. C. Schilder and E. T. Ryser (2007) Efficacy of chlorine dioxide gas sachets for enhancing the microbiological quality and safety of blueberries. Journal of Food Protection, 70(9):2084-2088.
[https://doi.org/10.4315/0362-028X-70.9.2084]

- Rural Development Administration (2018) Agricultural statistics of Management technology. http://nongsaro.go.kr, . Acceseed 6 Sep. 2018.
- Rural Development Administration (2019) Pesticide. http://nongsaro.go.kr, . Acceseed June 2019.
-
Saengnil, K., A. Chumyam, B. Faiyue and J. Uthaibutra (2014) Use of chlorine dioxide fumigation to alleviate enzymatic browning of harvested ‘Daw’ longan pericarp during storage under ambient conditions. Postharvest Biol. Technol., 91:49-56.
[https://doi.org/10.1016/j.postharvbio.2013.12.016]

-
Sy, K. V., M. B. Murray, M. D. Harrison and L. R. Beuchat (2005) Evaluation of gaseous chlorine dioxide as a sanitizer for killing Salmonella, Escherichia coli O157: H7, Listeria monocytogenes, and yeasts and molds on fresh and fresh-cut produce. Journal of Food Protection, 68(6):1176-1187.
[https://doi.org/10.4315/0362-028X-68.6.1176]

-
Trinetta, V., R. H. Linton and M. T. Morgan (2013) Use of chlorine dioxide gas for the postharvest control of Alternaria alternata and Stemphylium ves-icarium on Roma tomatoes. Journal of the Science of Food and Agriculture, 93(13):3330-3333.
[https://doi.org/10.1002/jsfa.6180]

-
Wu, V. C. H. and B. Kim (2007) Effect of a simple chlorine dioxide method for controlling five foodborne pathogens, yeasts and molds on blueberries. Food Microbiol., 24(7-8):794-800.
[https://doi.org/10.1016/j.fm.2007.03.010]

-
Yakup Sedat VELIOGLU, Şeyda FİKİRDEŞİCİ-ERGEN, Pelin AKSU and Ahmet ALTINDAĞ. (2017) Effects of ozone treatment on the degradation and toxicity of several pesticides in different groups. Journal of Agricultural Sciences, 24:245-255.
[https://doi.org/10.15832/ankutbd.446448]

-
Zhao, L., J. Ge, F. Liu and N. Jiang (2014) Effects of storage and processing on residue levels of chlorpyrifos in soybeans. Food Chemistry, 150: 182-186.
[https://doi.org/10.1016/j.foodchem.2013.10.124]

