Imidacloprid의 꿀벌 유충 급성 및 만성 독성평가
초록
Imidacloprid는 네오니코티노이드계 살충제로 주로 과실의 나방 및 진딧물 방제에 널리 사용되고 있으며 전세계적으로 양봉산물 중 화분, 화밀, 왁스에서 검출되고 있다. 국내 네오니코티노이드계 농약의 유충에 대한 독성연구는 시작단계 있어 본 연구에서는 꿀벌 유충 단회 및 반복노출시험을 통하여 imidacloprid가 꿀벌 유충에 미치는 영향을 살펴보고자 하였다. 유충 단회 및 반복 노출 시험에서 LD50을 구하기 위해 imidacloprid를 9.00, 3.60, 1.44, 0.58, 0.23 μg/larva로 처리하였다. 단회노출 시험은 4일차 유충에 약제를 30 μl 노출한 후 72시간 LD50 값을 구하였다. 단회 노출 후 72시간 LD50 값은 1.465(0.800-2.329) μg/larva이었다. 반복노출 시험은 이충 후 3,4,5,6 일차에 각각 20,30,40,50 μl씩 약제를 4일간 노출 후 시험 8일, 15일, 22일 차에 LD50 값을 구하였다. 반복 노출 후 LD50 값은 D8: 6.311 μg/larva, D15: 3.315 μg/larva, D22: 1.510 μg/larva이었다. 또한 imidacloprid 반복 노출 후 치사개체 및 이상증상을 관찰하였다. 약제 처리농도가 증가할수록 치사 개체 증상 중 유충단계에서 죽거나 갈변화 되어 죽는 비율이 번데기 단계에서 죽는 비율보다 상대적으로 높게 나타났다.
Abstract
Imidacloprid are widely used for pest control in agricultural area and have been detected in nectar, pollen, and wax. To date, only a few studies have been carried out to assess the effect of pesticides on honeybee larvae. Therefore we aimed to assess the acute and chronic toxicity of imidacloprid to honeybee larvae using an in vitro rearing method. The following imidacloprid doses were used to determine the LD50 for the acute and chronic test: 9.00, 3.60, 1.44, 0.58, 0.23 μg/larva. LD50 were calculated for larvae at 72h following a single diet exposure. The LD50 value was 1.465 (0.800 - 2.329) μg/larva. LD50 for in vitro reared honey bee worker brood at day 8, day 15, and day 22 after grafting for the chronic test were 6.311, 3.315, 1.510 μg/larva, respectively. Various anomalies and mortality symptoms were observed in the reared brood after the repeated exposure. The ratio of early or melanizing larval death to pupal death increased with higher imidacloprid concentrations.
Keywords:
honeybee larvae, imidacloprid, toxicity키워드:
꿀벌, 유충, imidacloprid서 론
꿀벌(Apis mellifera)은 화분활동을 하기 위해 벌통으로부터 보통 3-8 km 거리를 비행하며 농약을 포함한 여러 오염물질에 노출된다(Beekman and Ratnieks, 2000). 최근 여러 논문에서도 벌통 내부의 잔류 농약 검출을 보고 하고 있듯이 꿀벌은 종종 양봉 약품뿐만 아니라 환경오염물질, 농약, 다양한 독성물질에 동시다발적으로 노출된다(Chazat and Faucon, 2007; Mullin et al., 2010). 미국에서는 121종의 농약 및 대사물질이 887개 양봉 샘플(왁스, 화분, 벌 등)에서 발견되었다고 보고 되었다(Johnson et al., 2010).
이렇듯 꿀벌이 비행 및 화분활동 후 농약 및 대사물질을 벌통 안으로 가져오면서 꿀벌 유충은 오염된 화분(pollen)과 화밀(nectar)을 섭취함으로써 농약에 노출될 수 있다(Sanchez-Bayo and Goka, 2014; Tosi et al., 2018). 꿀벌 유충은 섭식 과정에서 섭취와 접촉이 동시에 이루어지며 꿀벌 성체에 비해 화학물질에 보다 민감하게 반응한다고 알려져 있어 유충단계의 건강상태가 봉군 전체의 건강과 수명에 영향을 주는 중요한 변수가 될 수 있다(WU et al., 2011; Zhu et al., 2014).
이에 유럽 및 미국에서는 꿀벌 위해성 평가 1단계에서 성체뿐만 아니라 꿀벌 유충독성을 평가하도록 되어 있다. 하지만 우리나라의 꿀벌 위해성평가 체계에서는 Tier 1단계에서 꿀벌 급성독성시험, Tier 2단계에서 꿀벌 엽상잔류시험, Tier 3단계에서 꿀벌 야외시험을 평가하도록 되어 있으며 아직 꿀벌 유충에 대한 안전성평가를 하지 않고 있는 상태이다. 따라서 국내에서도 농약등록단계에서 꿀벌 유충독성 시험법 도입에 대한 필요성 및 타당성을 검토 중에 있으며 이에 대한 시험법 확립을 하여 농약성분에 대한 꿀벌유충의 독성영향 연구결과를 최근에 발표하였다(Im et al., 2016; Paik et al., 2016).
벌통 안에서의 in vivo 농약의 꿀벌 유충 영향 시험은 다양한 환경변이로 인해 시험이 쉽지 않다. 따라서 in vitro 꿀벌 유충독성시험법이 개발되었고(Aupinel et al., 2007; Crailsheim et al., 2012; Schmehl et al., 2016), OECD 시험법도 최근 구축 되었다. 현재 OECD 시험법에서는 유충 단회노출 시험법(OECD No. 237, 2013)과 반복노출 시험법(OECD No. 239, 2016)이 등재되어 있다.
네오니코티노이드계 농약은 전세계적으로 가장 많이 사용되는 농약 중 하나이다(Blacquiere et al., 2012). 네오니코티노이드계 농약은 acetamiprid, clothianidin, dinotefuran, imidacloprid, nitenpyram, thiacloprid, thiamethoxam을 포함한다. Imidacloprid는 네오니코티노이드계 살충제로 곤충의 nicotinic acetylcholine receptor에 대한 선택적 길항체(agonist)로 작용, 신경전달을 저해함으로써 곤충을 치사시키는 작용기작을 나타낸다(Brown et al., 2006). Imidacloprid는 침투이행성 약제로 접촉독 및 섭식 살충효과를 가진다. 주로 과실의 나방 및 진딧물 방제에 널리 사용되고 있다(Elbert et al., 1991; Yang et al., 2012). Imidacloprid는 2017년 기준 국내 연간 수입량이 75,400 kg으로 네오니코티노이드계 농약 중 가장 많이 수입되는 원제이다(Korea Crop Protection Association, 2018). 그리고 imidacloprid는 유럽, 미국, 아시아에서 양봉 산물 중 화분(pollen)에서 평균 19.7 ppb, 화밀(nectar)에서 6.0 ppb, 왁스(wax)에서 26.5 ppb가 검출되었다고 보고된바 있다(Sanchez-Bayo and Goka, 2014). 최근 실험실, 반야외, 야외시험에서 수행된 연구결과에 의하면 imidacloprid는 꿀벌의 학습, 기억력, 비행활동, 귀소행동(homing behavior), 여왕벌의 생식력에 영향을 준다고 보고되어 있다(Bortolotti et al., 2003; Decourtye et al., 2003; Eiri and Nieh, 2012; Ramirez-Romero et al., 2005; Wu-smart and Spivak, 2016).
전 세계적으로 네오니코티노이드계 농약의 꿀벌 성체에 대한 독성 연구는 많이 이루어지고 있지만 유충에 대한 독성 연구는 시작단계라고 할 수 있다. 따라서, 본 연구에서는 꿀벌 유충 단회 및 반복노출 시험을 통하여 imidaclorprid가꿀벌 유충에 미치는 영향을 살펴보고자 하였다.
재료 및 방법
시약
시험에 사용한 약제는 Dr. Ehrenstorfer사의 imidacloprid (99.0%)를 구입하여 사용하였다. 양성대조물질로는 dimethoate (98.9%, Dr. Ehrenstorfer)을 사용하였다.
유충준비
Fig. 1은 OECD 가이드라인의 꿀벌 유충 단회 및 반복노출 시험법의 주요 과정을 그림으로 나타낸 것이다(OECD, 2013; OECD, 2016). 시험에 사용한 꿀벌은 전라북도 국립농업과학원 잠사양봉소재과 양봉장에 위치한 세 벌통에서 무작위 선발하였다. 시험 3일전(D-3)에 격왕판을 설치하여 공소비판에 여왕벌이 산란하게 한 뒤 다음날 산란을 확인하고 3일 후 시험 1일차(D1)에 1일령 유충을 48 well-plate (SPL, Korea)에 이충하였다.
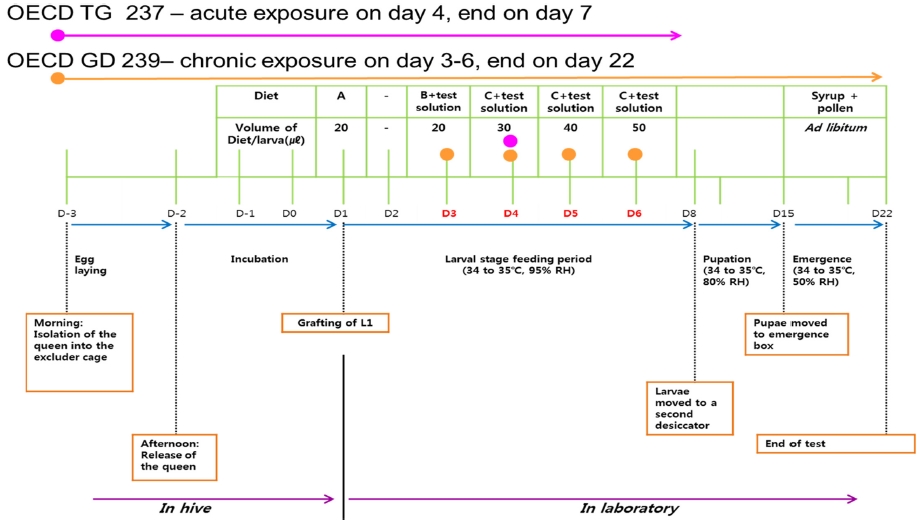
Schematic representation of the important steps of the larval acute and chronic toxicity test (D=day; RH=relative humidity). Adapted from OECD (2016).
이충하기 전 48 well plate (SPL, Korea)에 grafting cell cup (Niocoplast Society, France)를 넣고 유충먹이 A를 20 μl 주입 후 1일령 유충을 이충침(chinese grafting tool)을 이용하여 이충하였다. Grafting cell cup은 사용하기 전 70% 에탄올에 1시간 이상 담구어 소독하였으며 lamina-flow 후드에서 건조시킨 후 사용하였다.
유충먹이
유충먹이는 A, B, C 타입의 총 3종류로 구성은 Table 1과 같다. 증류수에 yeast extract (Bacto, Sparks, USA), dextrose (Difco, Sparks, USA), D-fructose (Junsei, Japan)를 넣어 혼합한 후 0.20 μm 필터(Sartorius, Germany)로 여과하였다. 여과한 용액과 로얄젤리(여주꿀벌농원, 한국)를 혼합하여 유충먹이를 제조하였다. 로얄젤리는 구입 직 후 소량으로 나누어 냉동(-20oC 이하) 보관하였으며 유충먹이 제조시마다 상온에 녹여 사용하였다. 유충먹이는 제조 후 +5oC 이하로 냉장보관하고 보관한지 3일 이상 지나면 폐기하며 유충에게 급여하기 전 유충의 생육온도인 35oC에 맞추고 생성된 기포를 충분히 제거한 후 사용하였다. 단회 및 반복노출 시험에서, 시험 1일차(D1)에 유충먹이 A를 20 μl, 시험 3일차(D3)에 유충먹이 B를 20 μl, 시험 4일차(D4)부터 6일차(D6)에 유충먹이 C를 30-50 μl 급여하였다.
약제처리
무처리군, 용매대조군, 양성대조군과 imidacloprid 5개 농도 처리군을 시험하였다. 각 시험군은 3반복씩 시험하였고 각 반복은 다른 봉군에서 이충한 유충으로 시험하였다. 추가적으로 시험 plate를 준비하여 1일차 유충을 이충하였고 시험 4일차(D4)에 처리군 및 대조군에서 죽은 유충이나 상태가 좋지 않은 유충을 건강한 개체로 대체하였다. 시험 4일차(D4)에 각 처리군마다 36마리 유충(12 larvae × 3 colonies = 36 larvae)에게 처리물질을 포함한 유충먹이 C를 30 μl씩 급여하였다. 양성대조군으로는 dimethoate을 사용하여 시험 4일차에 8.8 μg/larva로 처리하였으며 3반복 시험하였다.
100% 치사율이 발생하는 농도와 무처리군과 유의적 차이가 없는 치사율 발생 농도 구간을 결정하기 위한 예비시험을 수행하였다. 예비 시험 결과를 바탕으로 LC50을 구하기 위한 imidacloprid 처리군 5개 농도는 300.0, 120.0, 48.0, 19.20, 7.68 mg/l으로 처리하였다. 처리군 농도를 유충 한 마리 당 노출된 양으로 변환하면 9.00, 3.60, 1.44, 0.58, 0.23 μg/larva 이었다. Imidacloprid를 아세톤에 녹여 stock solution을 만든 후 유충먹이 C에 혼합하여 처리 농도별로 시험 4일차(D4)에 유충먹이를 급여하였으며 이때 먹이 중 용매의 함량은 3.45% 이었다.
단회노출 시험과 같이 시험군은 무처리군, 용매대조군, 양성대조군과 imidacloprid 5개 농도 처리군으로 정하였으며 각 처리군은 유충 12마리씩 3반복 시험을 수행하였다. 양성대조군으로는 dimethoate을 사용하여 시험 기간(D3-D6) 동안 노출된 총 양이 7.39 μg/larva가 되게 처리하였으며 3반복 시험하였다.
시험 3일차(D3)부터 6일차(D6)까지 총 140 μl의 먹이를 유충에게 공급하였으며 5개의 농도로 처리하였다. 시험 3일차(D3)부터 6일차(D6) 동안 유충에게 처리하는 각 처리군별 imidacloprid 총 양은 각각 9.00, 3.60, 1.44, 0.58, 0.23 μg/larva이었다(Table 2). Imidacloprid를 아세톤에 녹여 stock solution을 만든 후 시험 3일차(D3)에 유충먹이 B와 stock solution을 혼합하여 20 μl씩 급여하였고 시험 4일차(D4)부터 시험 6일차(D6)까지 유충먹이 C에 stock solution을 혼합하여 각각 30, 40, 50 μl씩 급여하였다. 급여 먹이 중 용매의 함량은 0.5% 이었다.
유충사육조건
단회노출 시험의 경우 이충이 완료된 시험 1일차(D1)부터 48 well-plate를 K2SO4 (Junsei, Japan) 포화용액을 이용하여 상대습도가 95±5%로 유지되는 데시게이터(Nalgene, USA, 30 × 30 × 45 cm) 안에 넣고, 데시게이터를 항온 인큐베이터(DAIHAN Scientific Co., Korea) 안에 넣어 온도를 34~35oC로 유지하였다. 인큐베이터는 일정한 암조건을 유지하였으며 사육조건을 이탈한 시간이 일일 15분을 초과하지 않도록 하였다.
반복노출 시험의 경우 시험 1일차부터 7일차(D1-D7)까지 단회노출 시험과 같은 조건으로 시험하였다. 시험기간(D1-D21) 동안 인큐베이터 온도는 34~35oC로 유지하였다. 시험 8일차(D8)에 48 well-plate을 NaCl(Sigma-Aldrich, USA) 포화용액을 이용하여 상대습도를 80±5%로 유지한 데시게이터로 이동하였고, 시험 15일차(D15)에 48 well-plate을 우화박스(emergence box)에 옮겨 상대습도를 50%로 유지하였다. 우화박스(180 × 115 × 130 mm) 뚜껑에는 공기가 통할 수 있도록 망사로 구역을 만들었으며 50% 자당용액을 공급할 수 있는 장치를 설치하였다.
치사개체 및 이상증상 확인
단회노출의 경우 시험 4일차(D4)에 약제를 노출하고 24, 48시간 후 먹이를 급여하기 전 치사개체 및 이상증상을 관찰하였으며, 약제 노출 72시간 후 추가적인 먹이 급여 없이 치사개체 및 이상증상과 먹이를 남긴 유충의 수를 기록하고 실험을 종료하였다. 유충색이 불투명해지거나 이충침으로 살짝 건드려도 움직임이 관찰되지 않을 때 죽은 것으로 간주하였다.
반복노출의 경우 시험 3일차(D3)에 약제를 최초 노출한 후 시험 4-6일차(D4-D6)에 정해진 시간에 약제를 노출하였다. 시험 4-6일차(D4-D6)에 약제를 노출하기 전 치사개체 및 이상증상을 관찰하였으며 시험 7일차(D7)에 추가적인 먹이와 약제의 급여 없이 치사개체 및 이상증상을 관찰하였다. 시험 8일차(D8)에 치사개체 및 이상증상을 기록하고 상대습도가 80±5%인 데시케이터로 이동하였다. 시험 11-13일차(D11-D13), 시험 15일차(D15)에 번데기 치사개체 및 이상증상을 기록하고 우화박스에 plate를 옮긴 후 상대습도를 50%로 유지하였다. 시험 17일차(D17)부터 관찰종료(D22) 시까지 우화개체 및 이상증상을 관찰하였다.
우화개체 및 이상증상은 Table 3과 같이 S (surviving), AD (adult workers deformed), FM (failed molt), FA (failed adult molt), MD (melanizing death)로 총 6개 그룹으로 분리하여 관찰 기록하였다. S는 번데기가 성공적으로 우화하여 정상적인 성충이 된 경우, AD는 번데기가 우화하여 기형을 가진 성충이 된 경우, FM은 머리, 몸통에서 번데기의 외관적인 특징을 관찰할 수 있으나 불완전한 번데기 상태로 죽는 경우, FA는 번데기가 최종 탈피에 실패하여 우화하지 못하고 죽는 경우, MD는 유충이 어두운 색을 띄거나 검은 반점을 보이며 죽는 경우, ED는 유충이 번데기 단계로 넘어가기 이전에 갈변화가 일어나거나 먹이에 잠겨 죽는 경우에 해당한다.
통계처리
꿀벌 유충의 imdacloprid 단회 및 반복노출의 LC50과 LD50 산출은 미국 EPA에서 제공하는 Probit 통계 프로그램(EPA analysis program probit, Version 1.5)을 이용하였다. 유충 치사율, 번데기 치사율, 우화율에서 imidacloprid 처리군과 대조군의 통계적 유의성을 판단하기 위해 SPSS software(IBM Armonk, NY, USA)를 사용하였다. 카이제곱 검정(Pearson’s chi–square test)을 실시하였고 기대빈도가 5보다 작은 셀이 전체의 25% 이상인 경우 Fisher의 정확성 검정(Fisher’s exact test)의 결과를 해석하였다. P<0.05를 통계적으로 유의한 것으로 판단 하였다.
결과 및 고찰
양성대조군 독성
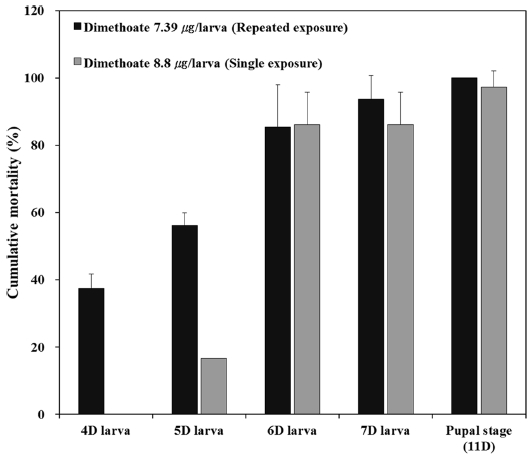
단회 및 반복노출 시험의 양성대조군 dimethoate 치사율을 Fig. 2에 나타내었다. 단회노출 dimethoate 처리군은 처리 후 72시간 누적 치사율이 86.11% 이었다. 반복노출 dimethoate 처리군은 시험 7일차(D7)에서 누적 치사율이 93.8% 이었고 시험 22일차(D22)에서 우화율이 0%였다. 단회 및 반복노출 시험의 유충 치사율은 양성대조군 유충 치사율이 50% 이상이어야 한다는 OECD 시험조건에 부합하였다.
Imidacloprid의 꿀벌 유충 단회노출 영향
Table 4는 시간에 따른 imidacloprid 처리군별 치사율을 나타낸다. 0.23, 0.58 μg/larva 처리군에서는 72시간 유충 누적 치사율이 30% 이하였고 1.44, 3.60, 9.00 μg/larva 처리군에서는 유충 누적 치사율이 70% 이상이였다. 3.60 μg/larva 처리군의 24시간, 48시간 후의 치사율이 1.44 μg/larva 처리군보다 더 높았지만 72시간에서는 두 처리 군 모두 누적치사율이 같았다. Table 5는 시험물질 처리 72시간 후 먹이가 남아 있는 유충 수를 나타낸다. 1.44 μg/larva 이상 처리군에서는 살아있는 유충 모두 먹이가 남았으며 유충이 살아 있어도 크기가 무처리군에 비해서 작았다. 0.58 μg/larva, 0.23 μg/larva 처리군에서는 살아있는 개체 중 각각 74%, 39.3%가 먹이가 남았다. 반면 무처리군과 용매 대조군에서는 먹이가 남아있는 유충이 없었다. 이는 imidacloprid가 저농도로 노출되어도 유충의 발달에 영향을 줄 수 있다는 것을 의미한다.
Starŏn et al. (2017)는 formetanate가 꿀벌 유충에 미치는 영향에 대한 연구를 수행하였으며 시험 7일차에 처리 농도별 유충 치사율과 살아있는 유충의 남아있는 먹이 양을 조사하였다. 그 결과 formetanate 432.9 mg/kg 처리군에서 36마리 유충 중 19마리가 생존했지만 그 중 12마리는 발달이 저해된 상태로 먹이가 남아 있는 상태였다. 저자는 꿀벌 유충의 남아 있는 먹이는 유충 성장저해현상과 함께 나타날 수 있다고 보고하였다.
꿀벌 독성을 나타낼 때 고독성(LD50= 0.001 – 1.99 μg/bee), 중간독성(LD50= 2.0 – 10.99 μg/bee), 저독성(LD50 >11 μg/bee)으로 분류한다(Hardstone and Scott, 2010). 본 연구에서는 LD50 값이 1.465 μg/larva 이고 이는 독성 스케일로 보았을 때 고독성에 속한다(Table 6). 참고문헌에 의하면 imidacloprid의 꿀벌 접촉 및 섭식 LD50 값은 각각 0.061, 0.013 μg/bee로 고독성이고 유충 LD50 값에 비해 24배 정도 독성이 높다(Sanchez-Bayo and Goka, 2014). 이 결과는 꿀벌 유충이 성체보다 imidacloprid에 대한 독성 민감도가 낮다는 것을 보여준다. 최근 imidacloprid 뿐만 아니라 thiamethoxam과 formetanate에 대한 유충 독성영향 연구에서도 유충이 성체에 비해 독성 민감도가 낮다고 보고된 바 있다(Dai et al., 2017; Staron et al., 2017; Tavares et al., 2015). Imidacloprid는 모든 nAChR에 작용하는 것이 아니라 특정 nAChR에 작용을 한다고 알려져 있다(Decourtye et al., 2004). 꿀벌은 11개의 nAChR subunit을 가지고 있고 각 subunit은 각기 다른 꿀벌 발육과정에서 발현된다(Jones et al., 2006). Imidacloprid의 주요 타겟이 되는 nAChR은 유충 초기 단계에서 형성이 되지 않는다(Yang et al., 2012). 이는 imidacloprid에 대한 유충과 성체의 독성 민감도 차이를 설명할 수 있는 주요 요인이 될 수 있다.
Imidacloprid의 꿀벌 유충 반복노출 영향
Fig. 3은 주요 일자별 누적 치사율을 나타낸다. 시험 8일차(D8)에 용매대조군 유충치사율은 5.56%, 0.23 μg/larva 처리군에서는 0.00%, 0.58 μg/larva 처리군에서는 2.78%였다. 용매 대조군의 치사율은 15% 이하로 OECD 기준에 적합하였다. 용매 대조군과 0.23 μg/larva 처리군의 시험 22일차(D22) 유충 치사율은 22.22% 이였다. 최고 농도 9.00 μg/larva 처리군에서는 시험 22일차(D22)에 유충이 100% 치사했으며 0.58, 1.44, 3.60 μg/larva 처리군에서 각각 36.11, 58.33, 86.11% 치사하였다.
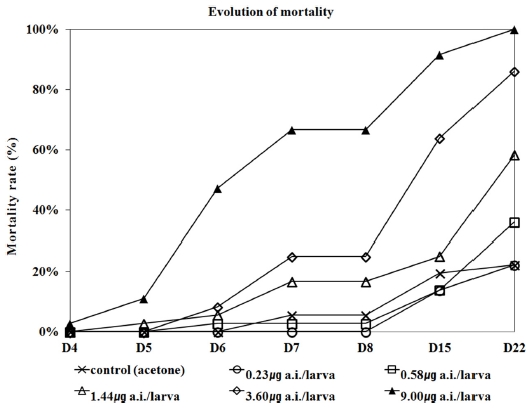
Evolution of mortality after oral application of five concentration of imidacloprid from day 4(D4) to day 22(D22).
용매대조군의 우화율은 77.78%로 우화율이 70%이상 되어야하는 OECD 기준에 적합하였다. 0.23 μg/larva 처리군의 우화율도 77.78%로 용매 대조군과 같았다. 1.44, 3.60 μg/larva 처리군에서는 우화율이 50% 이하였으며 최고 농도 처리군에서는 우화개체가 없었다. 용매 대조군 및 0.23, 0.58, 1.44 μg/larva 처리군의 치사증상은 유충치사율보다 번데기 치사율이 더 높았다. 이와 반대로 9.00 μg/larva 처리군에서는 유충 단계에서 약 70% 이상이 죽고 번데기 단계에서 30% 정도가 치사하였다(Fig. 4).
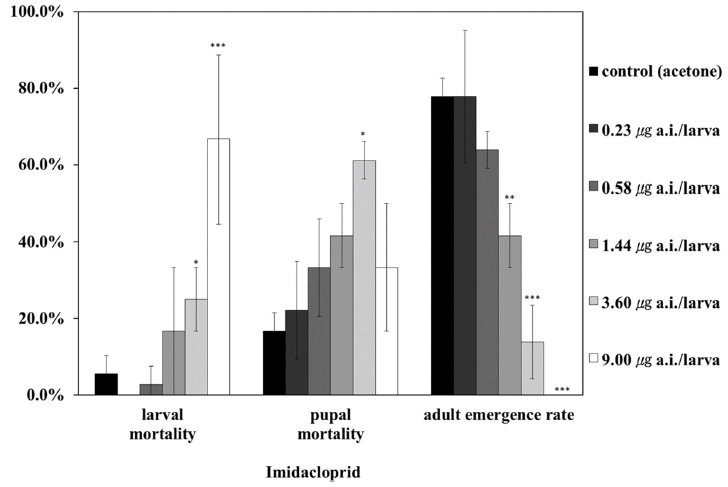
Laval mortality, pupal mortality and adult emergence rate of honeybees exposed to imidacloprid. The comparisons between exposed groups and control were performed with Chi-square test and Fisher's exact test (*P≤0.05, **P≤0.01 and ***P≤0.001) (n=36 individuals per group from 3 replicates).
Table 7은 imidacloprid 반복노출 시험 후 LC50 과 LD50값을 나타낸다. 시험 후 8일차(D8), 15일차(D15), 22일차(D22)의 LC50 값은 각각 45.078. 23.676, 10.778 mg/l 이었다. LD50 값은 각각 6.311, 3.315, 1.510 μg/larva 이었다.
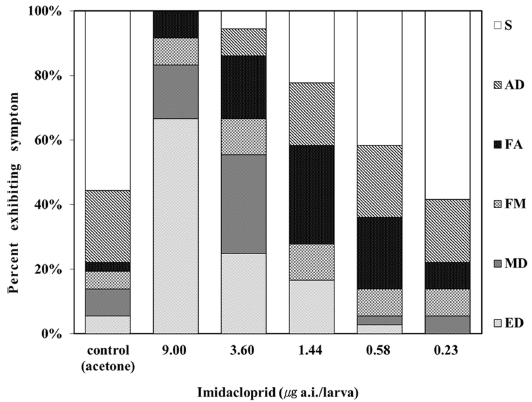
Fig. 5는 용매대조군과 imidacloprid 처리군 별 치사개체 증상 및 성공적으로 우화한 비율을 나타내었다. Fig. 6은 본 시험에서 관찰된 시험 일자 별 정상개체와 이상증상 개체의 예시를 보여준다. 9.00 μg/larva 처리군에서는 ED가 66.7%로 유충 치사율은 대부분 시험 8일차(D8) 이전에 발생하였다. 3.6 μg/larva 처리군의 치사증상은 MD가 30.6%로 가장 많이 차지했고 그 다음이 ED가 25%를 차지하였다. 1.44 μg/larva 처리군에서는 22.2%가 성공적으로 우화하였고 ED가 16.7%, FM이 11.1%, FA가 30.6%, AD가 19.4%를 차지하였다. 0.58 μg/larva 처리군은 41.7%가 성공적으로 우화하였고 AD가 22.2% FA가 22.2%, FM이 8.3%, MD가 2.8%, ED가 2.8%였다. 0.23 μg/larva 처리군은 시험 8일차(D8) 이전에 죽은 치사개체가 없었고 S가 58.3%, AD가 19.4%, FA가 8.3%, FM이 8.3%, MD가 5.6%를 차지하였다.
유충단계와 번데기 단계의 치사개체를 보면 약제 처리양이 증가할수록 치사개체 증상이 유충단계에서 죽거나, 갈변화되어서 죽는 경우가 많았고, 약제 처리양이 감소할수록 치사개체 증상 중 FM과 FA의 비율이 ED와 MD의 비율보다 더 높았다.
용매 대조군에서는 우화율이 77.78% 인데 이 중 AD가 22.2%, S가 55.6%를 차지하였다. 0.23 μg/larva 처리군에서도 용매대조군과 비슷하게 AD가 19.4%, S가 58.3%를 차지하였다. 실제 벌통 내부에서 유충은 세로로 세워져 있는 소비판에서 성장하는 반면 실험실에서 유충을 사육할 때는 plate를 수평으로 놓고 기르게 된다. 이로 인해 꼽추 등(humpback) 또는 날개 기형(wing deformation) 현상이 일어날 수 있다고 알려져 있다(Brodschneider et al., 2009). 이는 본 시험에서 저농도 또는 용매대조군에서 AD가 우화개체 중 약 20% 정도 발생한 것을 설명할 수 있다. 선행연구에서는 이런 현상을 방지하기 위해 plate를 얇은 왁스층으로 덮고 우화박스에 세로로 부착하여 가능한 벌통내부와 비슷한 환경을 만들어 시험을 하였다(Tavares et et al., 2017) .
Tavares et al. (2017)은 thiamethoxam을 0.00001 ng a.i/μl, 0.001 ng a.i/μl, 1.44 ng a.i/μl 농도로 유충에 노출시켰고 0.001 ng/μl 처리군에서는 유충 치사율이 무처리군과 통계적으로 유의한 차이가 없었지만 번데기 치사율과 우화율에는 통계적으로 유의한 영향을 미친 결과를 보고하였다. 또한 Grillone et al. (2017)은 꿀벌 유충 발달 과정 중 thiamethoxam이 0.2, 0.5 mg/l 농도로 노출되었을 때 유충의 갈변현상, 성장 지연, 기형 성체 발생 등을 포함한 반치사(sublethal) 영향을 준다는 사실을 발견하였다.
Yang et al. (2012)은 imidacloprid를 0.4 ng/larva에서 8000 ng/larva까지 꿀벌 유충에 노출시켜 번데기화율(pupation rate), 우화율(eclosion rate)을 관측하였고 0.4 ng/larva에서는 imidacloprid가 유충 우화율에 영향을 주지 않았고 24 ng/larva 부터 8000 ng/larva까지 노출양이 증가함에 따라 우화율이 통계적으로 유의하게 감소하는 것을 발견하였다. 또한 유충을 imidacloprid 0.0004-0.4 ng/larva로 처리하였을 때 0.04 ng/larva 이상 처리군에서 유충이 우화한 후 꿀벌 후각 행동이 영향을 받는 것을 발견하였다. 즉 imidacloprid가 유충 치사율에 영향을 주는 농도가 아닌 매우 저농도로 노출되어도 성체의 기억 및 학습능력에 영향을 줄 수 있다는 것이다.
본 시험에서 최저 농도처리군인 imidacloprid 0.23 μg/larva에서 우화율은 무처리군과 통계적으로 유의한 차이를 보이지 않았지만 선행연구 결과에 의하면 성체에서 기억 및 학습능력, 화분매개활동에 영향을 받을 것이라고 예상할 수 있다.
본 연구에서는 유충 단회 및 반복노출 시험법을 통해서 imidacloprid의 LD50 값을 구하였고 치사 및 이상증상을 관찰하였다. 향 후 본 연구에서 구축된 시험법을 활용하여 네오니코티노이드계 농약의 환경 중 검출 양으로 꿀벌 유충에 노출시켜 농약이 실제 유충단계뿐만 아니라 성체단계에서 어떤 영향을 미치는지 보다 정밀한 조사가 필요할 것이라고 생각된다.
Acknowledgments
본 연구는 국립농업과학원 기관고유 연구사업(과제번호: PJ013516)에 의해 수행되었습니다. 이에 감사드립니다.
References
-
Aupinel, P., D. Fortini, B. Michaud, F. Marolleau, J. B. Tasei and J. F. Odoux (2007) Toxicity of dimethoate and fenoxycarb to honey bee brood (Apis mellifera), using a new in vitro standardized feeding method. Pest Manag. Sci. 63(11):1090-1094.
[https://doi.org/10.1002/ps.1446]

-
Beekman, M and F. L. W. Ratnieks (2000) Long-range foraging by the honey-bee, Apis mellifera L. Funct. Ecol. 14(4):490-496.
[https://doi.org/10.1046/j.1365-2435.2000.00443.x]

-
Blacquiere, T., G. Smagghe, C. A. M. van Gestel and V. Mommaerts (2012) Neonicotinoids in bees: a review on concentrations, side-effects and risk assessment. Ecotoxicology. 21(4):973-992.
[https://doi.org/10.1007/s10646-012-0863-x]

- Bortolotti, L., R. Montanari, J. Marcelino, P. Medrzycki, S. Maini and C. Porrini (2003) Effects of sub-lethal imidacloprid doses on the homing rate and foraging activity of honey bees. Bull Insect. 56(1):63-67.
-
Brodschneider, R., U. Riessberger-Galle and K. Crailsheim (2009) Flight performance of artificially reared honeybees (Apis mellifera). Apidologie 40(4):441-449.
[https://doi.org/10.1051/apido/2009006]

-
Brown, L. A., M. Ihara, S. D. Buckingham, K. Matsuda and B. D. Sattelle (2006) Neonicotinoid insecticides display partial and super agonist actions on native insect nicotinic acetylcholine receptors. J. Neurochem. 99(2):608-615.
[https://doi.org/10.1111/j.1471-4159.2006.04084.x]

-
Chauzat, M. P and J. P. Faucon (2007) Pesticide residues in beeswax samples collected from honey bee colonies (Apis mellifera L.) in France. Pest Manag. Sci. 63(11):1100-1106.
[https://doi.org/10.1002/ps.1451]

-
Crailsheim, K., R. Brodschneider, P. Aupinel, D. Behrens, E. Genersch, J. Vollmann and U. Riessberger-Gallé (2012) Standard methods for artificial rearing of Apis mellifera larvae. J. Apic. Res. 52(1):1-16.
[https://doi.org/10.3896/IBRA.1.52.1.05]

-
Dai, P., C. J. Jack, A. N. Mortensen and J. D. Ellis (2017) Acute toxicity of five pesticides to Apis mellifera larvae reared in vitro. Pest Manag. Sci. 73(11):2282-2286.
[https://doi.org/10.1002/ps.4608]

-
Decourtye, A., C. Armengaud, M. Renou, J. Devillers and S. Cluzeau (2004) Imidacloprid impairs memory and brain metabolism in the honeybee (Apis mellifera L.). Pestic. Biochem. Physiol. 78(2):83-92.
[https://doi.org/10.1016/j.pestbp.2003.10.001]

-
Decourtye, A., E. Lacassie and M. H. Pham-Delegue (2003) Learning performances of honeybees (Apis mellifera L.) are differentially affected by imidacloprid according to the season. Pest Manag. Sci. 59(3):269-278.
[https://doi.org/10.1002/ps.631]

-
Eiri, D. M and J. C. Nieh (2012) A nicotinic acetylcholine receptor agonist affects honey bee sucrose responsiveness and decreases waggle dancing. J. Exp. Biol. 215(12):2022-2029.
[https://doi.org/10.1242/jeb.068718]

- Elbert, A., B. Becker, J. Hartwig and C. Erdelen (1991) Imidacloprid - a new systemic insecticide. Pflanzenschutz-Nachr Bayer. 44(2):113-136.
-
Fine, J.D., D.L. Cox-Foster and C.A. Mullin (2017) An inert pesticide adjuvant synergizes viral pathogenicity and mortality in honey bee larvae. Sci. Rep. 7(1):40499.
[https://doi.org/10.1038/srep40499]

-
Grillone, G., D. Laurino, A. Manino and M. Porporato (2017) Toxicity of thiamethoxam on in vitro reared honey bee brood. Apidologie. 48(5):635-643.
[https://doi.org/10.1007/s13592-017-0506-6]

-
Hardstone, M. C. and J. G. Scott (2010) Is Apis mellifera more sensitive to insecticides than other insects? Pest Manag. Sci. 66(11):1171-1180.
[https://doi.org/10.1002/ps.2001]

-
Im, J. T., K. M. Chon, K. H. Park, Y. S. Choi, M. L. Lee, H. Y. Kwon, J. Kim, S. M. Ryu, B. C. Moon and M. K. paik (2016) Acute Toxicity of Larval Honeybee to the Most Common Pesticides Detected in Pollen. J. Apic. 31(4):273-279.
[https://doi.org/10.17519/apiculture.2016.11.31.4.273]

-
Johnson, R. M., M. D. Ellis, C. A. Mullin and M. Frazier (2010) Pesticides and honey bee toxicity–USA. Apidologie. 41(3):312-331.
[https://doi.org/10.1051/apido/2010018]

-
Jones, A. K., V. Raymond-Delpech, S. H. Thany, M. Gauthier and D. B. Sattelle (2006) The nicotinic acetylcholine receptor gene family of the honey bee, Apis mellifera. Genome Res. 16(11):1422-1430.
[https://doi.org/10.1101/gr.4549206]

- Korea Crop Protection Association (2018) Agrochemical Year Book.
-
Mullin, C. A., M. Frazier, J. L. Frazier, S. Ashcraft, R. Simonds, D. vanEngelsdorp and J. S. Pettis (2010) High levels of miticides and agrochemicals in north American apiaries: implications for honey bee health. PLoSOne. 5(3):e9754.
[https://doi.org/10.1371/journal.pone.0009754]

- OECD guideline for the testing of chemicals. Test no. 237 (2013) honey bees (Apis mellifera) larval toxicity test, single exposure.
- OECD Guidance Document No. 239 (2016) Guidance document on honey bee larval toxicity test following repeated exposure. Series on testing and assessment. Number 239:7-41.
-
Paik, M. K., J. T. Im, K. M. Chon, K. H. Park, Y. S. Choi, M. L. Lee, C. H. Bae, J. H. KIM and B. C. Moon (2016) Synergistic and Antagonistic Interactions for Pesticide mixtures to Honeybee Larvae Toxicity. Korean J. Environ. Agric. 35(4):241-246.
[https://doi.org/10.5338/KJEA.2016.35.4.32]

-
Ramirez-Romero, R., J. Chaufaux and H. M. Pham-Delegue (2005) Effects of Cry1Ab protoxin, deltamethrin and imidacloprid on the foraging activity and the learning performances of the honeybee Apis mellifera, a comparative approach. Apidologie. 36(4):601-611.
[https://doi.org/10.1051/apido:2005039]

-
Sanchez-Bayo, F and K. Goka (2014) Pesticide residues and bees–a risk assessment. PLoS ONE. 9(4):e94482.
[https://doi.org/10.1371/journal.pone.0094482]

-
Schmehl, D. R., H. V. V. Tome, A. N. Mortensen, G. F. Martins and J. D. Ellis (2016) Protocol for the in vitro rearing of honey bee (Apis mellifera L.) workers. J. Apic. Res. 55(2):113-129.
[https://doi.org/10.1080/00218839.2016.1203530]

-
Starŏn, M., R. Sabo, A. Sobeková, L. Sabová, J. Legáth, L. Lohajová and P. Javorský (2017) Formetanate toxicity and changes in antioxidant enzyme system of Apis mellifera larvae. Environ. Sci. Pollut. Res. 24(16):14060-14070.
[https://doi.org/10.1007/s11356-017-8966-9]

-
Tavares, D. A., C. Dussaubat, A. Kretzschmar, S. M. Carvalho, E. C. Silva-Zacarin, O. Malaspina, G. Berail, J. Brunet and L. P. Belzunces (2017) Exposure of larvae to thiamethoxam affects the survival and physiology of the honey bee at post-embryonic stages. Environ. Pollut. 229:386-393.
[https://doi.org/10.1016/j.envpol.2017.05.092]

-
Tavares, D. A., T. C. Roat, S. M. Carvalho, E. C. M. Silva-Zacarin and Malaspina O (2015) In vitro effects of thiamethoxam on larvae of Africanized honey bee Apis mellifera (Hymenoptera: Apidae). Chemosphere. 135:370-378.
[https://doi.org/10.1016/j.chemosphere.2015.04.090]

-
Tosi, S., C. Costa, U. Vesco, G. Quaglia, and G. Guido (2018) A 3-year survey of Italian honeybee-collected pollen reveals widespread contamination by agricultural pesticides. Sci. Total Environ. 615:208-218.
[https://doi.org/10.1016/j.scitotenv.2017.09.226]

-
Wu, J. Y., C. M. Anelli and W. S. Sheppard (2011) Sub-lethal effects of pesticide residues in brood comb on worker honey Bee (Apis mellifera) development and longevity. PLoS One 6(2):e14720.
[https://doi.org/10.1371/journal.pone.0014720]

-
Wu-Smart, J and M. Spivak (2016) Sub-lethal effects of dietary neonicotinoid insecticide exposure on honey bee queen fecundity and colony development. Sci. Rep. 6(1):32108.
[https://doi.org/10.1038/srep32108]

-
Yang, E. C., H. C. Chang, W. Y. Wu and Y. W. Chen (2012) Impaired olfactory associative behavior of honeybee workers due to contamination of imidacloprid in the larval stage. PLoS ONE. 7(11):e49472.
[https://doi.org/10.1371/journal.pone.0049472]

-
Zhu, W., D. R. Schmehl, C. A. Mullin and J. L. Frazier (2014) Four common pesticides, their mixtures and a formulation solvent in the hive environment have high oral toxicity to honey bee larvae. PLoS ONE. 9(1):e77547.
[https://doi.org/10.1371/journal.pone.0077547]