
Pseudomonas viridiflava에 의한 큰꽃삽주 세균썩음병 발생 및 방제 농약 선발
초록
2016년에서 2017년에 걸쳐 국내 큰꽃삽주(Atractylodes macrocephala Koidz)를 재배하는 농가에서는 잎 가장자리가 썩어 들어가고 줄기와 뿌리까지 썩는 현재까지 보고되지 않은 새로운 병이 발생하여 그 피해가 막심하였다. 때문에 본 연구에서는 큰꽃삽주에 썩음증상을 일으키는 원인불명의 병에 대해 원인균을 분리, 동정하고 병원성을 검정하였으며 실내와 포장 실험을 통해 방제효과가 높은 농약을 선발하고자 수행하였다. 병든 부위로부터 콜로니의 색, 모양, 크기가 구별되는 9개 type의 세균을 순수 분리하였고 잎 절편과 식물체를 이용한 병원성 검정을 통해 유일하게 병원성을 보이는 한 종의 세균을 확인하였다. 16S rRNA 염기서열 분석에 기반 하여 큰꽃삽주에 썩음증상을 일으키는 균은 토양 내에 널리 존재하는 그람음성세균인 Pseudomonas viridiflava로 동정하였다. 실내실험과 포장검정을 통해 콜로니 생성 억제 효과가 뛰어나고 70% 이상의 병 방제효과를 보여 약효가 우수하고 약해가 없는 oxytetracycline 수화제, kasugamycin 입상수화제, oxolinic acid 수화제 등 3종의 농용항생제를 최종 선발하였다. 향후 선발한 약제는 P. viridiflava 에 의해 발생하는 큰꽃삽주의 세균썩음병(가칭)을 효과적으로 방제하는 방제제로 사용할 수 있을 것으로 기대한다.
Abstract
During 2016 to 2017, devastating bacterial rot symptom had been observed on Atractylodes macrocephala Koidz. in several cultivated fields in Yeongju-si and Jecheon-si. This experiment was carried out to identify a casual pathogen that has not been reported up to now from A. macrocephala and to selecte effective pesticide. Nine types of distinguishable bacterial isolates were isolated from the diseased leaves. Only one isolate caused dark brown leaf rot by leaf section assay and confirmed the pathogenicity of the isolate by artificial infection with potted plants. On the basis of 16S rRNA sequence analysis, the isolate isolated from A. macrocephala was identified as Pseudomonas viridiflava. Antibiotics test showed that streptomycin wettable powder (WP) and oxytetracycline + validamycin A wettable powder (WP) significantly suppressed the bacterial colony formation of P. viridiflava. However, validamycin A soluble concentrate (SC) did not show the positive inhibition effect on bacterial colony formation. The five bactericides were also applied in the two places of field. Foliar application of oxytetracycline wettable powder (WP), kasugamycin water dispersible granule (WG), and oxolinic acid wettable powder (WP) on the naturally infected A. macrocephala showed high control value (above 70%). These results showed that the bacterial rot of the A. macrocephala is caused by P. viridiflava and can be effectively controlled by selected bactericides.
Keywords:
Atractylodes macrocephala, Bacterial rot, Bactericides, Pseudomonas viridiflava키워드:
Atractylodes macrocephala, Pseudomonas viridiflava, 세균썩음병, 농용항생제서 론
국화과(Compositae), 삽주속(Atractypdes spp.)에 속하는 큰꽃삽주(Atractylodes macrocephala Koidz.)는 국내에 자생하는 삽주(Atractylodes japonica Koidz.)에 비해 생산성이 우수하므로 중국으로부터 국내에 도입되어 재배가 늘어나고 있는 작물이다(MAFRA., 2019). 큰꽃삽주와 삽주의 뿌리줄기를 그대로 또는 주피를 제거한 것을 한약재명으로 백출(白朮)이라 부르는데(MFDS, 2019; Lee et al., 2002), 백출은 예로부터 소화능력 개선과 위장 보호의 효과가 인정되어 십전대보탕(十全大補湯), 팔물탕(八物湯) 등 대표적인 한의약 처방에 포함되는 한약재이지만 대표적 수입 의존 한약재로서 국내 재배면적은 경작지와 임야를 포함하여 31 ha로 82톤을 생산하고 있다(MAFRA, 2019). 현재까지 삽주에 발생하는 병해로는 Colletotrichum gloeosporioides에 의한 탄저병, Sclerotium rolfsii에 의한 흰비단병, Phytophthora drechsleri에 의한 역병 등이 보고된 바 있으며(Lee et al., 1991; Kim et al., 1997) 큰꽃삽주에 발생하는 병으로는 P. drechsleri에 의한 역병이 유일하게 보고되어 있다(Kim et al., 1997). 큰꽃삽주는 농가 재배 시 장마기에 지상부가 시들어 뿌리를 포함한 식물체 전체가 썩는 역병 피해로 수확량 감소가 많은 작물이다. 또한 최근 경북 영주 및 충북 제천 등 큰꽃삽주를 재배하는 농가에서는 장마기 고온다습한 기후환경에 잎 가장자리나 상처부위가 짙은 갈색 또는 검은색으로 썩고 심하면 줄기와 뿌리가 썩는 증상이 발생하고 있으며(Fig. 1) 백출에 등록되어 있는 탄저병 방제 약제인 azoxystrobin 등 진균 적용약제 살포에도 방제 효과가 없는 원인미상의 병이 발생하여 작물 생산에 큰 문제가 되고 있다. 현재 전국적으로 1 ha 이상 재배되고 있는 약용작물은 큰꽃삽주를 포함하여 60여 작물이 있으나 한품목이라도 방제농약이 등록되어 있는 작물은 31개 작물에 불과하며 이마저도 등록된 적용약제의 수가 많지 않아 농가에서는 병해충 방제에 애로사항으로 작용하고 있다(MAFRA, 2019; RDA, 2019). 국내에서는 생산단계에서 판매단계까지의 농산식품 안전관리체계를 구축하여 소비자에게 안전한 농산물을 공급하자는 취지로 우수농산물관리제도(Good Agricultural Practice, GAP)를 2016년부터 본격적으로 시행하고 있으며 또한 2019년부터는 농약허용물질목록관리제도(Positive List System, PLS)를 시행하고 있다(RDA, 2019). 약용작물의 경우 식품의약품안전처에서는 식품의 기준 및 규격을 따르는 작물인 ‘구기자’ 등 몇 작물을 제외하고 식약공용농(임)산물로 규정한 대부분의 약용작물에 대해 PLS 적용을 제외하고 있지만 추후 적용이 예상되며 사전에 제도변화에 대응 할 필요가 있다. 따라서 본 연구에서는 큰꽃삽주 재배 시 농가에서 많은 피해를 보고 있는 미보고 병에 대해 원인균을 분리, 동정하고 병원성을 검정하였으며 실내와 포장 실험을 통해 방제효과가 높은 농약을 선발 하였기에 그 결과를 보고하고자 한다.
재료 및 방법
이병부위 오염균 분리
원인균 분리를 위해 농가포장에서 큰꽃삽주의 잎썩음 초기증상이 발생한 시료를 채집하고 건전부위를 포함한 병든 부위를 1×1 cm 크기로 잘라 1% NaOCl과 70% 에탄올에서 각각 1분 침지 후 멸균수로 용매를 깨끗이 세척하고 멸균증류수가 담긴 1.5 ml test tube에 넣어 곱게 마쇄하고, LB Agar (Tryptone 10.0 g, Yeast Extract 5.0 g, Sodium Chloride 10.0 g, Agar 15.0 g)에 100 μl를 도말하여 28oC에서 3일간 배양하였다. 이후 생성된 콜로니의 색, 모양, 크기를 기준으로 뚜렷한 차이를 보이는 단일 콜로니를 순수 분리하여 병원성 검정을 위한 시험균주로 사용하였다.
분리균주의 병원성 검정
큰꽃삽주에 잎썩음 증상을 일으키는 원인균을 확인하고자 잎 절편 접종과 식물체 접종시험을 수행하였다. 잎 절편 접종시험에서는 큰꽃삽주 이병부위로부터 분리한 각각의 균주를 1×105 cfu/ml 농도의 현탁액 10 ml를 흡수시킨 여과지를 페트리디시(150×20 mm)에 올리고 종근을 화분에 파종하고 6개월간 온실에서 생육시킨 건전한 식물체로부터 엽병을 포함한 잎을 잘라 잎의 한쪽 면만이 여과지에 닿게 치상한 후 완전히 밀봉하고 30oC 배양기에서 3일 경과 후 잎썩음 증상유무를 관찰하였다. 식물체 접종시험에서는 6개월간 생육시킨 건전한 식물체에 잎 절편 시험으로부터 병원성이 확인된 균주를 대상으로 병원성 유무를 최종 확인하고자 수행하였으며 1×105 cfu/ml 농도로 잎에서 흘러내리지 않을 정도로 분무접종하고, 30oC, 상대습도가 95% 이상인 접종상(DS-53C, Dasol Scientific Co., Hwaseong, Korea)에서 3일 배양 후 20-30oC가 유지되는 유리온실에 옮겨 병 발생 상황을 관찰하였다. 두 시험 모두 3반복 시험을 하였고 접종하지 않은 무 접종구를 대조구로 하였다.
원인균 동정을 위한 PCR 및 염기서열 분석
병원성 검정 결과 큰꽃삽주의 잎썩음 증상 원인균으로 확인된 균주를 동정하기 위해 16S rRNA 유전자 분석을 수행하였다. Genomic DNA는 병원성이 확인된 균주를 LB Agar에 도말 접종하여 30oC에서 2일간 배양 하여 균체를 수확하여 QIAamp DNA Mini kit (Qiagen, Germany)를 이용하여 추출하였다. 추출한 Genomic DNA는 16S rRNA 유전자 증폭을 위하여 27F와 1492R 프라이머를 이용하여 PCR을 수행하였다(Lane, 1991). PCR 산물은 1% agarose gel에서 전기영동 하여 DNA를 확인하였다. 이후 PCR Clean-Up System (Promega, USA)으로 정제하여, ㈜마크로젠(Seoul, Korea)에 의뢰하여 염기서열 분석을 하였다. 염기서열 분석결과는 MEGA ver. 5.0 (Tamura et al., 2011)을 이용하여 교정하고, EzTaxon-e server (http://eztaxon-e.ezbiocloud.net)와 GenBank database를 통해 기존에 보고된 16S rRNA 염기서열과 비교하여 동정하였다. 계통수는 MAFFT v7 (Katoh and Standley, 2013)을 이용해 정렬한 후 Kimura 2-parameter model (Kimura, 1980)과 1,000회 반복 bootstrapping으로 MEGA ver. 5.0을 사용하여 neighbor-joining tree를 작성하였다.
세균썩음증상 방제약제 실내 선발
큰꽃삽주 세균썩음증상은 곰팡이병인 역병과 함께 장마기 고온다습한 기상환경에서 주로 발생하여 재배 농가에 막대한 피해를 주고 있으며 현재 큰꽃삽주 탄저병 방제약제로 등록되어 있는 azoxystrobin 수화제 등 5품목은 세균에 방제효과가 없어 효과적인 농용항생제의 선발이 필요하다. 본 연구에서는 국내 시판되는 농용항생제 중 streptomycin 수화제, oxolinic acid 수화제, oxytetracycline + validamycin A 수화제, kasugamycin 액제, validamycin A 액제 등 5개 품목을 선정하여 농용항생제별 타 작물의 희석배수를 준용하여 약제배지(LB Agar + bactericides) 조제 후 잎썩음 부위로부터 분리된 모든 세균을 각각 도말하고 30oC 배양기에 7일간 치상 후 약제배지 상의 콜로니 생성 유무로 항균효과를 검정하였다.
세균썩음증상 방제약제 포장 선발
포장시험은 충북 음성과 강원 평창에 위치한 농촌진흥청 인삼특작부 시험연구포장 두 장소에서 약효, 약해시험을 수행하였으며 2017년 인삼특작부에서 채종한 큰꽃삽주 종자를 200구 연결포트에 파종하여 비닐하우스에서 2개월 육묘하였다. 정식 5개월 전 본포에 충분히 부숙된 우분퇴비(2 ton/10a)를 시용하였으며 정식 직전 두둑형성기를 이용고랑과 고랑사이를 160 cm 폭으로 두둑을 형성한 후 검은색 비닐 멀칭을 하고 한 처리구 당 30×20 cm 재식간격으로 2열로 유묘를 이식하였다. 시험구는 난괴법 3반복으로 각 처리구당 약효는 10 m2, 약해시험은 5 m2의 면적에서 수행하였으며 약제처리 전까지 타 병해충 방제를 위한 약제는 살포하지 않았다. 시험 약제는 실내 시험 결과를 바탕으로 농촌진흥청 농자재산업과로부터 추천을 받은 streptomycin 수화제, oxolinic acid 수화제, oxytetracycline 수화제, kasugamycin 입상수화제, validamycin A 입상수화제 등 단일성분 5품목을 사용하였으며 병 발생 초기에 엽면살포를 시작하여 7일 간격으로 3회를 살포하였다. 대상 농약의 약효는 최종약제 처리 7일 후 구당 10주, 주당 10엽씩 이병엽수를 조사하여 무처리 대비 방제가를 산출하였고 약해는 기준량, 배량 약제 살포 후 외관상 잎, 줄기 부위에 나타나는 이상 증상 발생을 달관에 의해 판정하였다.
결과 및 고찰
큰꽃삽주 세균썩음증상 오염균 분리 및 병원성검정
초기 병징 부위를 수거하여 표면을 살균하고 멸균증류수에 넣어 마쇄한 후 LB Agar에 도말하여 생성된 콜로니의 색, 모양, 크기가 서로 뚜렷이 구별되는 총 9 type의 세균을 순수 분리하였다(Fig. 2).
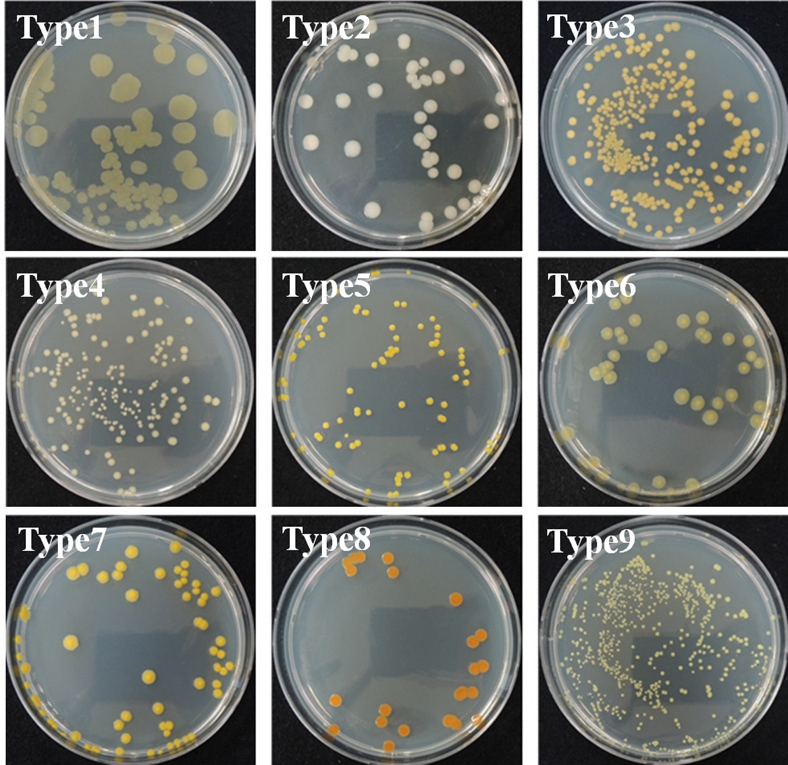
Nine types of bacterial strains isolated from leaf rot symptom in A. macrocephala. Each strain showed a different colony color, shape and size.
순수 분리한 9 type 세균의 잎 절편 접종시험에서는 type1 균주만 유일하게 접종 후 3일에 잎 끝이 썩는 증상이 발생하였으며 나머지 균주들은 10일이 지난 후 까지도 어떠한 경미한 병징도 나타나지 않았다(Fig. 3). 때문에 잎 절편 접종 실험 시 병원성을 보이는 type1 균주를 대상으로 하여 식물체 대상 확인실험을 수행하였으며 접종 후 30oC, 95% 이상 상대습도가 유지되는 접종상에서 3일간 배양한 결과 잎 가장자리부터 검게 썩는 초기 병징이 발생하였고 20-30oC가 유지되는 유리온실에 옮기고 10일이 지나 식물체가 완전히 고사하였다. 병징 부위로부터 다시 type1 세균이 분리되었고 이러한 병의 진전 양상은 농가 포장에서의 병 발생 양상과 완전히 일치하였다. 본 실험 결과로 type1 세균만이 큰꽃삽주에 썩음증상을 일으키는 세균임을 최종적으로 확인하였다(Fig. 4).

Occurrence of leaf rot symptom in leaf section assay using cutting leaves (A: A. macrocephala leaves soaked in type1 bacterial suspensions, B: non-treated control. C: leaf rot Symptom after treating type1 bacterial suspensions).
큰꽃삽주 세균썩음증상 원인균 동정
큰꽃삽주(A. macrocephala) 잎썩음 증상의 병반부로부터 분리된 균주의 16S rRNA 영역 염기서열을 분석한 결과 Pseudomonas viridiflava와 같은 그룹을 형성하였고, 기준균주인 Pseudomonas viridiflava DSM 6694와 염기서열이 일치하였다. 따라서 큰꽃삽주 잎썩음 증상으로부터 분리하여 병원성을 확인한 균주는 P. viridiflava로 최종 동정하였다(Fig. 5).

Neighbor joining tree inferred from the 16S rRNA sequences of Pseudomonas species. Bootstrap scores > 50 are presented at the nodes. The scale bar indicates the number of nucleotide substitutions per site. Bacteria isolated from A. macrocephala are indicated in bold.
P. viridiflava는 토양 내에 널리 존재하는 그람음성세균으로 뉴질랜드에서 재배하는 키위에서 최초로 병을 일으키는 세균임이 밝혀진 바 있다(Balestra and Varvaro, 1998). 이후 현재까지 P. viridiflava는 전 세계적으로 토마토, 멜론, 오이, 양배추, 양파, 상추 등 수많은 작물에서 잎, 줄기, 열매 등 식물체에 병을 일으키는 것으로 보고되어 지고 있다(Little et al., 1994; Lee et al., 2000; Aysan et al., 2003; Pérez et al., 2004; Balestra et al., 2008; Ibrahim et al., 2010; Taylor et al., 2011; Moretti et al., 2012; Végh et al., 2012; Popović et al., 2015; Wang et al., 2015; Aksoy et al., 2017; Nehaya et al., 2017; Albu et al., 2018; Seo et al., 2018). 또한 이 균은 당근, 바질, 무 등의 종자와 종묘에도 오염되어 종자 전염하는 세균으로도 보고된 바가 있다(Shakya et al., 1989; Minuto et al., 2008; Almeida et al., 2013). 본 연구에서는 큰꽃삽주에 발생하는 세균썩음증상의 원인균이 P. viridiflava임을 최초로 밝혀 P. viridiflava에 의한 큰꽃삽주 세균썩음병으로 명명하고자 제안하며 방제 농약 선발 시험을 추가로 수행하였다.
큰꽃삽주 세균썩음병 방제약제 실내 선발
잎썩음 부위로부터 분리된 9개 type의 세균을 각각 약제배지에 도말하고 콜로니 생성 유무로 항균효과를 검정한 결과 잎썩음 증상을 일으키는 원인균으로 확인 한 P. viridiflava에 대해서는 validamycin A 액제를 제외한 모든 농용항생제가 콜로니 생성 억제 효과가 있음을 확인하였다. 특히 streptomycin 수화제와 oxytetracycline + validamycin A 수화제는 분리된 9개 type 세균 모두에서 콜로니 생성을 억제하여 가장 광범위한 항균활성을 보였으며, oxolinic acid 수화제, kasugamycin 액제, validamycin A 액제는 각각 5, 3, 2종의 분리 세균에 대해 콜로니 생성 억제 효과를 보여 주었다(Table 1).
큰꽃삽주 세균썩음병 방제약제 포장 선발
충북 음성과 강원 평창 두 포장에서의 큰꽃삽주 세균썩음병 자연 발병률은 무처리 이병엽률이 각각 33.6, 27.0%로 무처리 최소발병률 20%를 초과하여 시험의 신뢰성을 확보하였다. 약효와 약해 시험의 결과 음성 포장에서는 oxytetracycline 수화제, kasugamycin 입상수화제, oxolinic acid 수화제가 각각 91.0, 86.1, 84.1%의 무처리 대비 방제가를 나타내었으나 validamycin A 입상수화제의 경우 무처리 대비 방제가가 60.3%로 낮았다. 평창 포장에서는 oxytetracycline 수화제, kasugamycin 입상수화제, oxolinic acid 수화제가 각각 93.8, 83.9, 83.9%의 무처리 대비 방제가를 나타내었고, 마찬가지로 validamycin A 입상수화제의 경우 무처리 대비 방제가가 61.7%로 매우 낮았다(Table 2). 이 결과는 validamycin A 액제가 세균썩음병의 원인균인 P. viridiflava에 대해 콜로니생성 억제효과가 없는 실내 실험경향과도 일치하는 것을 확인 할 수 있었다.
하지만 Streptomycin 수화제의 경우 두 포장 모두에서 식물체에 잎이 황화되고 갈변되는 외관상 약해를 보였다(Fig 6). Streptomycin에 의한 식물체 약해 발생은 포장 실험 당해년도(2018년 8월)의 기상환경이 초기 병 발생 이후 약제살포 기간 중 일평균 온도가 30oC가 넘는 날이 있을 정도로 고온 현상이 심했던 원인으로 판단되어 진다. 결론적으로 본 연구를 통해 큰꽃삽주 세균썩음병 방제를 위해 방제가가 높은 oxytetracycline 수화제, kasugamycin 입상수화제, oxolinic acid 수화제 등 3종의 농용항생제를 최종 선발하였다. 향후 추가 실험을 통해 광범위한 항균활성을 보였지만 약해를 보인 streptomycin에 대해 희석배수, 적정 방제시기 등에 관한 연구도 더 진행되어져야 할 것으로 판단된다.
Acknowledgments
본 연구는 농촌진흥청 시험연구사업(과제번호: PJ012669022019)의 연구비 지원에 의해 이루어진 것임.
References
- Aksoy, H. M., M. Ozturk and A. Aktas (2017) First report of Pseudomonas viridiflava causing cabbage bacterial leaf spot in Turkey. Journal of Plant Pathology 99(3):801.
-
Albu, S., M. Lai, P. W. Woods and L. B. Kumagai (2018) First Report of Pseudomonas viridiflava as the causal agent of bacterial leaf spot of Mexican heather in California. Plant Dis. 102(12):2633.
[https://doi.org/10.1094/PDIS-03-18-0405-PDN]

-
Almeida, I. M. G, K. W. Maciel, J. R. Neto and L. O. S. Beriam (2013) Pseudomonas viridiflava in imported carrot seeds. Australasian Plant Dis. Notes 8(1):17-19.
[https://doi.org/10.1007/s13314-012-0086-2]

-
Aysan, Y, M. Mirik, A. Ala, F. Sahin and O. Cinar (2003) First report of Pseudomonas viridiflava on melon in Turkey. Plant Pathology 52(6):800.
[https://doi.org/10.1111/j.1365-3059.2003.00909.x]

-
Balestra, G. M. A Mazzaglia and A Rossetti (2008) Outbreak of bacterial blossom blight caused by Pseudomonas viridiflava on Actinidia chinensis kiwifruit plants in Italy. Plant Dis. 92(12):1707.
[https://doi.org/10.1094/PDIS-92-12-1707A]

- Balestra, G. M. and L. Varvaro (1998) Seasonal fluctuations in kiwifruit phyllosphere and ice nucleation activity of Pseudomonas viridiflava. J. Plant Pathol. 80(2):151-156.
-
Ibrahim, Y. and Y. Molan (2010) Occurrence of bacterial leaf spot disease on lettuce caused by Pseudomonas viridiflava in the Kingdom of Saudi Arabia. Plant Pathology 59(2):402.
[https://doi.org/10.1111/j.1365-3059.2009.02167.x]

-
Katoh, K and D. M. Standley (2013) MAFFT multiple sequence alignment software version 7: improvements in performance and usability. Mol. Biol. Evol. 30(4):772-780.
[https://doi.org/10.1093/molbev/mst010]

- Lane, D. J. (1991) 16S/23S rRNA sequencing. In: Stackebrandt E, Goodfellow M, eds. Nucleic acid techniques in bacterial systematics. John Wiley & Sons. New York. pp.115–147.
- Kim, H. K., D. K. Kim and H. J. Jee (1997) Occurrence of rhizome rot of Atractylodes spp. caused by Phytophthora drechsleri. Plant Pathol. J. 13(6):433-437.
-
Kimura, M. (1980) A simple method for estimating evolutionary rates of base substitutions through comparative studies of nucleotide sequences. J. Mol. Evol. 16(2):111-120.
[https://doi.org/10.1007/BF01731581]

- Lee, E. J., J. K. Cha and J. E. Choi (2000) Bacterial root rot and bacterial leaf blight of Ficus spp. by Pseudomonas cichorii and P. viridiflava in Korea. Res. Plant Dis. 6(1):6-9.
- Lee, E. J., Y. H. Lee, W. D. Cho, W. G. Kim and K. S. Jin (1991) Compendium of medicinal plant diseases with colour plates. National Institute of Agricultural Science and Technology. Suwon, Korea. pp.68-70.
- Lee, J. H., Y. K. Kim, S. P. Hong and C. S. Kim (2002) Study of taxonomic origins of Atractylodis Rhizoma Alba and Atractylodis Rhizoma. Korean Journal of Oriental Medicine 8(1):55-63.
-
Little, E. L., R. L. Gilbertson and S. T. Koike (1994) First report of Pseudomonas viridiflava causing a leaf necrosis on basil. Plant Dis. 78(8):831.
[https://doi.org/10.1094/PD-78-0831D]

-
Martín-Sanz, A, J. L. Palomo, M. Pérez de la Vega and C. Caminero (2010) First report of bacterial blight caused by Pseudomonas viridiflava on pea in Spain. Plant Dis. 94(1):128.
[https://doi.org/10.1094/PDIS-94-1-0128A]

- Ministry of Agriculture, Food and Rural Affairs (MAFRA) (2019) Production results of special crops. Ministry of Agriculture, Food and Rural Affairs. Sejong, Korea. pp.41 and 60.
- Ministry of Food and Drug Safety (MFDS) (2019) The Korea pharmacopoeia. Ministry of Food and Drug Safety. Seoul, Korea. pp.44.
-
Minuto, A., G. Minuto, P. Martini, M. Odasso, E. Biondi, S. Mucini and M. Scortichini (2008) First report of Pseudomonas viridiflava in basil seedlings and plants in soilless crop in Italy. Australasian Plant Dis. Notes 3(1):165.
[https://doi.org/10.1071/DN08064]

-
Moretti, C., R. Fakhr and R. Buonaurio (2012) Calendula officinalis: a new natural host of Pseudomonas viridiflava in Italy. Plant Dis. 96(2):285.
[https://doi.org/10.1094/PDIS-08-11-0691]

-
Nehaya, A., M. Ihsan and A. Amani (2017) Isolation and Identification of Pseudomonas viridiflava, the causal agent of fruit rotting of Cucumis sativus. Jordan J. Agri. Sci. 13(1):79-91.
[https://doi.org/10.12816/0039717]

- Pérez, F., P. Silvera and W. Gepp (2004) Pseudomonas viridiflava (Burkholder) Dowson: causal agent of necrotic spots on onion and garlic (Allium spp.) leaves in Uruguay. Agrociencia 8(2):33-37.
-
Popović, T., Ž. Ivanović and M. Ignjatov (2015) First report of Pseudomonas viridiflava causing pith necrosis of tomato (Solanum lycopersicum) in Serbia. Plant Dis. 99(7):1033.
[https://doi.org/10.1094/PDIS-01-15-0052-PDN]

- Rural Development Administration (2019) Pesticides information service. http://pis.rda.go.kr, . Accessed 14 October 2019.
-
Shakya, D. D. and F. Vinther (1989) Occurrence of Pseudomonas viridiflava in seedlings of radish. J. Phytopathology 124(2):123-127.
[https://doi.org/10.1111/j.1439-0434.1989.tb04905.x]

- Seo, Y. H., M. J. Park, C. G. Back and J. H. Park (2018) First report of Pseudomonas viridiflava causing leaf spot of cucumber in Korea. Res. Plant Dis. 24(4):328-331.
-
Tamura, K., D. Peterson, N. Peterson, G. Stecher, M. Nei and S. Kumar (2011) MEGA5: molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods. Mol. Biol. Evol. 28(10):2731-2739.
[https://doi.org/10.1093/molbev/msr121]

-
Taylor, R. K., M. K. Romberg and B. J. R. Alexander (2011) A bacterial disease of hellebore caused by Pseudomonas viridiflava in New Zealand. Australasian Plant Dis. Notes 6(1):28-29.
[https://doi.org/10.1007/s13314-011-0010-1]

-
Végh, A, M. Hevesi, Zs. Némethy and L. Palkovics (2012) First report of bacterial leaf spot of basil caused by Pseudomonas viridiflava in Hungary. Plant Dis. 96(1):141.
[https://doi.org/10.1094/PDIS-09-11-0726]

-
Wang, Y., C. Y. Zeng, X. R. Chen and C. D. Yang (2015) First report of leaf blight on Saposhnikovia divaricata by Pseudomonas viridiflava in Gansu, China. Plant Dis. 99(2):281.
[https://doi.org/10.1094/PDIS-06-14-0641-PDN]




