시설재배 애호박 중 Dichlorvos와 Etofenprox 사용에 따른 경시적 잔류량 변화
 ; Ji-Yeon Bae1, †
; Ji-Yeon Bae1, † ; Deuk-Yeong Lee1
; Deuk-Yeong Lee1 ; Yeong-Jin Kim1, 2
; Yeong-Jin Kim1, 2 ; Dong-Yeol Lee3
; Dong-Yeol Lee3 ; Jin-Hyo Kim1, *
; Jin-Hyo Kim1, *
초록
파밤나방 등의 해충 방제용 살충제로 등록된 20% dichlorvos와 10% etofenprox 혼합제를 애호박 시설재배지에 살포하여 이들의 경시적 잔류변화와 생물학적 반감기 및 잔류위해성을 평가하였다. 약액 살포 당일 dichlorvos의 초기 잔류량은 애호박 열매와 잎에서 0.016-0.025 mg kg-1과 0.916-1.111 mg kg-1이었으나, 약액 살포 당일을 제외한 모든 시료에서 LOQ 미만으로 불검출 되었다. Etofenprox의 초기 잔류량은 열매에서 0.075-0.098 mg kg-1로 검출되었으나, 잠정 최대 잔류허용기준(Maximum residue limit, MRL)인 0.2 mg kg-1을 초과하지 않았고, 잎에서는 6.378-7.443 mg kg-1로 열매의 초기 잔류량보다 80배 이상 높았다. Etofenprox의 작물 잔류 반감기는 열매와 잎에서 각각 3.5일과 7.1일이었다. 약액 살포 후 3일차 잔류를 기준으로 etofenprox에 대해 평가한 호박 열매와 잎의 식이 섭취 노출에 따른 전체연령 평균 ADI 기여도는 각각 0.018%와 0.027%이었다. 또한, 연령대별 식이 섭취 위해평가 결과, 영유아(1-2세, 0.044%ADI)와 고령층(≥65세, 0.031%ADI)에서 전체연령대 평균 %ADI 보다 높게 나타나 식이 섭취 위해평가 시 이들 연령층에 대한 면밀한 검토가 필요할 것이다.
Abstract
Dichlorvos and etofenprox as insecticides were widely used for crop protection, but the residues of the pesticides in the fruit and the leaf of squash were not studied well. In here, the residues dissipation and the biological half-lives were investigated in the fruit and the leaf of squash. The residues of dichlorvos in the leaf and fruit of squash were detected 0.916-1.111 mg kg-1 and 0.016-0.025mg kg-1 on 0 day-after-treatment (DAT) respectively, but no detection showed after 3 DAT both in the fruit and in the leaf. The etofenprox residues were 0.075-0.098 mg kg-1 and 6.378-7.443 mg kg-1 on 0 DAT in the fruit and the leaf, but the residue concentration in the fruit was below the temporal maximum residue limit (0.2 mg kg-1) regardless of the harvest date. The half-lives of etofenprox in the fruit and the leaf were 3.5 and 7.1 day, respectively. In addition, the dietary exposure risks of etofenprox were estimated to 0.018% and 0.027% of acceptable daily intake (ADI) for all age group from the fruit and the leaf. Furthermore, the %ADI for the infant group (1-2-year-old, 0.044% ADI) and the elder age group (≥65-year-old, 0.031% ADI) were higher than all the age groups from the dietary of the fruit.
Keywords:
Biological half-life, Dichlorvos, Etofenprox, Residual safety, Squash키워드:
디클로르보스, 에토펜프록스, 생물학적 반감기, 잔류안전성, 애호박서 론
우리나라 국민의 먹거리 안전에 관한 인식이 높아짐에 따라 농식품 구매에서 잔류농약은 주요 고려사항이다. 한국농촌경제연구원에서 성인 6,176명을 대상으로 실시한 식품소비행태조사 결과에 따르면, 소비자가 가장 우려하는 식품위해물질은 채소, 과일의 잔류농약이 20.4%로 가장 높았으며, 중금속, 환경호르몬 등이 13.5%, 이물질 11.9%, 방사능 11.6%, 식중독균 9.3%, 축산 및 어류의 항생제 8.6%, 자연독성 7.4%, 식품첨가물 5.9% 순으로 집계되었다(KREI, 2019). 특히, 채소, 과일의 잔류농약에 대한 우려정도를 ‘매우 우려된다’ 부터 ‘전혀 우려되지 않는다’까지 5단계로 나누었을 때, ‘우려되는 편이다’ 45.0%, ‘매우 우려된다’ 24.9%, ‘보통이다’ 17.8% 순으로 조사되었다. 농산물 품질 향상 및 생산성 향상을 목적으로 사용되는 농약은 작물 별 최대 잔류허용기준(Maximum residue limit, MRL)과 농약안전사용기준 등을 설정하여 안전하게 관리되고 있고, 또한 2018년까지 시행되던 Negative List System (NLS)제도를 대체한 농약 허용물질 목록관리제도(Positive List System, PLS)가 2019년부터 모든 농산물에 대해 시행되고 있음에도 불구하고, 여전히 농산물을 섭취하는 소비자들의 불안감은 높다(Choi et al., 2018; An et al., 2019; Lee et al., 2019; Jeong et al., 2020; Oh et al., 2020; Park et al., 2020). 반면, NAQS (2017)의 2016년도 농산물 중 유해물질 잔류실태조사에 따르면 다소비농산물 54개 품목의 생산량 가중치를 반영한 평균 부적합률은 1.8%로 소비자의 우려에 비해 높지 않았고, 호박 등 과채류의 부적합률은 0.7%로 전체 부적합률 평균보다 낮은 것으로 확인되었다. 하지만 호박의 부적합율(0.8%)은 과채류 평균 부적합률보다 높았고, carbendazim과 dinotefuran, etofenprox등의 검출빈도가 높았다.
호박의 국내 재배면적은 9,874 ha이며, 시설재배 호박의 면적은 3,060 ha로 과채류 중 수박 다음으로 재배면적이 높은 작물이다(KOSIS, 2020). 현재 국내에서 재배중인 호박은 늙은호박, 쥬키니 호박, 단호박, 애호박 등이 있으며, 이중 애호박(Cucurbita moschata Duchesne)은 영양학적으로 칼슘, 칼륨, 인 등의 무기질과 비타민 A가 다량 함유되어 있고, 소화흡수가 좋아 위장이 약하거나 당뇨, 비만 및 산후 부기를 저감 시키는 효과가 있어 가장 널리 재배되고 있다(Oh et al., 2010).
애호박은 4월 중순 파종한 후 6월 중순부터 10월 초순까지 재배하며, 주요발생 해충은 응애, 온실가루이, 총채벌레 등의 미소해충과 담배거세미나방, 파밤나방 등의 나방류와 호박과실파리 등이 알려져 있다(Park et al., 2016; Kim et al., 2020). 이들 해충 중 파밤나방의 방제에는 chlorantraniliprole, chromafenozide, cyantraniliprole, emamectin benzoate, flufenoxuron, lufenuron, metaflumizone, methoxyfenozide, spinetoram 등 9종이 등록되어 사용되고 있으나, 저항성발현 억제와 해충방제 효율을 높이기 위한 다양한 유효성분과 이들 성분의 혼합제에 대한 수요가 꾸준히 제기되고 있다(KCPA, 2020).
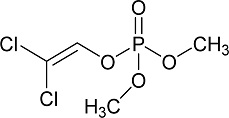
유기인계 농약인 dichlorvos는 1B 그룹에 속하는 acetylcholinesterase 저해제(IRAC, 2021)로 오이의 목화진딧물, 복숭아와 사과의 썩덩나무노린재, 배추와 파의 파밤나방, 고추의 담배나방, 배추의 배추좀나방 등의 해충방제에 등록되어 사용되고 있다(KCPA, 2020). Dichlorvos의 작물 잔류 반감기와 토양 잔류 반감기가 모두 4일 이내로 길지 않으며(Deivendran et al., 2006; Liang et al., 2012; IUPAC, 2021), 이는 dichlorvos의 높은 증기압(2.10 × 103mPa, 20oC)으로 인한 휘발손실이 주된 원인으로 알려져 있다(EPA, 2006). 특히, dichlorvos의 높은 증기압으로 인한 농작업자의 노출 위해성 증가가 문제되어 2011년 dichlorvos를 50%이상 함유하는 제형을 고독성 농약으로 분류하고, 등록취소 하였다. 이에 따라, 최근에는 λ-cyhalothrin과 emamectin benzoate, etofenprox, bifenthrin 등과 20%의 dichlorvos를 혼합한 제형으로 유통되고 있다(KCPA, 2020).
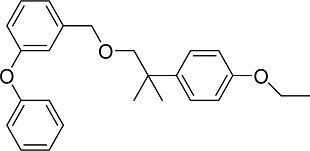
Etofenprox는 곤충신경계의 Na통로를 조절하여 살충효과를 나타내는 3A 그룹에 해당되는 pyrethroid계 살충제로(IRAC, 2021) 과채류의 복숭아혹진딧물, 꽃노랑총채벌레, 담배나방, 거세미나방, 파밤나방 등의 방제에 사용되고 있다(KCPA, 2020). 또한, etofenprox는 0.5-20%의 단제와 함께 dichlorvos와의 혼합제로도 유통되고 있다(KCPA, 2020). Etofenprox의 작물 잔류 반감기는 파에서 7.9-9.5일, 어수리에서 2.7-3.3일로 보고된 바 있으며(Hwang et al., 2015; An et al., 2019), 호박에서의 잔류연구는 부족한 상황이다.
호박에 대한 dichlorvos와 etofenprox의 MRL은 일본에서 각각 0.1mg kg-1과 1mg kg-1으로 설정되어 있으며, 유럽연합(European Union, EU)에서 각각 0.01mg kg-1로 설정되어 있다. 하지만, 우리나라는 dichlorvos와 etofenprox에 대한 호박의 MRL이 설정되어 있지 않으나, etofenprox에 대해서는 잠정 MRL인 0.2mg kg-1이 설정되어 있다(MFDS, 2020). 이에 따라, 본 연구에서는 애호박 시설재배지에서 20% dichlorvos와 10% etofenprox 혼합제 살포 후 이들의 경시적 잔류변화를 평가하고, 이들의 생물학적 반감기와 잔류위해성을 검토하였다.
재료 및 방법
표준품 및 시약
Dichlorvos와 etofenprox의 분석용 표준품은 Kemidas Co. (Suwon, Korea)에서 구입하여 사용하였고, 애호박에 대한 dichlorvos와 etofenprox의 잔류 시험은 20% dichlorvos와 10% etofenprox 혼합제인 유제(NongHyup Chemical Co., Ltd., Seongnam, Korea)를 사용하였으며, 시험대상 성분의 이화학적 특성은 Table 1과 같다.
시험에 사용한 용매인 acetonitrile (ACN)과 methanol, water는 Burdick & JacksonTM (Honeywell International Inc, Morris Plains, NJ, USA)의 high-performance liquid chromatography (HPLC) grade를 사용하였고, ammonium acetate (Sigma-Aldrich, Inc., St. Louis, MO, USA)와 formic acid (MerckKGaA, Darmstadt, Germany)는 순도 >98%를 사용하였다. 호박 중 dichlorvos의 추출에는 Phenomenex Inc. (Torrance, CA, USA)의 rOQTM QuEChERS kit(6 g, MgSO4 anhydrous, 1 g NaCl, 1 g sodium citrate tribasic dihydrate 및 0.5 g sodium citrate dibasic sesquihydrate)를 사용하였고, 추출시료의 정제를 위한 dispersive-solid phase extraction (d-SPE)는 Agilent Technologies, Inc. (Santa Clara, CA, USA)에서 구입한 EN method d-SPE kit (C18 25 mg, Primary secondary amine (PSA) 25 mg, MgSO4 150 mg)와 Supelclean ENVI-CarbTM (Supelco®, Sigma-Aldrich, Inc., Bellefonte, PA, USA)를 사용하였다. 호박 중 etofenprox의 추출에 사용한 Q-sep QuEChERS extraction kit (6 g MgSO4, 1.5 g NaOAc)는 Restek Co. (Bellefonte, PA, USA)에서 구매하여 사용하였고, 추출시료의 정제는 Agilent Technologies, Inc. (Santa Clara, CA, USA)의 AOAC method d-SPE kit (PSA 25 mg, MgSO4 150 mg)를 사용하였다.
시험포장 및 약제 처리
애호박의 잔류성 시험은 경남 진주시 대곡면 유곡리에 소재한 시설재배지에서 4월부터 5월까지 실시하였고, 품종은 진동애호박(Asia Seed Co., Seoul, Korea)을 사용하였다. 잔류포장시험의 대조구와 시험구는 각각 48m2 (1.6m× 30m)로 조성하여 시험구별 3반복 배치하였고, 시험구의 시험 약제 간 교차오염 방지를 위해 1.6m 이상의 완충구를 확보하였다. 시험 약제는 1,000배 희석하여 충전식 분무기를 이용하여 시험구 전체에 약액이 충분히 흐를 정도로 균일하게 살포하였으며, 약제는 수확 7일전과 수확당일에 총 2회 처리하였다(Table 2). 재배기간 동안 시설재배지의 평균온도는 19.8oC (5.3-37.9oC), 평균 상대습도는 78% (11-100%)이었다. 잔류분석을 위한 시료는 약제 살포 후 0일 (2시간후), 3일, 5일, 7일, 14일에 시료를 수확하였으며, 애호박 시료는 개당 500 g 이상인 시료를 처리구당 5 kg 이상 수확하였고, 애호박 잎 시료는 처리구당 1 kg 이상 수확하였다. 수확한 시료는 냉장상태로 실험실로 옮긴 후 드라이아이스와 함께 곱게 분쇄하고 잔류분석 전까지 -20oC서 보관하였다.
잔류분석 시료 전처리
애호박 열매와 잎 중 dichlorvos의 잔류분석을 위한 시료 전처리는 균질화 한 시료 10.0 g에 ACN 10mL를 가한 후 rOQTM QuEChERS kit를 첨가하여 30분간 진탕 추출하고, 20분간 초음파추출(Powersonic 410, Hwashin Tech Co., Ltd., Seoul, Korea) 하였다. 추출시료는 4oC, 4000 rpm에서 10분간 원심분리(LABOGENE 1580R, LabogenTM, Bio-Medical Science Co., Ltd., Seoul, Korea)하고, 상등액 1 mL를 취하여 EN method d-SPE kit와 ENVI-Carb 25 mg이 담긴 e-tube에 넣고 3분간 교반 후 syringe filter (0.22 μm, BIOFACT Co., Ltd, Daejeon, Korea)로 여과하여 잔류분석용 시료로 제조하였다. Etofenprox 잔류분석을 위한 시료 전처리는 균질화한 시료 10.0 g에 ACN 10mL를 가한 후 Q-sep QuEChERS extraction kit를 첨가하여 30분간 진탕 추출하고, 20분간 초음파 추출하였다. 추출시료는 4oC, 4000 rpm에서 10분간 원심분리하고, 상등액 1mL를 취하여 AOAC method d-SPE kit에 넣고 3분간 교반 후 syringe filter로 여과하여 잔류분석용 시료로 제조하였다.
기기분석 조건
잔류분석 전처리 시료의 dichlorvos 잔류분석은 LC-MS/MS (Agilent Technologies 6420 TripleQuad, Santa Clara, CA, USA)를 사용하여 Table 3의 조건에 따라 분석하였다. 이동상은 5 mM ammonium acetate를 포함한 0.1% formic acid 수용액과 5 mM ammonium acetate와 0.1% formic acid를 포함한 methanol을 gradient조건에서 사용하였고, ThermoFisher Scientific Inc. (Waltham, MA, USA)의 Acclaim RSLC 120 C18 (2.1 × 100 mm, 2.2 μm) 칼럼을 사용하여 분리하였다. Etofenprox 잔류분석은 Rtx5-MS (0.25 × 30 m, 0.25 μm, Resteck Co., Bellefonte, PA, USA) 칼럼으로 분리하여 Table 4의 분석조건에 따라 selected ion monitoring (SIM)의 방법으로 GC-MS (QP2020, Shimadzu Co., Kyoto, Japan)를 사용하여 분석하였다.
분석법 검증
Dichlorvos와 etofenprox의 검량선 작성을 위해 사용한 농약 표준품은 100mg L-1 stock solution을 제조한 후 무처리 애호박 열매와 잎 시료의 추출물을 사용하여 matrix-matched standard를 제조하였다. Dichlorvos와 etofenprox의 검량선은 각각 0.02-2.0 mg kg-1와 0.01-1.0 mg kg-1에서 작성하였다. Dichlorvos와 etofenprox의 정량한계(Limit of quantitation, LOQ)는 S/N비 10이상을 기준으로 산출하였고(Lee et al., 2015), 회수율 시험은 0.02 mg kg-1과 0.2mg kg-1에서 5반복 실시하였다.
생물학적 반감기 산출
생물학적 반감기 산출은 Kong et al. (2018) 등과 Hwang et al. (2019) 등이 사용한 방법에 따라 Eq. 1을 적용하여 회귀식을 산출하고, 반감기(t1/2)는 Eq. 2를 사용하여 산출하였다.
| (Eq. 1) |
| (Eq. 2) |
잔류 안전성 평가
Dichlorvos와 etofenprox의 잔류 안전성 평가는 검출된 최대 잔류량과 2018년 국민영양통계 중 전체 연령별 식이 섭취량 자료 및 체중을 고려하여 일일섭취추정량(Estimated Daily Intake, EDI)을 Eq. 3과 같이 산출하였다(KHIDI, 2018; Choi et al., 2021). 식품의약품안전처(Ministry of Food and Drug Safety, MFDS)의 잔류물질정보에 등록되어 있는 일일섭취허용량(Acceptable daily intake, ADI)과 EDI로 %ADI를 아래의 Eq. 4와 같이 산출하였다.
| (Eq. 3) |
| (Eq. 4) |
결과 및 고찰
분석법 검증
애호박 중 dichlorvos와 etofenprox의 잔류분석을 위한 검량선의 linearity (R2)는 모두 >0.999이었고, 애호박 열매와 잎에서의 LOQ는 dichlorvos의 경우 모두 0.02mg kg-1이었으며 etofenprox는 모두 0.01 mg kg-1이었다. Dichlorvos와 etofenprox의 회수율은 0.02 mg kg-1와 0.2mg kg-1에서 시험하였고, 그 결과 dichlorvos는 잎과 열매에서 98.0-112%이었으며, etofenprox는 93.9-102%이었다. 이들 정량분석에 대한 변이계수(Coefficient of variation, CV)는 1.2-10.9%이었다(Table 5).
애호박 중 dichlorvos의 경시적 잔류 변화
20% Dichlorvos와 10% etofenprox의 혼합제는 파밤나방 방제에 사용 시 1,000배 희석액을 배추와 파에서는 수확 7일전까지 2-3회이내 사용할 수 있도록 안전사용기준이 설정되어 있다(KCPA, 2020). 이에 따라, 본 연구에서는 20% dichlorvos와 10% etofenprox 혼합제 1,000배 희석액을 7일 간격 2회 살포 후 애호박의 열매와 잎에서 그 잔류량을 조사하였다. Dichlorvos의 약액 살포 당일 초기 잔류량은 열매에서 0.016-0.025 mg kg-1이었고, 잎에서 0.916-1.111 mg kg-1이었다. 약액 살포 당일을 제외한 모든 시료에서 dichlorvos는 LOQ 미만으로 불검출 되었다. 따라서, dichlorvos의 호박열매와 잎에서의 잔류 반감기는 3일이내로 추정되었다. 이는 Liang et al. (2012) 등이 과채류인 오이에서 보고한 초기 잔류량(0.027 mg kg-1)과 작물 잔류 반감기(3.48일)가 유사함을 확인할 수 있었다. 현재 dichlorvos에 대한 애호박열매와 잎에서의 MRL은 미설정 되어있으나, 약액 살포 3일차 이후 불검출 되므로 애호박의 잎과 열매에 대한 dichlorvos의 MRL은 PLS 일률기준인 0.01mg kg-1을 고려해볼 수 있을 것이다.
애호박 중 etofenprox의 경시적 잔류 변화
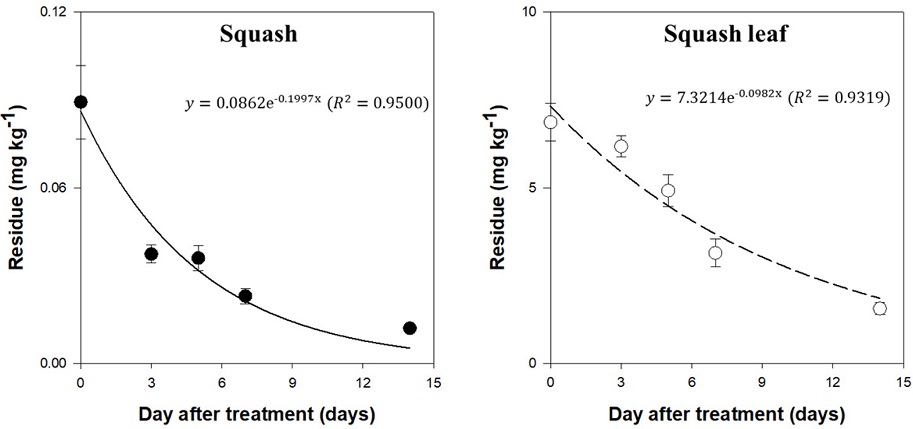
애호박 열매와 잎에서 약액 살포 당일 초기 잔류량은 각각 0.075-0.098 mg kg-1와 6.378-7.443 mg kg-1이었고, 최종 약제처리 14일 경과 후 etofenprox의 잔류량은 각각 0.011-0.013 mg kg-1와 1.412-1.742 mg kg-1로 감소함을 확인하였다(Table 6). Etofenprox에 대한 호박 열매의 생물학적 반감기는 각각 3.5일이었고(Fig. 1), 과채류인 토마토(2.15일)의 반감기와 유사하였다(Malhat et al., 2012). 또한, 호박 잎에서의 반감기는 7.1일로 엽경채류인 파(7.9일)와 유사하였고, 엽채류인 어수리(2.7-3.3일)와 배추(3.2일) 보다는 길었다(Lee et al., 2009; Hwang et al., 2015; An et al., 2019).
Etofenprox의 약액 살포 당일 초기 잔류량은 호박 열매에 대해 현재 설정된 잠정 MRL (0.2 mg kg-1)을 초과하지 않았다. 하지만, 호박 잎의 잔류량은 열매의 잔류량보다 약 80배 이상 높았으며, 이에 대한 MRL은 설정되어 있지 않다. 이에 따라, 호박 잎을 중심으로 식이 섭취량과 잔류량을 고려한 잔류위해평가가 필요하였다.
애호박에 대한 etofenprox의 잔류 위해성
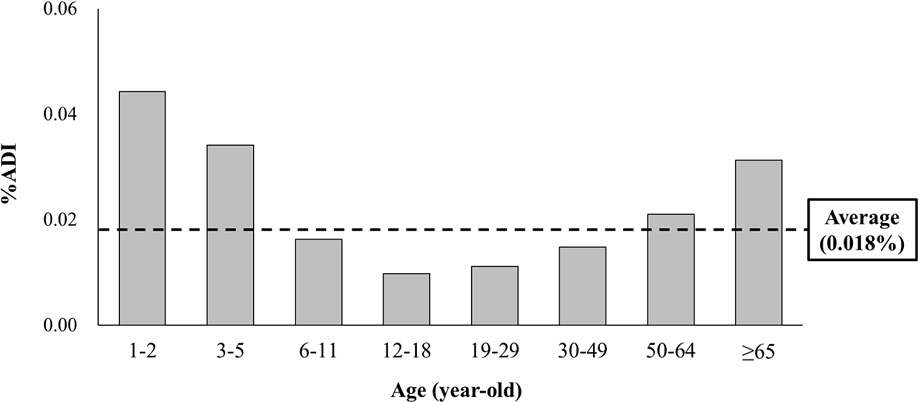
애호박 열매와 잎의 dichlorvos와 etofenprox의 잔류량과 식이 섭취량을 고려하여 20% dichlorvos와 10% etofenprox 유제 살포 후 잔류량에 따른 식이 섭취 위해평가를 실시하였다. Dichlorvos는 약액 살포 3일 후부터 잎과 열매에서 모두 불검출 되어 위해평가대상에서 제외하였고, etofenprox는 호박 열매의 경우 살포 당일 초기 잔류농도가 잠정 MRL 미만으로 확인된 바 있으나, 잎에서의 MRL은 설정되어 있지 않다. 따라서, dichlorvos와 etofenprox 혼합제 사용에 따른 잔류위해성은 dichlorvos 안전성이 확인된 약액 살포 후 3일차를 기준으로 호박 열매와 잎에서 etofenprox에 대해 평가하였다. 현재 전체 작물에 등록된 etofenprox의 이론적 일일 최대섭취량(Theoretical maximum daily intake, TMDI)은 0.014 mg kgbw-1 day-1로 ADI의 46.3% 였으며, 호박 열매에 설정된 잠정 MRL의 %ADI는 0.097%로 높지 않았다. 호박잎에 대한 MRL은 설정되어 있지 않으며, 이에 따라 약액 살포 3일차를 기준으로 산출한 EDI는 8.06 × 10-6mg kgbw-1 day-1이었으며, %ADI는 0.027%로 호박 잎과 열매의 섭취에 따른 위해성이 높지 않음을 확인할 수 있었다. 또한, 호박 열매 섭취량을 고려한 연령대별 위해평가 결과, 영유아(1-2세) 그룹에서 EDI가 1.33 × 10-5mg kgbw-1 day-1이었고, %ADI는 0.044%로 가장 높았으며, 청소년(12-18세) 그룹(0.010% ADI)에서 가장 낮았다. 연령에 따른 etofenprox의 %ADI는 U자형 그래프가 나타났다(Fig. 2). 이러한 결과의 원인을 분석해보면, 영유아 그룹과 어린이(6-11세) 그룹의 호박 열매의 일일 섭취량은 각각 4.27 g과 4.39 g으로 큰 차이가 없었으나, 평균 체중이 12.0 kg과 33.5 kg으로 약 3배 정도 영유아 그룹이 낮아 ADI기여도가 높게 나타남을 확인할 수 있었다. 또한, ADI기여도가 가장 낮은 청소년 그룹과 고령층(65세 이상, 0.031% ADI) 그룹의 평균 체중은 각각 59.7 kg과 60.6 kg으로 체중의 차이는 미미하였으나, 고령층 그룹의 식이 섭취량이 15.25 g으로 청소년 그룹(4.67 g) 보다 3.2배 높아 성인의 경우 etofenprox에 대한 ADI기여도는 식이 섭취량에 의존함을 확인할 수 있었다. 또한, 호박 잎의 경우에서도 식이 섭취량이 많은 고령층에서 ADI 기여도(0.068%)가 다른 연령층에 비해 높음을 확인하였다. 이에 따라, 영유아와 고령층에 대한 식이 섭취 위해성이 전체 연령 평균값 보다 높아 식이 섭취 위해평가 시 이들 연령층에 대한 면밀한 검토가 필요할 것이다.
Acknowledgments
본 연구는 농촌진흥청 공동연구과제사업(Project No. PJ01449602) 지원에 의해 수행되었습니다.
References
-
An JM, Shin SJ, Kim MG, Hwang HR, Chang SY, et al., 2019. Residual characteristics of etofenprox, pyrifluquinazon, spirotetramat and sulfoxaflor in cow parsnip (Heracleum moellendorffii L.) of minor crop. Korean J. Pestic. Sci. 23(2):61-69. (In Korean)
[https://doi.org/10.7585/kjps.2019.23.2.61]

-
Choi GH, Lee DY, Ryu SH, Ro JH, Park BJ, et al., 2018. Investigation of the bioconcentration factor of endosulfan for rice from soil. Korean J. Pestic. Sci. 22(1):25-28. (In Korean)
[https://doi.org/10.7585/kjps.2018.22.1.25]

-
Choi GH, Lee DY, Bruce-Vanderpuije P, Song AR, Lee HS, et al., 2021. Environmental and dietary exposure of perfluorooctanoic acid and perfluorooctanesulfonic acid in the Nakdong river, Korea. Environ. Geochem. Health. 43:347-360.
[https://doi.org/10.1007/s10653-020-00721-0]

-
Deivendran A, Kumari B, Yadav GS, 2006. Dissipation of endosulfan and dichlorvos residues in/on cauliflower curds. Environ. Monit. Assess. 116:307-313.
[https://doi.org/10.1007/s10661-006-7394-y]

-
Hwang KW, Bang WS, Jo HW, Moon JK, 2015. Dissipation and removal of the etofenprox residue during processing in spring onion. J. Agric. Food. Chem. 63:6675-6680. (In Korean)
[https://doi.org/10.1021/acs.jafc.5b02345]

-
Hwang KW, Kim HJ, Sun JH, Jeong KS, Lee TH, et al., 2019. Establishment of pre-harvest residue limit (PHRL) of buprofezin and pyridaben in squash. Korean J. Pestic. Sci. 23(3):154-161. (In Korean)
[https://doi.org/10.7585/kjps.2019.23.3.154]

- Insecticide Resistance Action Committee (IRAC), 2021. The IRAC mode of action classification online. https://irac-online.org/modes-of-action/, (Accessed Feb. 16. 2021).
- International Union of Pure and Applied Chemistry (IUPAC), 2021. IUPAC Pesticide Properties DataBase. http://sitem.herts.ac.uk/aeru/iupac/atoz.htm, (Accessed Feb. 16. 2021).
-
Jeong DK, Jeong WM, Goo YM, Kil YS, Sin SM, et al., 2020. Study on residual characteristics of mandipropamid and metalaxyl-M in Cnidium officinale Makino. Korean J. Pestic. Sci. 24(2):172-179. (In Korean)
[https://doi.org/10.7585/kjps.2020.24.2.172]

-
Kim JH, Choi MK, Moon HC, Chon HG, 2020. Occurrence of major diseases in pesticide-free cultivated tomato and cucurbit in Jeollabuk-do, South Korea. Korean J. Environ. Biol. 38(3):486-495. (In Korean)
[https://doi.org/10.11626/KJEB.2020.38.3.486]

-
Kong SH, Lee DY, Song YH, Park KH, Seo WD, et al., 2018. Residue safety on ethephon in soybean leaf by drenching and foliar application. J. Appl. Biol. Chem. 61(1):75-78.
[https://doi.org/10.3839/jabc.2018.011]

- Korea Crop Protection Association (KCPA), 2020. Agrochemical use guide book. https://www.koreacpa.org/ko/use-book/, (Accessed Feb. 10. 2021). (In Korean)
- Korea Health Industry Development Institute (KHIDI), 2018. Korea National Health & Nutrition Examination Survey. https://www.khidi.or.kr/kps/dhraStat/result2?menuId=MENU01653&year=2018, (Accessed Feb. 10. 2021). (In Korean)
- Korea Rural Economic Institute (KREI), 2019. The consumer behavior survey for food 2019. Naju, Republic of Korea, pp. 683-694. (In Korean)
- Korean Statistical Information Service (KOSIS), 2020. Vegetable Production (Fruit Vegetables). https://kosis.kr/statHtml/statHtml.do?orgId=101&tblId=DT_1ET0027, (Accessed Feb. 10. 2021). (In Korean)
-
Lee DY, Jeong DK, Choi GH, Lee DY, Kang KY, et al., 2015. Residual characteristics of bistrifluron and fluopicolide in Korean cabbage for establishing pre-harvest residue limit. Korean J. Pestic. Sci. 19(4):361-369. (In Korean)
[https://doi.org/10.7585/kjps.2015.19.4.361]

- Lee EY, No HH, Park YS, Kang KW, Kim JK, et al., 2009. Residual characteristics of etofenprox and methoxyfenozide in Chinese cabbage. Korean J. Pestic. Sci. 13(1):13-20. (In Korean)
-
Lee SY, Paik MK, Kim NS, Park ES, Son EH, et al., 2019. A survey on pesticide use by farmers for positive list system settlement. Korean J. Pestic. Sci. 23(4):358-370. (In Korean)
[https://doi.org/10.7585/kjps.2019.23.4.358]

-
Liang Y, Wang W, Shen Y, Liu Y, Liu XJ, 2012. Dynamics and residues of chlorpyrifos and dichlorvos in cucumber grown in greenhouse. Food Control. 26(2):231-234.
[https://doi.org/10.1016/j.foodcont.2012.01.029]

-
Malhat F, Abdallah H, Nasr I, 2012. Estimation of etofenprox residues in tomato fruits by QuEChERS methodology and HPLC-DAD. Bull. Environ. Contam. Toxicol. 88:891-893.
[https://doi.org/10.1007/s00128-012-0627-6]

- Ministry of Food and Drug Safety (MFDS), 2020. Pesticide and veterinary Drugs Information. https://www.foodsafetykorea.go.kr/residue/main.do, (Accessed Dec. 15. 2020). (In Korean)
- National Agricultural Products Quality Management Service (NAQS), 2017. 2016 Annual report for quality management of agricultural products. Gimcheon, Republic of Korea, p. 19-22. (In Korean)
-
Oh CK, Kim MC, Oh MC, Yang TS, Hyun JS, et al., 2010. Antioxidant activities in enzymatic hydrolysates of pumpkin powder (Cucurbita spp.). J. Korean Soc. Food Sci. Nutr. 39(2):172-178. (In Korean)
[https://doi.org/10.3746/jkfn.2010.39.2.172]

-
Oh KY, Choi GH, Bae JY, Lee DY, Lee SW, et al., 2020. Effect of soil organic matter content on plant uptake factor of ginseng for endosulfan. J. Appl. Biol. Chem. 63(4):401-406.
[https://doi.org/10.3839/jabc.2020.052]

- Park BK, Jung SH, Kwon SH, Ye EY, Lee HJ, et al., 2020. Monitoring and risk assessment of pesticide residues on stalk and stem vegetables marketed in Incheon metropolitan area. J. Food Hyg. Saf. 35(4):365-374.
-
Park KS, Kim YT, Kim HS, Lee JH, Lee HI, et al., 2016. Bacterial spot disease of green pumpkin by Pesudomonas syringae pv. syringae. Res. Plant Dis. 22(3):158-167.
[https://doi.org/10.5423/RPD.2016.22.3.158]

- United States Environmental Protection Agency (EPA), 2006. Interim reregistration eligibility decision for dichlorvos (DDVP). Washington D.C. USA, p. 120-157.
Kyeong-Yeol Oh, Department of Agricultural Chemistry, Institute of Agriculture and Life Science (IALS), Gyeongsang National University, Ph.D. student, https://orcid.org/0000-0002-1699-4164
Ji-Yeon Bae, Department of Agricultural Chemistry, Institute of Agriculture and Life Science (IALS), Gyeongsang National University, Master, http://orcid.org/0000-0003-4872-9143
Deuk-Yeong Lee, Department of Agricultural Chemistry, Institute of Agriculture and Life Science (IALS), Gyeongsang National University, Ph.D. student, http://orcid.org/0000-0001-6047-5276
Yeong-Jin Kim, Department of Agricultural Chemistry, Gyeongsang National University, Ph.D. student; Environmental Chemistry Research Group, Korea Institute of Toxicology, Researcher, https://orcid.org/0000-0002-3926-9387
Dong-Yeol Lee, Anti-Aging Research Group, Gyeongnam Oriental Anti-Aging Institute, Researcher, https://orcid.org/0000-0003-1192-1932
Jin-Hyo Kim, Department of Agricultural Chemistry, Institute of Agriculture and Life Science (IALS), Gyeongsang National University, Professor, https://orcid.org/0000-0002-0341-7085