
미생물 제제의 범용 적용을 위한 후보 미생물의 다병원균 길항 활성 및 생장촉진 기능 평가
초록
본 연구의 목적은 화학비료 기반 재배체계에 적용 가능한 후보 미생물 7종을 선발하여, 비료에 의한 생육 촉진 효과를 보완·증폭하고 동시에 미생물 길항작용을 통한 병해 저감 가능성을 제시하는 데 있다. 항균활성 평가에서 토마토시들음병균은 1/5 PDK에서 H2, 1/5 TSA에서 H1 처리구의 억제 길이가 가장 길었고, 토마토탄저병균은 H2·R5가 두 배지에서 공통적으로 높은 억제 효과를 보였다. 고추역병균은 1/5 TSA에서 H1에서만 억제가 확인되었으며, 고추·벼 주요 병원균 전반에서 H2, H4, R5가 비교적 안정적인 항균활성을 나타냈다. 생장촉진 형질 평가에서 H3는 IAA 생성이 가장 높았고, siderophore는 H3를 제외한 균주에서 확인되었으며 특히 H4, R5가 우수하였다. 질소 고정은 유의성이 없었으나 R7은 단백질 분해 및 biofilm 형성이 높고, H2는 셀룰로스 분해와 biofilm 형성이 우수하였다. 이상의 결과는 H2, H4, R5, R7 균주가 화학비료와 병행 투입되는 기능성 미생물로서 근권 정착 및 복합기작 (항균·철 경쟁·효소활성·biofilm)을 통해 비료 유래 생육향상과 병 발생 억제를 동시 달성할 잠재력이 있음을 시사하며, 지속가능 농업을 위한 미생물-비료 복합제 개발의 기초자료로 활용될 수 있다.
Abstract
The purpose of our study was to select candidate microbial strains as functional additives for fertilizer-based cropping systems by demonstrating their potential to both enhance plant growth and mitigate disease through microbial antagonism. We assessed the major pathogen-antagonistic and plant growth-promoting characteristics of seven isolates in tomato, pepper, and rice plants. In tomato wilt, the largest inhibition zone was associated with strain H2 grown on 1/5 Potato Dextrose Peptone (PDK) medium, whereas maximum inhibition was observed with strain H1 on 1/5 Tryptic Soy Agar (TSA) medium. In tomato anthracnose, we observed consistently strong inhibition with H2 and R5 in both media. In pepper, only H1 on 1/5 TSA suppressed Phytophthora blight. Strains H2, H4, R5 exhibited stable growth in their antagonism against pepper and rice pathogens, indicating comparatively stable activity. Regarding growth-promoting features, all the strains produced indole-3-acetic acid (IAA), with H3 producing the highest level. Other than H3, all the strains produced siderophore. The largest halo zones were recorded for H4 and R5. Although nitrogen fixation was not statistically significant, several strains showed notable enzymatic and colonization traits. R7 displayed high protease activity and strong biofilm formation, while H2 exhibited the highest cellulase activity and robust biofilm formation. Our combined results suggest that H2, H4, and R5 (and, in part, R7) are promising candidates to develop as fertilizer-compatible microbial additives that can both improve crop vigor and reduce disease pressure through multiple mechanisms (antibiosis, iron competition, extracellular enzymes, and rhizosphere colonization). Our research provides the groundwork to design integrated microbial fertilizer products to support enhanced sustainable crop production.
Keywords:
Antifungal activity, Colonization, Plant growth-promoting키워드:
항진균 활성, 정착력, 식물 생장 촉진서 론
현대 농업체계에서 안정적인 수량 확보를 위해 화학비료와 화학농약 투입이 증가해 왔으나, 화학재 의존은 토양 생물 다양성 저하, 환경부하, 그리고 병해의 만성적 재발이라는 한계를 동반한다. 특히 시비는 작물 생육을 직접 촉진하지만, 근권·토양 병원균의 압력을 근본적으로 낮추지는 못하며, 오히려 비료 성분과 염류농도 변화가 근권 미생물 군집과 병 발생 양상을 교란하여 “생육 촉진과 병해 관리”를 분리해 접근할 경우 작물 재배 현장에의 효율이 제한될 수 있다. 이러한 배경으로, 최근에는 비료의 공급 기능에 유용미생물의 생물자극(biostimulation) 및 생물방제(biocontrol) 기능을 결합한 “미생물-비료 복합제” 개념이 주목받고 있다. 비료 사용 체계에 추가되는 형태의 미생물 제제는 농업인 관점에서 적용 장벽이 낮고, 동일 시비 과정에서 양분 이용효율 향상과 병해 저감 효과의 동시 달성을 지향할 수 있다(Calvo et al., 2014; du Jardin, 2015; Backer et al., 2018). 또한 PGPR(plant growth-promoting rhizobacteria)과 같은 유용미생물 기반 제제는 지속가능 농업 투입재로서 상용화가 확대되고 있으나, 제형·운송·저장 안정성과 현장 재현성 확보가 여전히 핵심 과제로 남아 있다(Santos et al., 2019; Fadiji et al., 2024).
유용미생물이 작물 생육을 촉진하는 기작은 크게 양분관련 기작과 병해억제 기작으로 구분된다. 양분관련 기작으로는 식물호르몬(특히 IAA) 생산, 양분 가용화 및 흡수 촉진, 철 획득 경쟁(siderophore 생산) 등이 대표적이며(Vessey, 2003; Bhattacharyya and Jha, 2012; Spaepen and Vanderleyden, 2011), 병해억제 기작으로는 항생물질·휘발성 물질·세포벽 분해효소 생산, 공간 경쟁, 그리고 유도저항성(induced resistance) 유발을 통한 병원균 억제가 포함된다(Compant et al., 2005; Haas and Defago, 2005; Ongena and Jacques, 2008). 예로, IAA는 뿌리 분지와 근모 발달을 촉진하여 양분과 수분 흡수 기반을 확장할 수 있으며(Patten and Glick, 2002; Spaepen and Vanderleyden, 2011), siderophore는 철 제한 조건에서 병원균과의 경쟁 우위를 제공함으로써 병 억제에 기여할 수 있다(Haas and Defago, 2005). 이러한 다기능성은 미생물-비료 복합제 설계에서 중요한 근거가 된다. 즉, 비료가 제공하는 양분 기반 위에서 유용미생물이 근권 정착과 생장촉진을 유도하고, 동시에 병원균의 초기 정착·확산을 저해하는 방향으로 작동한다면, 화학비료 투입 효율을 높이면서 병해 부담을 낮추는 통합적 관리가 가능해진다(Glick, 2012; Backer et al., 2018).
그러나 유용미생물 기반 제품의 현장 성과는 실험실 수준의 항균성이나 단일 생장촉진 지표만으로 충분히 예측되기 어렵다. 토양, 작물, 기상 등의 조건에 따른 생존력, 근권 정착성, 토착 미생물과의 경쟁 작용, 그리고 제형의 보조제에 의해 효능이 크게 달라지기 때문이다(Malusá et al., 2012; Santos et al., 2019; Fadiji et al., 2024). 특히 유용미생물의 표면 부착 및 생물막(biofilm) 형성은 근권에서의 지속적 정착과 기능 발현(양분 흡수, 병원균 억제, 신호물질)에 밀접히 연결되며(Ramey et al., 2004; Bogino et al., 2013), 제형 관점에서는 저장 중 생존율과 시비 조건(염류, pH, 수분)에서의 생리적 안정성이 제품 품질의 핵심 변수가 된다(Malusá et al., 2012; Fadiji et al., 2024). 따라서 미생물-비료 복합제 개발을 위해서는 (i) 다양한 병원균에 대한 길항 스펙트럼, (ii) 생장촉진 관련 형질(IAA, siderophore 등), (iii) 정착성 지표(biofilm 등), (iv) 영양 조건 변화에 대한 항균성 재현성까지 포괄하는 다면적 평가가 요구된다(Compant et al., 2005; Backer et al., 2018).
본 연구는 최종적으로 비료에 혼입 또는 동시 처리 가능한 “미생물-비료 복합제” 후보 균주를 도출하기 위한 기초 자료를 제공하고자 수행되었다. 이를 위해 서로 다른 영양 조건을 갖는 배지에서 다양한 작물 병원균을 대상으로 길항활성을 평가하고, 동시에 IAA 생성, siderophore 생성, 인산 가용화, 질소고정 관련 반응, 단백질 및 셀룰로스 분해능, amylase 활성, biofilm 형성 등 생장촉진 및 정착 관련 형질을 체계적으로 조사하였다(Vessey, 2003; Spaepen and Vanderleyden, 2011; Malusá et al., 2012). 이러한 접근은 “병해 저감형 미생물제” 또는 “생육촉진형 미생물제”를 분리하여 개발하는 방식에서 한 단계 나아가, 화학비료의 생육촉진 효과를 보완 및 증폭하면서 미생물의 병 억제 기능을 동시에 구현할 수 있는 복합제 설계의 과학적 근거를 축적하는 데 목적이 있다(du Jardin, 2015; Backer et al., 2018; Fadiji et al., 2024). 나아가, 본 연구에서 제시하는 복합 기능 미생물 선발 절차는 미생물 복합제의 제품화 과정에서 요구되는 효능 재현성 및 적용 편의성 확보에 기여할 것으로 기대된다(Santos et al., 2019).
재료 및 방법
평가 대상 미생물 균주의 동정
본 연구에서 평가된 균주는 총 7 가지로 모두 선행 연구에서 농업적 기능이 확인되어 지식재산권이 확보되어 있는 균주들이다. 기업과의 비밀유지 계약에 의해 원 균주명을 공개하지 않으며, 본 연구에서는 각 균주명을 H1, H2, H3, H4, R5, R6, R7으로 명명하여 수행하였다. 균주의 동정은 16S rRNA 유전자 염기서열 분석을 통하여 속(Genus)수준에서 수행하였다.
진균성 식물병원균에 대한 in vitro 항균 활성 평가
토마토시들음병(Fusarium oxysporum f. sp. lycopersici, KACC 40037), 토마토탄저병(Colletotrichum coccodes, KACC 40802), 고추역병(Phytophthora capsici, KACC 40481), 고추탄저병(Colletotrichum gloeosporioides, KACC 40690), 벼잎집무늬마름병(Rhizoctonia solani, KACC 40101), 벼도열병(Magnaporthe oryzae, KACC 46551) 병원균이 길항미생물의 항균 활성 평가에 사용되었다. 본 연구에서 사용된 병원균은 국립농업과학원 농업미생물은행(KACC)에서 분양받아 사용하였으며, 벼도열병균은 생물작용제로 보유, 제조 신고 후 사용하였으며, 실험 종료 후 폐기신고를 완료하였다.
진균성 병원균에 대한 후보 미생물의 항균 활성 평가를 위해 petri dish에서 대치배양 방법을 사용하였다. 삼각플라스크에 1/5 PDK agar(Potato Dextrose Peptone Agar; 2 g potato dextrose broth, 2 g peptone, 20 g agar per L), 1/5 TSA(Tryptic Soy Agar; 6 g tryptic soy broth, 20 g agar per L) 배지를 고온(120oC, 15분) 멸균 후 90 mm petri dish에 25 ml씩 분주하여 굳힌 후 멸균된 8mm paper disk를 치상하였다. Paper disk에 각 후보 미생물 현탁액을 1 × 108 cfu/ml 농도로 20 µl씩 처리하고 28oC 항온기에서 생육하였다. 미생물이 생장한 것을 확인한 후 paper disk와 병원균 agar block 각각의 중심부 30 mm 위치에 대상 병원균 3 mm agar block을 치상하여 처리구당 4반복 실험을 진행하였다. 28oC 항온기에 보관 후 무처리구의 균사가 petri dish 전체 표면에 자라면 균사의 생장이 억제된 부분의 길이를 측정하였다.
후보 미생물의 진균성 병원균 억제 결과 값은 Kruskal-Wallis Rank Sum Test로 유의성 분석을 진행하였으며, 후보 미생물 간의 차이를 확인하기 위해 Conover Test 분석을 통해 처리구간의 유의한 차이를 그룹으로 표시하였다. R program (version 4.0.3)의 ggplot2 package를 사용하여 분석 및 시각화를 수행하였다.
평가 대상 미생물 균주의 작물 생장 촉진 효능 평가
식물 호르몬(Indole Acetic Acid, IAA) 생성능을 평가하기 위해 15 ml conical tube(SPL)에 멸균된 1/5 TSB(tryptic soy broth), 0.1%의 tryptophane이 첨가된 1/5 TSB 배지를 5 ml씩 담고 후보 미생물을 접종한 후 28℃ 항온기에서 14일간 배양하였다. 원심분리(4,000rpm, 10분) 후 상층액 1 ml과 Salkowski’s reagent(35% HCLO4 50 ml, 0.5M FeCl3 1 ml) 2 ml을 유리 test tube에 혼합한 다음 30분간 실온에 보관 후 분홍색으로 발색 되는 정도를 OD530 nm에서 측정하여 비교하였다.
철이온흡착력(siderophore 생성능)을 확인하기 위해 chrome azurole S (CAS) blue agar plate assay 방법을 이용하였다. CAS 평판 배지 중앙에 멸균된 8 mm paper disk를 올린 후 각 미생물을 1 × 108 cfu/ml 농도로 20 µl씩 접종 후 28oC 항온기에 14일간 보관하고 orange halo zone 형성을 확인하였다.
인산 가용화 능력을 알아보기 위하여 0.5% calcium phosphate (10CaO·3P2O5·H2O)가 첨가된 Pikovskaya′s agar 배지를 이용하였다. 배지 중앙에 멸균된 8 mm paper disk를 올린 후 각 미생물을 1 × 108 cfu/ml 농도로 20 µl씩 접종 후 28oC 항온기에 14일간 보관하고 clean zone 형성을 확인하였다
질소 고정능 검사를 위해 NFB 배지를 test tube에 5 ml 분주한 후 각 미생물을 108 cfu/ml 농도로 10 µl씩 접종한 후 28oC 항온기에 7일간 보관하였다. 이후 배지색상의 변화로 질소 고정능 유무를 확인하였다.
단백질 분해능을 알아보기 위하여 skim milk agar(10 g skim milk powder, 18 g agar per L) 배지를 이용하였다. 배지 중앙에 멸균된 8 mm paper disk를 올린 후 각 미생물을 108 cfu/ml 농도로 20 µl씩 접종 후 28oC 항온기에 3일간 보관하고 clean zone 형성을 확인하였다.
셀룰로오스 분해능은 cellulose agar(10 g carboxylmethyl cellulose, 1 g yeast extract, 0.05 g MnSO4, 4 g KH2PO4, 1 g MgSO4·7H2O, 2 g CaCl2, 0.05 g FeSO4, 2 g NH4Cl, 18 g agar per L))를 사용하였다. 배지 중앙에 멸균된 8 mm paper disk를 올린 후 각 미생물을 108 cfu/ml 농도로 20 µl씩 접종 후 28oC 항온기에 5일간 보관하였다. 5일 후 0.1% Congo red로 염색한 후 1M NaCl로 두 번 세척하고 4oC 냉장고에 24시간 보관 후 clean zone 형성을 확인하였다.
키틴 분해능을 알아보기 위하여 minimal media에 정제된 키틴을 첨가한 배지를 만들어 배지 중앙에 멸균된 8 mm paper disk를 올린 후 각 미생물을 108 cfu/ml 농도로 20 µl씩 접종 후 28oC 항온기에 5일간 배양하였다. 5일 후 0.1% Congo red로 염색한 후 1M NaCl로 두 번 세척하고 4oC 냉장고에 24시간 보관 후 clean zone 형성을 확인하였다.
아밀라제 활성 검정을 위하여 Bennet agar(10 g glucose, 1 g yeast extract, 2 g bacto-peptone, 1 g beef extract, 15 g agar per L) 배지에 0.2% soluble starch를 첨가한 배지를 사용하였다. 배지 중앙에 멸균된 8mm paper disk를 올린 후 각 미생물을 108 cfu/ml 농도로 20 µl씩 접종 후 28oC 항온기에 3일간 배양하였다. 10% Lugol’s solution을 이용하여 염색한 후 clean zone 형성을 관찰하였다.
후보 미생물이 외부 환경으로부터 보호하고 정착에 도움을 주는 생물막(biofilm) 형성에 대해 알아보기 위해 MM [(10.5 g K2HPO4, 4.5 g KH2PO4, 1 g (NH4)2SO4, 0.5 g Na3C6 H5O7·2H2O, 0.2 g MgSO4 7H2O, 5 g dextrose, 16g agar/L)] media를 사용하여 실험을 진행하였다.
결과 및 고찰
평가 대상 미생물 균주의 동정
본 연구에서 사용된 7개의 균주는 16S rRNA 유전자 염기서열 분석결과 Bacillus 6종, 그리고 Streptomyces 1종으로 재확인되었다(Table 1). H1균주는 Streptomyces bacillaris, H2, Bacillus amyloliquefaciens; H3는 Bacillus aryabhattai; H4, Bacillus velenzeinsis; R5는 Bacillus velezensis, R6번 균주는 Bacillus velenzeinsis로, R7은 Bacillus velezensis로 확인되었다.
진균성 식물병원균에 대한 in vitro 항균 활성 평가
토마토시들음병에 대한 항균활성 평가 결과 1/5 PDK 배지에서는 H2 균주 처리구에서 억제된 부분의 길이가 가장 길었으며, 1/5 TSA 배지에서는 H1 균주 처리구에서 토마토 시들음병균의 억제된 길이가 가장 길었다(Fig. 1A). 배지 종류에 따라 우점 균주가 달라진 것은 항균물질의 생산 또는 확산이 영양 조건(탄소원/질소원 조성)에 의해 크게 좌우됨을 시사한다. 특히 H2(1/5 PDK)와 H1(1/5 TSA)의 차이는 균주별 대사 전략이 상이함을 보여, 적용 환경(근권 영양상태)에 따른 균주 선택이 필요하다. 토마토탄저병에 대한 항균 활성 평가 결과 1/5 PDK 배지에서는 H2, H4, R5 균주 처리구에, 1/5 TSA 배지에서는 H2, R5, R7 균주 처리구에서 토마토 탄저병원균 억제된 길이가 가장 길었다(Fig. 1B). H2와 R5가 두 배지 모두에서 상위 억제 효과를 보인 점은 배지 의존성이 비교적 낮은 ‘안정적 항균활성’ 균주일 가능성을 뒷받침한다. 반면 H4와 R7의 반응 차이는 특정 영양 조건에서만 항균 관련 대사가 강화될 수 있음을 의미한다.
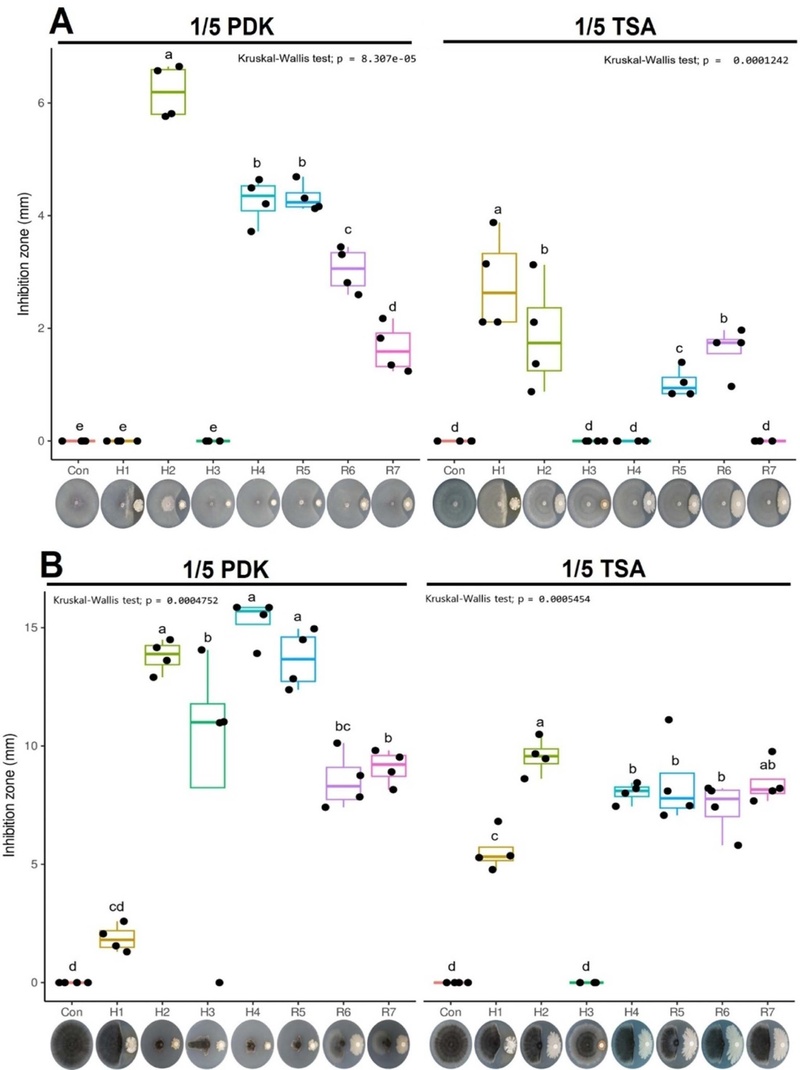
Antifungal activity of candidate microbes against tomato pathogens: (A) Fusarium oxysporum f. sp. lycopersici and (B) Colletotrichum coccodes. Microbial suspensions (1 × 108 CFU mL−1; 20 μL) were applied to paper discs and incubated at 28°C. A 3-mm pathogen agar plug was placed 30 mm from the disc (n = 4), and inhibition length was measured at full growth of the control. Data were analyzed by the Kruskal–Wallis test.
고추역병에 대한 항균활성 평가 결과 1/5 PDK 배지에서는 H1, H4, R5 균주 처리구에서 억제된 길이가 길었으며, 1/5 TSA 배지에서는 H1 균주 처리구에서만 고추 역병균 억제되었다(Fig. 2A). 1/5 TSA에서 억제가 H1에서만 확인된 결과는 역병균에 대한 길항이 특정 균주가 보유한 표적 특이적 메커니즘에 의해 주도될 가능성을 시사한다. 또한 TSA 조건에서 다른 균주들의 억제가 소실된 점은 배지 조성에 따라 길항형질 발현이 억제될 수 있음을 보여준다. 고추탄저병에 대한 항균활성 평가 결과 1/5 PDK 배지에서는 H2, H4, R5 균주 처리구에서 억제된 길이가 길었고, 1/5 TSA 배지에서는 H4, R5, R7 균주의 처리구에서 고추 탄저병원균의 억제된 길이가 가장 길었다(Fig. 2B). 두 배지에서 반복적으로 상위권에 위치한 H4와 R5 균주는 고추 탄저병원균에 대해 비교적 재현성 높은 억제력을 갖는 후보로 해석될 수 있다. 특히 배지에 따라 상위 조합이 달라진 점은 ‘균주–병원균–환경’ 상호작용을 고려한 선발 전략의 타당성을 시사한다.
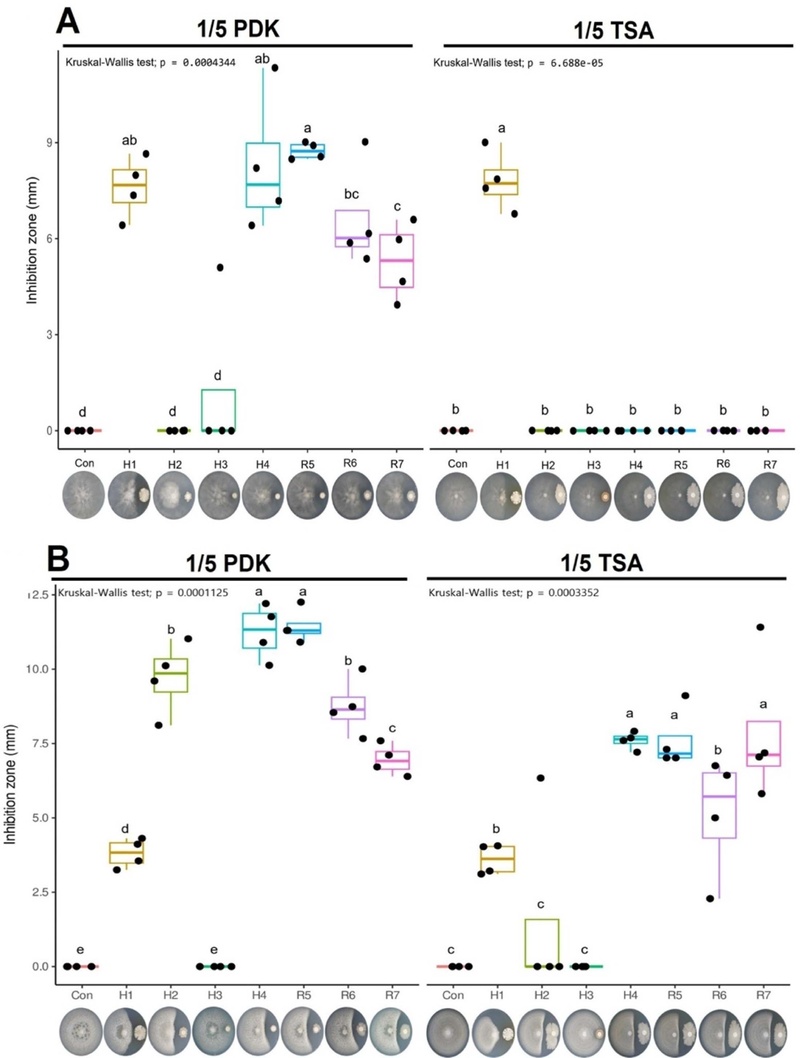
Antifungal activity of candidate microbes against pepper pathogens: (A) Phytophthora capsici and (B) Colletotrichum gloeosporioides. Microbial suspensions (1 × 108 CFU mL−1; 20 μL) were applied to paper discs and incubated at 28°C. A 3-mm pathogen agar plug was placed 30 mm from the disc (n = 4), and inhibition length was measured when the control fully colonized the plate. Data were analyzed by the Kruskal–Wallis test.
벼잎집무늬마름병에 대한 항균활성 평가 결과 1/5 PDK 배지에서는 H2, H4, R5 균주 처리구에서 억제된 길이가 길었으며, 1/5 TSA 배지에서는 H2 균주 처리구에서 억제된 길이가 가장 길었다(Fig. 3A). H2가 두 조건에서 모두 유의한 억제를 보인 것은 대상병원균에 대하여 안정적인 길항 잠재력을 가질 수 있음을 시사한다. 반면 TSA에서 H2가 단독으로 두드러진 결과는 특정 배지 조건에서 H2의 항균형질 발현이 상대적으로 강화될 가능성을 보여준다. 벼도열병에 대한 항균활성 평가 결과 1/5 PDK 배지에서는 H2, H4, R5 균주 처리구에서 억제된 길이가 길게 확인되었으며, 1/5 TSA 배지에서는 H2, H4, R5 균주 처리구에서 억제된 길이가 길게 확인되었다(Fig. 3B). 도열병균에 대해 H2, H4, R5가 두 배지 모두에서 상위 억제 양상을 보인 점은 해당 균주들이 비교적 다양한 항균 레퍼토리를 보유했을 가능성을 시사한다. 이는 향후 포장 조건에서도 안정적 성능을 기대할 수 있는 후보군으로서 우선 검증 가치가 높다.
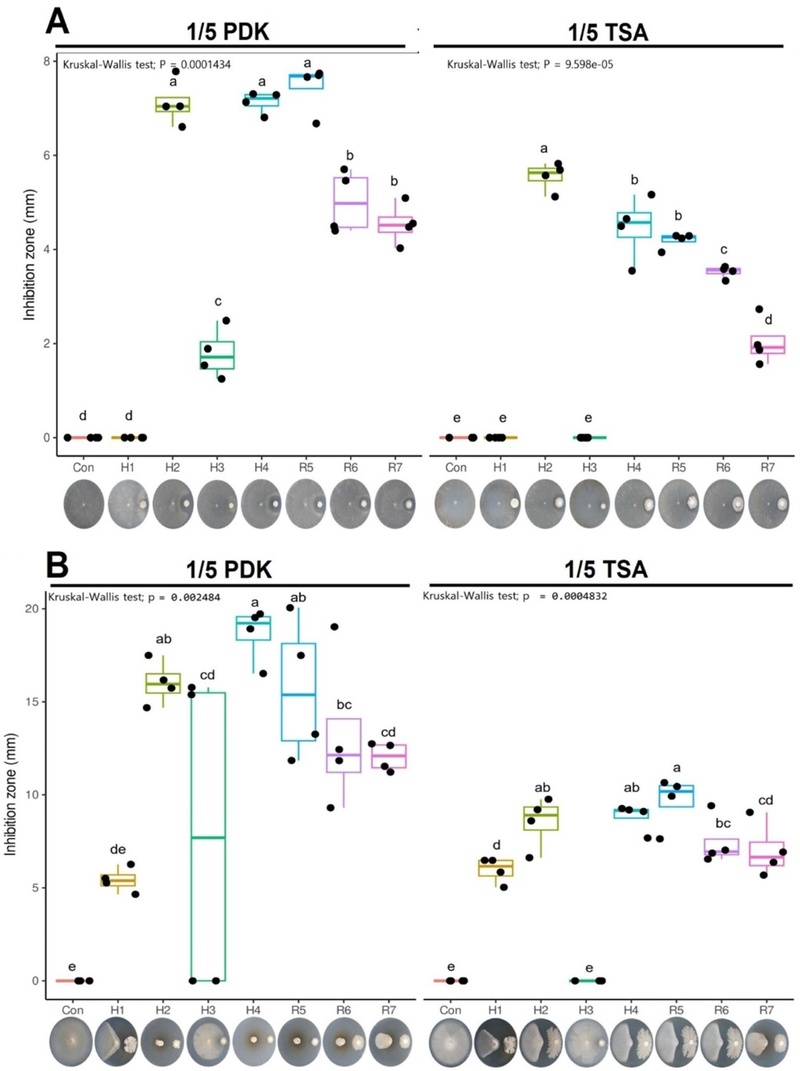
Antifungal activity of candidate microbes against rice pathogens: (A) Rhizoctonia solani and (B) Magnaporthe oryzae. Microbial suspensions (1 × 108 CFU mL−1; 20 μL) were applied to paper discs and incubated at 28°C. A 3-mm pathogen agar plug was placed 30 mm from the disc (n = 4), and inhibition length was measured when the control fully colonized the plate. Data were analyzed by the Kruskal–Wallis test.
작물 생장촉진 효능 평가
후보 미생물 모두 IAA 생성능을 가지고 있는 것을 확인할 수 있었으며 분홍색으로 확연한 차이를 보인 H3 균주의 OD530 nm 측정 수치가 0.0972로 가장 높아 IAA 생성능력이 가장 좋은 것을 확인하였다(Fig. 4A). IAA 생성은 뿌리 생장 및 측근 발달 촉진과 연계될 수 있어 H3는 생장촉진 측면에서 우수 후보로 평가된다. 다만 과도한 IAA는 조건에 따라 생육 불균형을 유발할 수 있으므로, 실제 식물 수준에서 최적 농도/효과 검증이 필요하다.
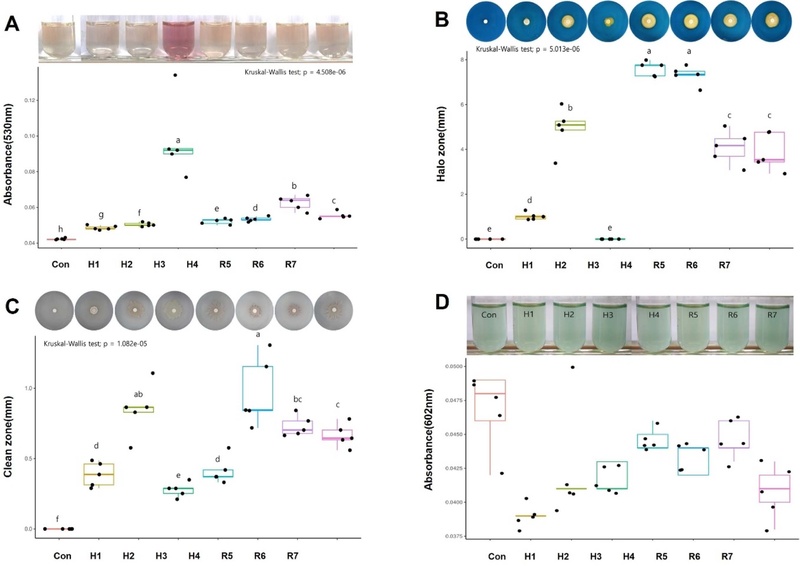
Assays for plant growth–promoting traits of candidate microbes. (A) Indole-3-acetic acid (IAA) production was determined after 14 d at 28°C in 1/5 TSB with/without 0.1% tryptophan using Salkowski’s reagent and measuring absorbance at 530 nm. (B) Siderophore production was assessed on CAS blue agar by the formation of an orange halo zone after 14 d at 28°C. (C) Phosphate solubilization was evaluated on Pikovskaya’s agar containing 0.5% calcium phosphate by measuring clear-zone formation after 14 d at 28°C. (D) Nitrogen fixation was tested in NFB broth (7 d at 28°C) based on color change of the medium.
철이온흡착력(siderophore)을 확인 한 결과 H3 균주를 제외한 모든 균주에서 siderophore 생성능이 확인되었으며, H4, R5 균주의 orange halo zone이 각각 7.6, 7.3 mm로 유의미한 차이를 보였다(Fig. 4B). Siderophore 생성은 근권에서 철 경쟁을 통해 병원균 생장을 간접 억제하는 주요 기작으로 알려져, H4와 R5의 높은 halo는 생물학적 방제 잠재력과 연결될 수 있다. 특히 H3에서 siderophore가 확인되지 않은 점은 생장촉진(IAA)과 길항(철 경쟁) 형질이 균주별로 분리되어 나타날 수 있음을 보여준다.
인산 가용화능은 모든 균주에서 확인되었지만 clean zone의 길이 1 mm 미만으로 낮게 확인되었고 이중 R5 균주가 유의미한 차이를 보였다(Fig. 4C). 인산 가용화능이 전반적으로 낮게 나타난 것은 해당 후보군의 주요 생장촉진 기작이 인산 가용화보다는 다른 형질(IAA, biofilm, 효소활성 등)에 의해 좌우될 가능성을 시사한다. 그럼에도 R5의 상대적 우수성은 복합 기작형 후보로서의 장점을 추가로 제공한다.
질소고정 평가 시약을 육안상으로 확인했을 때 배지색상이 미세한 차이를 보였으나 OD602 nm에서 측정한 결과 통계적으로 유의미한 차이가 없어 질소 고정능을 가진 미생물은 없는 것으로 확인되었다(Fig. 4D). 질소고정이 확인되지 않은 결과는 생장촉진 효과가 질소 공급보다는 근권 정착성 또는 영양·호르몬 조절 기능에 기인할 가능성이 높다는 것을 나타낸다. 또한 육안 판독과 정량값의 불일치는 정량 기반 판정의 중요성을 뒷받침한다.
단백질 분해능은 모든 균주에서 확인되었으며, R7 균주가 clean zone 12.6 mm로 가장 높았다. H4, R5, R6 균주는 R7 균주와 통계적으로 유의미한 차이는 있었으나 clean zone 평균이 각각 12.3, 12.0, 11.9 mm로 높게 확인되었다(Fig. 5A). 단백질 분해효소는 병원균 구조 단백질 또는 감염 관련 단백질을 저해할 수 있어, H4, R5, R6, R7의 높은 활성은 직접 길항 기작의 한 축으로 작동할 여지가 있다. 특히 R7은 효소 기반 억제력 관점에서 우선 후보 균주로로 고려될 수 있다.
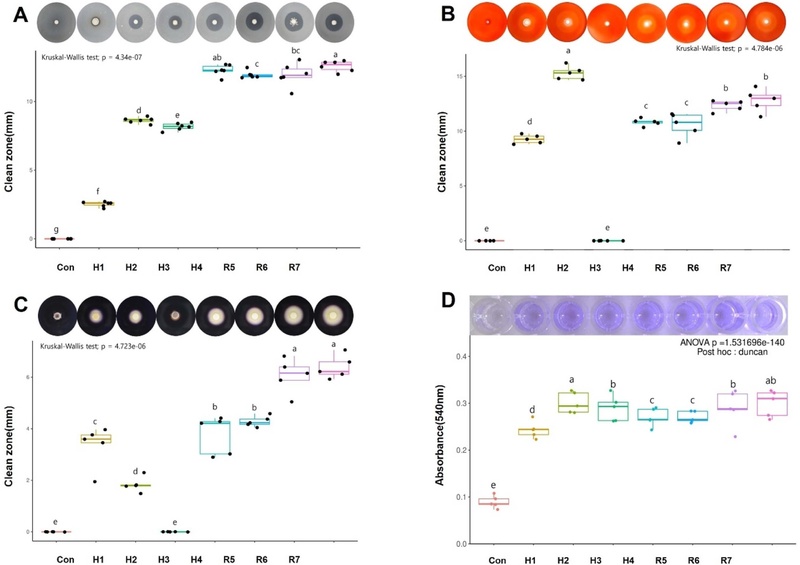
Assays for extracellular enzyme activities and biofilm formation of candidate microbes. (A) Protease activity was evaluated on skim milk agar by measuring clear-zone formation after 3 d at 28°C. (B) Cellulase activity was assessed on cellulose agar; plates were incubated for 5 d at 28°C, stained with 0.1% Congo red, washed with 1 M NaCl, and clear zones were recorded after 24 h at 4°C. (C) Amylase activity was determined on Bennett agar supplemented with 0.2% soluble starch; after 3 d at 28°C, plates were stained with Lugol’s solution and clear zones were measured. (D) Biofilm formation was assessed using MM medium under incubation at 28°C.
후보 미생물의 셀룰로오스 분해능은 H3 균주를 제외한 모든 균주에서 확인되었으며, 이중 H2 균주가 clean zone 15.3 mm로 가장 높았다(Fig. 5B). 셀룰라아제 활성은 유기물 분해를 통한 근권 적응성 향상 및 경쟁력 강화에 기여할 수 있어, H2의 높은 활성은 정착성과 지속성 측면에서 강점이 될 수 있다. 반면 H3는 ‘호르몬(IAA) 중심’의 생장촉진형 균주일 가능성을 시사한다.
후보 미생물 7종 모두 키틴 분해능은 확인되지 않았다(data not shown). 키틴분해능 부재는 항균활성이 주로 키틴분해효소 기반이 아니라 다른 대사산물(항생물질, 휘발성물질 등)이나 경쟁 기작(철 경쟁, biofilm 등)에 의해 나타날 가능성을 시사한다. 따라서 길항 메커니즘 규명을 위해 추가적인 대사체/휘발성 물질 분석이 유용할 수 있다.
후보 미생물의 아밀라제 활성은 H3 균주를 제외한 모든 균주에서 확인되었으며, R6, R7 균주의 clean zone 길이가 각각 6.0, 6.2 mm로 가장 높았다(Fig. 5C). 아밀라제 활성은 탄수화물 이용성 확대를 통해 근권 경쟁력 및 정착성을 높일 수 있어, R6, R7의 우수성은 생태적 적응 측면에서 의미가 있다. H3에서 활성이 낮은 점은 H3의 기능적 프로파일이 다른 균주들과 뚜렷이 구분됨을 다시 확인시킨다.
후보 미생물 모두 biofilm 형성이 확인되었고 H2, R7 균주의 biofilm 형성이 가장 높은 것으로 확인되었다(Fig. 5D). Biofilm 형성은 뿌리 표면 부착 및 근권 정착과 직결되므로, H2와 R7은 실제 재배 환경에서 안정적 군집 형성 및 지속 효과를 기대할 수 있는 후보로 평가된다. 특히 항균활성(H2) 또는 효소활성(R7)과 결합될 경우 현장 적용성이 더 높아질 수 있다.
Acknowledgments
이 연구는 2026년도 경상국립대학교 연구년제 연구교수 연구지원비에 의하여 수행되었습니다.
이해상충관계
저자는 이해상충관계가 없음을 선언합니다.
REFERENCES
-
Backer R, Rokem JS, Ilangumaran G, Lamont J, Praslickova D, et al., 2018. Plant growth-promoting rhizobacteria: context, mechanisms of action, and roadmap to commercialization of biostimulants for sustainable agriculture. Front. Plant Sci. 9:1473.
[https://doi.org/10.3389/fpls.2018.01473]

-
Bhattacharyya PN, Jha DK, 2012. Plant growth-promoting rhizobacteria (PGPR): emergence in agriculture. World J. Microbiol. Biotechnol. 28(4):1327-1350.
[https://doi.org/10.1007/s11274-011-0979-9]

-
Bogino PC, Oliva Mde la M, Sorroche FG, Giordano W, 2013. The role of bacterial biofilms and surface components in plant-bacterial associations. Int. J. Mol. Sci. 14(8):15838-15859.
[https://doi.org/10.3390/ijms140815838]

-
Calvo P, Nelson L, Kloepper JW, 2014. Agricultural uses of plant biostimulants. Plant Soil 383(1-2):3-41.
[https://doi.org/10.1007/s11104-014-2131-8]

-
Compant S, Duffy B, Nowak J, Clément C, Ait Barka EA, 2005. Use of plant growth-promoting bacteria for biocontrol of plant diseases: principles, mechanisms of action, and future prospects. Appl. Environ. Microbiol. 71(9):4951-4959.
[https://doi.org/10.1128/AEM.71.9.4951-4959.2005]

-
du Jardin P, 2015. Plant biostimulants: definition, concept, main categories and regulation. Sci. Hortic. 196:3-14.
[https://doi.org/10.1016/j.scienta.2015.09.021]

-
Fadiji AE, Xiong C, Egidi E, Singh BK, 2024. Formulation challenges associated with microbial biofertilizers in sustainable agriculture and paths forward. J. Sustain. Agric. Environ. 3(3):e70006.
[https://doi.org/10.1002/sae2.70006]

-
Glick BR, 2012. Plant growth-promoting bacteria: mechanisms and applications. Scientifica (Cairo). 2012:963401.
[https://doi.org/10.6064/2012/963401]

-
Haas D, Defago G, 2005. Biological control of soil-borne pathogens by fluorescent pseudomonads. Nat. Rev. Microbiol. 3(4):307-319.
[https://doi.org/10.1038/nrmicro1129]

-
Malusá E, Sas-Paszt L, Ciesielska J, 2012. Technologies for beneficial microorganisms inocula used as biofertilizers. Sci. World J. 2012:491206.
[https://doi.org/10.1100/2012/491206]

-
Ongena M, Jacques P, 2008. Bacillus lipopeptides: versatile weapons for plant disease biocontrol. Trends Microbiol. 16(3):115-125.
[https://doi.org/10.1016/j.tim.2007.12.009]

-
Patten CL, Glick BR, 2002. Role of Pseudomonas putida indoleacetic acid in development of the host plant root system. Appl. Environ. Microbiol. 68(8):3795-3801.
[https://doi.org/10.1128/AEM.68.8.3795-3801.2002]

-
Ramey BE, Koutsoudis M, von Bodman SB, Fuqua C, 2004. Biofilm formation in plant-microbe associations. Curr. Opin. Microbiol. 7(6):602-609.
[https://doi.org/10.1016/j.mib.2004.10.014]

-
Santos MS, Nogueira MA, Hungria M, 2019. Microbial inoculants: reviewing the past, discussing the present and previewing an outstanding future for the use of beneficial bacteria in agriculture. AMB Express 9(1):205.
[https://doi.org/10.1186/s13568-019-0932-0]

-
Spaepen S, Vanderleyden J, 2011. Auxin and plant-microbe interactions. Cold Spring Harb. Perspect. Biol. 3(4):a001438.
[https://doi.org/10.1101/cshperspect.a001438]

-
Vessey JK, 2003. Plant growth promoting rhizobacteria as biofertilizers. Plant Soil 255(2):571-586.
[https://doi.org/10.1023/A:1026037216893]

Gun Young Han: Gyeongsang National University, Researcher, ORCID http://orcid.org/0009-0005-7511-6336.
Young A Oh: Namhae Chemical Corp., General Manager
Dong Ryul Lee: Namhae Chemical Corp., Researcher
Changsoon Kang: Namhae Chemical Corp., Director
Yong Bok Lee: Gyeongsang National University, Professor
Youn-Sig Kwak: Gyeongsang National University, Professor, ORCID http://orcid.org/0000-0003-2139-1808.
Research design: Kwak Y, Kang C, Investigation: Han GY, Oh YA, Lee DR, Data analysis: Han GY, Lee YB, Writing: Kwak Y, Kang C.

