무궁화에서 월동한 목화진딧물 개체군의 농자재에 대한 약효와 살충제 저항성 돌연변이 발생 빈도 추정
 ; Eun Young Yang2 ; Yul Kyun Ahn2 ; Sora Kim1, 3, 4
; Eun Young Yang2 ; Yul Kyun Ahn2 ; Sora Kim1, 3, 4 ; Deok Ho Kwon2, *
; Deok Ho Kwon2, *
초록
무궁화에서 월동한 목화진딧물 7개 개체군을 대상으로 농자재 30종에 대한 약효 평가를 수행하였다. 화학합성살충제 작용기작 1, 3, 4, 28번 그룹에 포함되는 17종과 유기농업자재 7종의 처리구에서 평균적으로 약 60% 이상의 약효가 있음을 확인하였다. GJ 개체군은 17종의 농자재에 대해 28.2%(6.7~46.7%)의 사충율을 나타내어 약효 저항성을 지닌 것으로 확인되었다. 16개 야외 개체군에서 화학합성살충제 저항성 관련 돌연변이 비율을 측정한 결과, S431F(86.8%) > A302S(33.8%) > M918L(26.3%) > R81T(3.8%) > L1014F(1.6%) 순서로 나타나, 월동 후 약제 저항성 돌연변이가 유전될 수 있음을 확인하였다. 본 연구 결과는 무궁화 식재지 증가에 따른 목화진딧물의 밀도 조절에 중요한 관리 정보를 제공할 것이다.
Abstract
The efficacy of 30 agrochemicals was evaluated against seven overwintered field populations of the cotton aphid, Aphis gossypii, collected frosm Hibiscus syriacus. Seventeen synthetic pesticides (IRAC groups 1, 3, 4, and 28) and seven organic materials showed mean mortalities exceeding 60%. In contrast, the GJ population showed markedly reduced susceptibility, with an average mortality of 28.2% (6.7−46.7%) across 17 tested agrochemicals, indicating the presence of strong insecticide resistance. To investigate the genetic basis of insecticide resistance, the frequencies of resistance–associated mutations were analyzed in 16 field populations. The detected mutation frequencies followed the order S431F (86.8%) > A302S (33.8%) > M918L (26.3%) > R81T (3.8%) > L1014F (1.6%), suggesting that resistance-related mutations can be maintained and transmitted after overwintering. Taken together, these findings provide critical information for the effective management of cotton aphid populations in response to the increasing planting of H. syriacus and highlight the necessity of resistance-informed insecticide selection for sustainable aphid control.
Keywords:
Cotton aphid, Hibiscus syriacus, Organic agricultural materials, Point mutation, Synthetic pesticides키워드:
목화진딧물, 무궁화, 화학합성살충제, 유기농업자재, 점돌연변이서 론
목화진딧물(Aphis gossypii Glover)은 전 세계적으로 분포하는 대표적인 흡즙성 해충으로, 채소류, 과수류, 화훼작물 등 다양한 농작물에 피해를 유발한다(Ebert and Cartwright, 1997). 특히, 짧은 세대기간과 단위생식을 통한 빠른 개체군 증가 특성을 지니며, 흡즙에 의한 피해뿐 아니라 여러 식물 바이러스의 매개체로서 생산성 저하의 주요 원인으로 알려져 있다(Jayasinghe et al., 2022). 또한, 감로 분비로 인한 그을음병을 유발하여 기주 식물의 광합성을 억제시키고 열매를 오염시켜 상품성을 저하시키는 주요 관리 대상 해충이다(Agrios, 1988).
목화진딧물의 기주 이용과 생활사를 살펴보면 서식지의 환경에 따라 연중 무성생식만 지속하는 무환형(anholocyclic type)과 유성생식과 무성생식을 교대로 하는 유환형(holocyclic type)으로 구분된다. 유환형은 계절에 따라 기주를 교대하는 이기주유환형(heteroecious holocyclic type)과 동기주유환형(autoecious holocyclic type)으로 세분화된다. 무환형은 환경이 따뜻한 지역에서 나타나고, 유환형은 일본, 중국 그리고 한국 등 계절이 구분된 환경에서 발견된다(Paik et al., 1974; Inaizumi, 1980; Slosser et al., 1989; Chen et al., 1990). 국내에서 나타나는 목화진딧물은 이기주유환형에 포함되며, 1차 기주에서 4월 중순 경에 부화 및 증식한 후 다양한 2차 기주(고추, 오이, 수박, 멜론 재배지 및 육묘)로 분산된 후 서식하다가, 10월 경에 다시 1차 기주로 돌아와 유성생식을 통해 산란한다(Paik et al., 1974). 무궁화는 대표적인 1차 기주로, 목화진딧물의 주요 월동 산란처이다(Shim et al., 1979).
한편, 국내에서는 2016년 ‘산림자원의 조성 및 관리에 관한 법률’에 근거하여 무궁화의 체계적인 보급 및 관리를 위해 무궁화진흥계획을 수립하여 시행하고 있다(Republic of Korea, 2016). 이로 인해 무궁화가 많은 지역의 가로수나 공원에 식재되어 일반인의 무궁화에 대한 친밀도를 향상시키는 노력을 하고 있다(KFS, 2021; KFS, 2026). 목화진딧물의 대표 1차 기주인 무궁화의 식재 면적 증대는 목화진딧물 밀도 증가에 영향을 줄 수 있다. 또한, 4월 중순에서 5월 하순까지 가로수나 공원에 식재된 무궁화 신초에 대량 증식한 목화진딧물은 감로를 분비하여 그을음병을 유발시켜 무궁화에 대한 친밀도를 떨어뜨리는 주요 원인이 될 수 있다. 뿐만 아니라, 증식한 목화진딧물이 농작물을 포함한 2차 기주로 이동할 경우, 직접적인 흡즙, 감로로 인한 그을음병 유발, 그리고 식물 병원성 바이러스 전파로 경제적 피해를 유발할 수 있다.. 따라서 무궁화에 발생하는 목화진딧물을 효과적으로 관리할 수 있는 방제 체계 수립이 필요하다.
목화진딧물의 방제는 물리적, 생물학적, 화학적 방제법들이 구축되어 있으나(Kinley et al., 2021), 일반적으로 화학적 방제법이 주로 적용된다. 하지만, 목화진딧물의 짧은 세대기간으로 인해 이미 다양한 작용기작을 지닌 화학합성살충제(유기인계, 피레스로이드계, 네오니코티노이드계)에 대해 저항성이 빠르게 발달된 것으로 보고되어 있다(Bass et al., 2015; Feyereisen et al., 2015; Wang et al., 2021). 분자생물학적 측면에서 유기인계와 카바메이트계 약제 작용점인 acetylcholinesterase type-1(AChE1) 상에 A208S와 S431F 돌연변이가 약제 민감도에 반응하는 것으로 보고되었다(Toda et al., 2008) 피레스로이드계 약제 작용점인 voltage-gated sodium channel(VGSC) 상에서는 L1014F와 M918L 돌연변이가 약제 감수성을 저하시키는 것으로 보고되었으며(Pires Paula et al., 2021), 네오니코티노이드계 약제에서는 R81T돌연변이가 nicotinic acetylcholine receptor(nAChR) 상에 약효 감소에 영향을 주는 것으로 보고되었다(Hirata et al., 2017). 목화진딧물의 효과적인 방제를 위해 대상 개체군의 약제 저항성을 고려한 약제 선택이 요구된다. 따라서, 무궁화에 발생한 목화진딧물 방제 시 불특정 다수의 일반인에 대한 노출 안전성과 농업인의 경제성이 고려되어야 한다. 본 연구는 무궁화에서 월동 후 발생한 목화진딧물을 대상으로 화학합성살충제와 유기농업자재에 대해 선제적으로 약효 스크리닝을 수행하여, 무궁화 식재 면적 증가에 따른 목화진딧물의 밀도 증가에 의한 부작용을 사전 관리하기 위해 수행하였다. 또한 분자생물학적 측면에서 월동 무궁화 개체군의 살충제 저항성 관련 돌연변이 보유 여부도 기초 연구로서 조사하였다.
재료 및 방법
국내 무궁화에서 월동한 목화진딧물 개체군의 채집
본 실험에 사용한 목화진딧물은 13개 시·군에서 채집한 16개 개체군으로, 월동 후 무궁화 신초에서 증식 중인 개체들을 대상으로 채집하였다(Table 1). 채집 시 각 개체군은 대상 구역 내 서로 다른 최소 3개체의 무궁화 신초에서 서식하는 개체들을 채집하여 하나의 집단(pool)으로 구성하였다. 16개 개체군의 암컷 성충은 채집 후 분자생물학적 종 동정과 약제 저항성 돌연변이 진단을 위한 gDNA 추출을 위하여 100% 에탄올에 침지 후 -20oC에 보관하였다. 그 중 7개 개체군(GJ, BE, SJ1, WJ1, WJ3, JJ, SJ2)은 채집 후 즉시 약효 평가에 사용되었다.
생물검정
화학합성살충제 22종과 유기농업자재 8종으로 야외에서 채집한 7개 개체군에 대한 약효 평가를 수행하였다(Table 2). 생물검정은 선행 연구에서 수행한 엽침지법을 변형하여, 무궁화 잎을 사용하여 수행하였다(Kim et al., 2023). 무궁화의 엽절편(Ø 46 mm)을 각 약제 별 제조사의 추천농도 희석액에 10초간 침지하고 흄 후드(실험실용배기기, 동재산업)에서 30분간 음건하였다. 침지한 엽절편은 1% agarose gel 5 mL를 넣어 굳힌 breeding dish (Ø 50 mm, SPL)에 치상하고, 무시충 목화진딧물 15마리를 3반복으로 접종하였다. 24시간 후 관찰 시, 세필붓(1.2 mm, 1호, 화홍)으로 자극하였을 때 충체 길이만큼 움직이지 않으면 사충수에 포함하여 사충율을 계산하였다.
종 동정 및 약제 저항성 돌연변이 분석
채집한 16개 개체군 별 무시충 목화진딧물 10마리를 대상으로 HigeneTM Genomic DNA prep kit (BIOFACT, Daejeon, Korea)를 사용하여 제조사의 매뉴얼에 따라 genomic DNA를 추출하였다. 대상 시료를 추출 버퍼와 proteinase K를 넣고 65oC에서 10분간 열처리한 후, gDNA binding column에 gDNA를 분리한 후 elution buffer를 넣어 최종 추출 후 표적 유전자 증폭에 사용하였다. 유전자 증폭은 총 35 µL 반응액에 DNA template 5 µL, 프라이머 1 µL(5 pmole/µL)(Table 3), 10 mM dNTP, 그리고 0.4 µL의 AmpONETM Taq DNA Polymerase (Geneall, Korea)를 첨가하였다. 반응 조건은 초기 95oC/2 min과 95oC/20 s + 60oC/20 s + 72oC/1 min에서 35회 수행한 후 72oC/5 min으로 진행하였다. 1% agarose gel 전기 영동을 통하여 유전자 증폭을 확인한 후, 증폭 산물을 마크로젠(MACROGEN, Seoul, Korea)에 의뢰하여 염기서열 분석을 진행하였다. 형질빈도는 Chromas (Technelysium Pty Ltd, Australia)를 이용하여 염기에 해당하는 시그널의 상대적인 비를 토대로 추정하였다.
통계분석 및 시각화
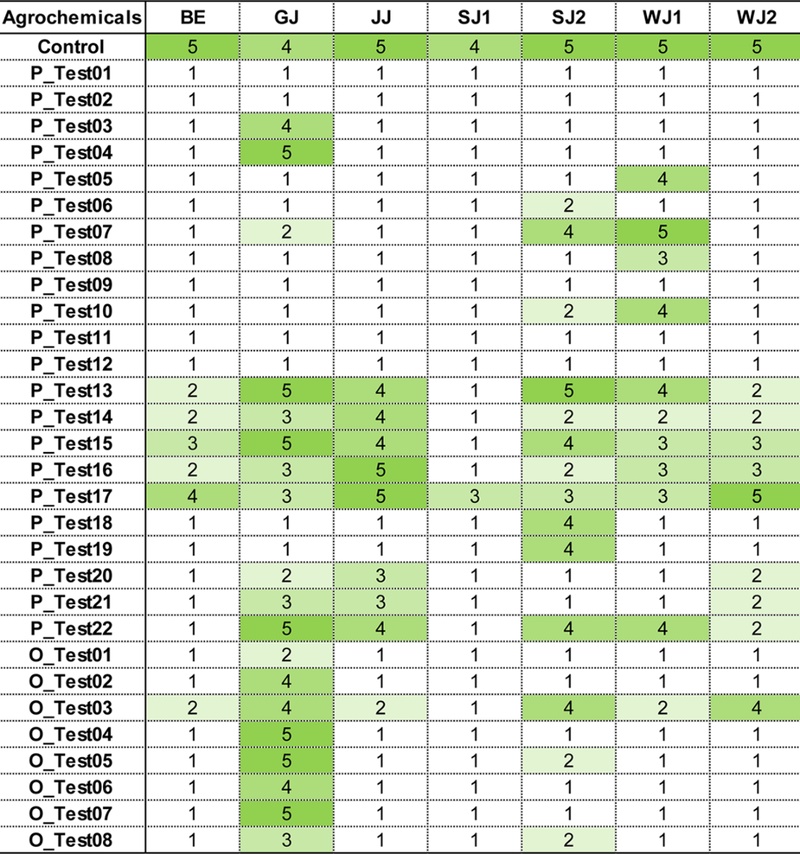
본 연구의 통계분석은 R software를 활용하였다(R core team, 2025). 약제 별 사충율 비교 및 화학합성살충제와 유기농업자재에 대한 개체군 별 약효 비교에 일원분산분석을 진행하였고, 사후 검정은 R 내 multcomp 패키지의 glht 함수를 이용하여 Tukey’s HSD test를 실시하였다. 작용기작 별 사충율 비교에는 반복수가 일정하지 않으므로 비모수통계분석법인 Kruskal-Wallis test(Krustal and Wallis, 1952)를 수행한 후 Dunn’s multiple comparisons test(Dunn, 1961)를 적용하여 분석하였다. 유의성 차이의 표시는 cld 함수를 이용하여 알파벳 소문자로 표시하였다. 개체군 별 약효 등급 시각화는 5단계(1단계, 81−100%; 2단계, 61−80%; 3단계, 41−60%; 4단계, 21−40%; 5단계, 0−20%)로 구분하였다.
결 과
무궁화에서 월동한 진딧물의 종 동정
16개 지역의 무궁화에서 월동한 진딧물을 채집하여, 각 개체군 별 10마리의 DNA를 추출한 후 분자생물학적 종 동정을 수행하였다. 그 결과, 모든 개체군이 99.8%−100%의 일치도로 목화진딧물(Aphis gossypii)(Acc. number: MT430940.1)로 나타났다(Table 4).
농자재에 대한 약효 평가 결과
무궁화에서 월동한 목화진딧물 7개 개체군을 대상으로 화학합성살충제 22종과 유기농업자재 8종에 대한 약효를 평가하였다(Figs. 1, 2, 3). 개체군 별 무처리구 사충율은 평균 15.1%였으며, 약제 처리구의 사충율은 4.5%−100%로 서로 다르게 나타났다(F30,626= 17.994, P < 0.001)(Fig. 1). 화학합성살충제와 유기농업자재 중 17종과 7종의 약제가 약 60%이상의 사충율을 보였다. 특히, 화학합성살충제 중에서 작용기작 표시기호를 기준으로 1, 3, 4, 28번 그룹에 포함되는 약제들이 약 60% 이상의 약효를 나타내었다(P < 0.0001) (Fig. 2).
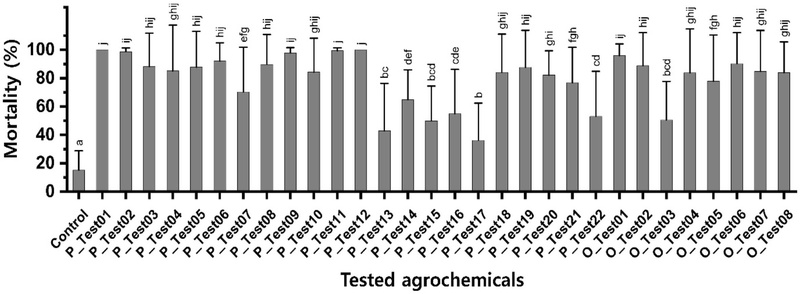
Average mortality at 24 h of 7 Aphis gossypii populations against 22 synthetic pesticides and 8 organic agricultural materials. Error bars indicate the standard deviations and the same letters are not significantly different by Tukey’s HSD.
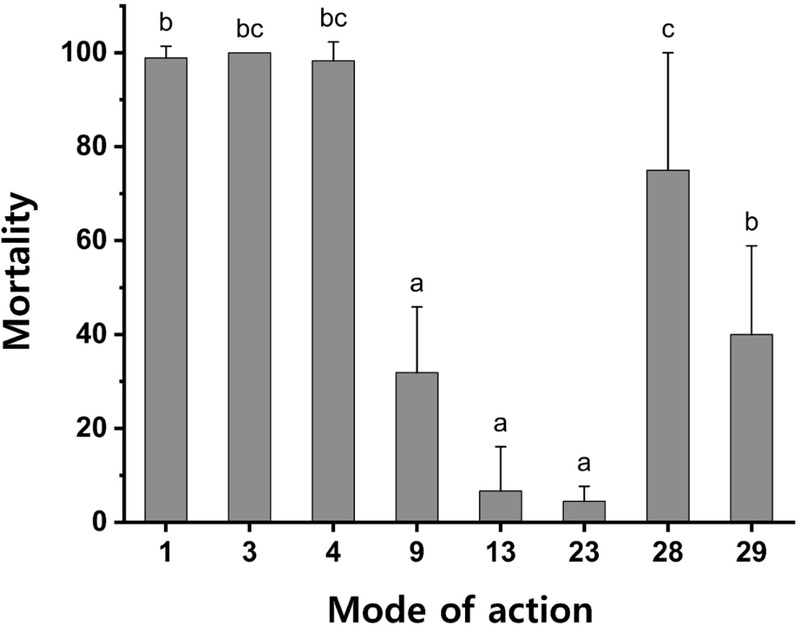
Comparisons of average mortality by mode of action in seven Aphis gossypii populations (BE, GJ, JJ, SJ1, SJ2, WJ1, WJ3). Error bars indicate the standard deviations. Small alphabetical characters represent the statistical significance (P < 0.05) determined by multiple comparison analysis based on Dunn’s method in Kruskal-Wallis test.
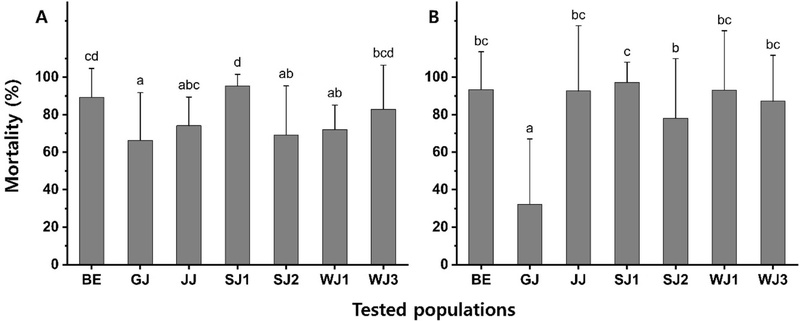
Comparisons of average mortality in seven Aphis gossypii populations (BE, GJ, JJ, SJ1, SJ2, WJ1, WJ3) against synthetic pesticides (A) and organic agricultural materials (B). Letters above error bars indicating the standard deviations mean the statistical difference by Tukey’s HSD.
야외 개체군 별로 살펴보면, 화학합성살충제에 대해서는 GJ와 SJ2에서 평균 66.3%와 69.2%의 사충율을 보였고(F6,455 = 9.718, P < 0.001)(Fig. 3A), 특히, 유기농업자재에서는 GJ가 32.2%의 평균 사충율을 나타내었다(F6,161 = 32.553, P < 0.001)(Fig. 3B). GJ는 총 30종의 농자재 중 16종에서 60% 이하의 사충율을 나타내어 가장 낮은 약효를 지닌 것으로 확인되었다(Table 5).
약제 저항성 돌연변이 비율
채집한 목화진딧물 16개 개체군의 약제 저항성 돌연변이 비율을 산출하였다(Table 6). 유기인계와 카바메이트계 약제 작용점인 A ChE1상의 A302S 돌연변이는 평균 33.8%로서 BA, GJ, WJ1 개체군이 99-100%의 비율을 보였고, S431F의 경우 평균 86.8%로서 모든 개체군에서 44−100%의 비율을 나타내었다. 피레스로이드계 약제 작용점인 VSSC 상의 L1014F 돌연변이는 전체적으로 낮은 비율(1.6%)을 보유하며 SJ2 개체군에서만 26%의 비율로 나타났으나, M918L은 평균 26.3%로서 상대적으로 높은 돌연변이 비율을 보였는데, BR, DJ, GJ, SC, TA, 그리고 WJ1 개체군에서 60−100%의 비율을 보였다. nAChR 유전자의 R81T 돌연변이는 평균 3.8%로서 WJ1 개체군에서만 61%의 비율로 나타났다. 결론적으로, 무궁화에서 월동한 개체군에서 약제 저항성 관련 돌연변이를 보유한 채로 국내에서 생존하는 것을 확인하였으며, 국내 개체군의 돌연변이 빈도는 S431F > A302S > M918L > R81T > L1014F순서로 나타났다.
고 찰
본 연구는 목화진딧물의 1차 기주인 무궁화에서 채집한 7 개체군을 대상으로 30종의 농자재에 대한 약효 평가 결과를 제시하였다. 또한 월동 개체군의 유기인계, 피레스로이드계, 네오니코티노이드계 살충제의 저항성 관련 돌연변이의 존재 여부를 처음으로 밝힌 연구이다.
무궁화에서 월동한 목화진딧물은 시험에 사용한 화학합성 살충제에 대해 전반적으로 높은 약효를 나타내는 것으로 확인되었다. 따라서 무궁화 식재지 증가에 따른 목화진딧물 밀도 증가 시 선발된 농자재를 기반으로 방제가 가능함을 시사한다(Figs. 1, 2). 화학합성살충제 중에서 작용기작 9번, 13번 그룹의 약제들은 약효가 낮게 나타났는데, 이는 사충율 관찰 시간이 24시간으로 짧았고, 해당 약제들의 지효성에 의한 것으로 판단된다. 무궁화 신초에서 정착한 목화진딧물은 무궁화 본엽에서 흡즙력이 감소하고 무처리구 생존률이 약 67%까지 감소하는 것을 확인하여(data not shown), 약효 관찰 기간을 연장할 수 없었다. 이러한 현상은 과수에서 발생한 목화진딧물이 주로 신초에서 발생하였다는 기존 보고와 일치하고(Roistacher et al., 1984; Kwon et al., 2023), 목화진딧물의 필수 영양분 공급원이 주로 신초이지 본엽이 아닌 것을 반증하는 것으로 판단된다. 향후, 무궁화에서 발생한 목화진딧물의 생물검정방법 수립을 위한 추가 연구가 필요할 것이다.
유기농업자재를 이용한 약효 평가에서 O_Test03을 제외하고 7종의 약제에서 사충율이 약 77% 이상으로 나타나는 것을 확인하였다(Fig. 1). 국내에서 유기농업자재를 주요 성분을 기준으로 분류체계를 제안하고(Kwon et al., 2021), 무궁화, 오이, 멜론에서 채집한 목화진딧물을 대상으로 유기농업자재의 약효 스크리닝을 수행하여 유기농업자재 33종 중 7종의 약제는 약 80% 이상의 사충율을 보여 대체 가능한 것으로 나타났다(Kim et al., 2023). 또한, 야외 무궁화의 신초에 발생한 목화진딧물을 대상으로 평가한 결과에서도 유기농업자재의 약효가 나타나(Kwon et al., 2023), 공원의 가로수나 조경수로 식재된 무궁화에 발생한 목화진딧물에 대해 화학합성살충제를 대체하여 유기농업자재로 방제가 가능함을 의미한다.
목화진딧물은 다양한 화학합성살충제에 대해 저항성이 발달된 것으로 보고 되었다(Bass et al., 2015; Feyereisen et al., 2015). 본 연구에서는 16 개체군의 gDNA pool을 대상으로 분자생물학적 분석 결과, 유기인계, 피레스로이드계 그리고 네오니코티노이드계 약제 관련 돌연변이가 월동 개체군에서 존재하는 것을 확인하였다. 유기인계 약제 관련 S431F돌연변이의 비율이 가장 높았고, 피레스로이드계 저항성 관련 L1014F돌연변이의 비율이 가장 낮았다(Table 6). 다만, 유기인계 약제 저항성 빈도와 약효 감소 사이에 상관성은 뚜렷하게 나타나지 않았다(data not shown). 즉, 야외 개체군의 약제 저항성 돌연변이 비율은 약제의 효과와 직접적인 관련성이 낮고, 개체군의 반수치사약량(혹은 농도) 값과 상관성이 높을 것으로 생각된다.
본 연구는 월동 무궁화에 서식하는 목화진딧물 개체군의 밀도 증가와 환경에 미치는 영향을 고려하여 필요한 방제 정보를 제공하고자 화학합성살충제와 유기농업자재에 대한 약효 평가 결과이다. 선발된 약제는 목화진딧물의 안전하고 선제적 관리에 기여할 것이다. 또한 기초 연구 차원에서 수행된 약제 저항성 형질비율 연구는 약제 살포에 따른 야외 개체군의 생태계 상에서 적응현상을 분자유전학적 관점에서 이해하는데 도움을 줄 것으로 사료된다.
Acknowledgments
본 연구는 농촌진흥청의 농업정책지원기술개발사업(RS-2022-RD010375)의 지원을 받아 수행되었음.
이해상충관계
저자는 이해상충관계가 없음을 선언합니다.
REFERENCES
-
Agrios G, 1988. Plant pathology 3rd (ed) Academic Press. San Diego 920.
[https://doi.org/10.1016/B978-0-12-044563-9.50005-0]

-
Bass C, Denholm I, Williamson MS, Nauen R, 2015. The global status of insect resistance to neonicotinoid insecticides. Pestic. Biochem. Physiol. 121:78-87.
[https://doi.org/10.1016/j.pestbp.2015.04.004]

- Chen Q, Shen ZR, Wang YM, 2006. Phenotypic plasticity of aphids and its genetic basis. Acta Entomologica Sinica. 49(5):859-866.
-
Dunn OJ, 1961. Multiple comparisons among means. J. Am. Stat. Assoc. 56(293):52-64.
[https://doi.org/10.1080/01621459.1961.10482090]

- Ebert TA, Cartwright B, 1997. Biology and ecology of Aphis gossypii Glover (Homoptera: aphididae). Southwest. Entomol. 22(1):116-153.
-
Feyereisen R, Dermauw W, Van Leeuwen T, 2015. Genotype to phenotype, the molecular and physiological dimensions of resistance in arthropods. Pestic. Biochem. Physiol. 121:61-77.
[https://doi.org/10.1016/j.pestbp.2015.01.004]

-
Hirata K, Jouraku A, Kuwazaki S, Kanazawa J, Iwasa T, 2017. The R81T mutation in the nicotinic acetylcholine receptor of Aphis gossypii is associated with neonicotinoid insecticide resistance with differential effects for cyano-and nitro-substituted neonicotinoids. Pestic. Biochem. Physiol. 143:57-65.
[https://doi.org/10.1016/j.pestbp.2017.09.009]

- Inaizumi M, 1980. Studies on the life-cycle and polymorphism of Aphis gossypii Glover (Homoptera, Aphididae). Special Bulletin of the College of Agriculture Utsunomiya University 37: 1-112.
-
Jayasinghe WH, Akhter MS, Nakahara K, Maruthi MN, 2022. Effect of aphid biology and morphology on plant virus transmission. Pest Manag. Sci. 78(2):416-427.
[https://doi.org/10.1002/ps.6629]

-
Kim MH, Im JS, Ahn YG, Kwon HY, Park YM, et al., 2023. Insecticidal efficacy monitoring of agricultural materials against Aphis gossypii populations collected at agricultural and forestry area. Korean. J. Pestic. Sci 27(2):75-84. (In Korean)
[https://doi.org/10.7585/kjps.2023.27.2.75]

-
Kinley C, Banu AN, Raut A, Wahengbam J, Jamtsho T, 2021. A review on past, present and future approaches for aphids management. J. Entomol. Res. 45(2):336-346.
[https://doi.org/10.5958/0974-4576.2021.00053.0]

- Korea Forest Service (KFS), 2021. Beautiful mugunghwa spot (11-1400000-000854-01). (In Korean)
- Korea Forest Service (KFS), 2026. Nationwide survey on Mugunghwa growers based on the Act on the Creation and Management of Forest Resources. Retrived on https://nfsv.forest.go.kr/kfsweb/cop/bbs/selectBoardList.do?bbsId=BBSMSTR_1660&mn=AR03_06_02_10
-
Kruskal WH, Wallis WA, 1952. Use of ranks in one-criterion variance analysis. J. Am. Stat. Assoc. 47(260):583-621.
[https://doi.org/10.1080/01621459.1952.10483441]

-
Kwon DH, Kwack GY, Won SM, Kim M, Choi HJ, et al., 2021. Establishment of classification system of major ingredients in organic agricultural materials associated with insect pest control. Korean. J. Pestic. Sci. 25(4):287-304. (In Korean)
[https://doi.org/10.7585/kjps.2021.25.4.287]

-
Kwon DH, Lee YH, Im JS, Ahn YG, Kwon HY, et al., 2023. Establishment of topical shoot spray method of organic agricultural materials for the efficient control of Aphis gossypii in Hibiscus syriacus. Korean J. Pestic. Sci. 27(3):187-201. (In Korean)
[https://doi.org/10.7585/kjps.2023.27.3.187]

- Paik WH, Song KW, Choi SS, 1974. Flying aphid population at the horticultural experiment station, Suweon. Kor. J. Pl. Prot., 13(1):25-31. (In Korean)
-
Pires Paula, D, Lozano RE, Menger JP, Andow DA, Koch RL, 2021. Identification of point mutations related to pyrethroid resistance in voltage-gated sodium channel genes in Aphis glycines. Entomol. Gen. 41(3):243-255.
[https://doi.org/10.1127/entomologia/2021/1226]

- R core team, 2025. R software (Version 4.5.0.).
- Republic of Korea, 2016. Act on the creation and management of forest resources. Retrived on https://www.law.go.kr/%EB%B2%95%EB%A0%B9/%EC%82%B0%EB%A6%BC%EC%9E%90%EC%9B%90%EC%9D%98%EC%A1%B0%EC%84%B1%EB%B0%8F%EA%B4%80%EB%A6%AC%EC%97%90%EA%B4%80%ED%95%9C%EB%B2%95%EB%A5%A0
-
Roistacher CN, Bar-Joseph M, Carson T, 1984. Preferential feeding by Aphis ossypii on young leaves of sweet orange, grapefruit and lemon. IOCV Conference Proceedings. 9(9):19-22.
[https://doi.org/10.5070/C51MW5T2B0]

- Shim ZY, Park JS, Paik WH, 1979. Studies on the life history of cotton aphid, Aphis gossypii Glover (Homoptera). Korean J. Pl. Prot. 18(2):85-88.
- Slosser JE, Pinchak WE, Rummel D, 1989. A review of known and potential factors affecting the population dynamics of the cotton aphid. Southwestern Entomologist. 14(3):302-313.
-
Toda S, Komazaki S, Izawa H, Nakada K, Kanazaki S, et al., 2008. Development of molecular diagnostics of the two point mutations in acetylcholinesterase gene associated with insecticide resistance in the cotton aphid, Aphis gossypii Glover, (Homoptera: Aphididae) and a survey of genotypic frequency in field populations. Appl. Entomol. Zool. 43(1):127-133.
[https://doi.org/10.1303/aez.2008.127]

-
Wang ZJ, Liang CR, Shang ZY, Yu QT, Xue CB, 2021. Insecticide resistance and resistance mechanisms in the melon aphid, Aphis gossypii, in Shandong, China. Pestic. Biochem. Physiol. 172:104768.
[https://doi.org/10.1016/j.pestbp.2020.104768]

Joon Hyun Park: Rearing, Bioassay, Data analysis, Writing
Gi Ryeol Yu: Rearing, Bioassay, Data analysis, Writing, https://orcid.org/0009-0008-6423-6019
Eun Young Yang: Draft review, Information collection, Writing
Yul Gyun Ahn: Draft review, Information collection, Writing
Sora Kim: Draft review, Information collection, Writing, https://orcid.org/0000-0003-4402-5421
Deok Ho Kwon: Experiment design, Data analysis, Draft review & editing, https://orcid.org/0000-0003-2162-4771