청양 지역 고추와 구기자에서 분리한 탄저병균의 동정, 균학적 특징 및 살균제 저항성
초록
병든 고추와 구기자 열매에서 분리한 탄저병균 11균주와 36균주를 동정한 후, 몇 가지의 균학적 특징과 살균제에 대한 반응을 조사하였다. 고추에서 분리한 병원균은 모두 Colletotrichum acutatum의 A2 그룹으로 동정되었다. 구기자에서 분리한 병원균은 14균주가 C. gloeosporioides, 22균주가 C. acutatum으로 동정되었으며, C. acutatum 균주는 15균주가 A1 그룹, 7균주가 A3 그룹에 속하였다. 25°C의 PDA 배지에서 10일간 배양한 후 병원균 균총의 색깔을 조사한 결과, 분리한 기주에 관계없이 C. acutatum은 회백색의 균총을 보였으며, C. gloeosporioides는 균총의 중앙은 주황색을, 주변부로 갈수록 회백색과 주황색이 혼재된 색깔을 나타냈다. 고추에서 분리한 C. acutatum의 분생포자 중에서 양끝이 둥근 형태을 나타내는 포자의 비율은 95% 이상이었으나, 구기자 균주는 75%로, 약 25%의 분생포자가 최소한 한 쪽이 뾰족한 형태를 나타내었다. 실험에서 사용한 모든 균주는 Colletotrichum의 종에 관계없이 25°C가 생장 적온이었다. 한천희석법을 통해서 조사한 고추의 C. acutatum A2 그룹에 속하는 균주의 carbendazim과 carbendazim/diethofencarb 대한 평균 EC50값은 0.68과 3.16 μg/ml이었으며, 구기자의 C. acutatum A1과 A3 그룹은 carbendazim에 대해서 0.21과 0.24 μg/ml, 그리고 합제에 대해서는 1.52와 3.35 μg/ml이었다. 또한 구기자에서 분리한 C. gloeosporioides의 평균 EC50값은 각각의 살균제에 대해서 0.12와 0.92 μg/ml이었다. 두 살균제에 대한 저항성 요인 값(Rf값)은 구기자에서 분리한 C. acutatum 균주 집단이 고추 균주 집단보다 더 높았다.
Abstract
It was conducted to identify all 47 isolates obtained from infected fruits of pepper and boxthorn, and to investigate the mycological characteristics and the response to fungicides. All of 11 isolates from pepper were identified as Colletotrichum acutatum included into A2 group. Among 36 isolates from boxthorn, 14 isolates were identified as C. gloeosporioides, and the others were done as C. acutatum, which were composed as A1 group with 15 isolates and A3 with 7 isolates. After incubating the isolates on PDA at 25°C for 10 days, the colony color of C. acutatum was greyish white, while that of C. gloeosporioides was orange at center of colony and was gradually turned into an greyish white to the periphery. The rate of conidia showing ellongated ellipsoidal shape with round ends was over 95% in C. acutatum isolated from pepper. However, C. acutatum isolated from boxthorn produced ellongated ellipsoidal conidia with the rate of 75%, and the others were pointed at one or both ends. Regardless of species of Colletotrichum, all isolated used in this study was showed an optimal temperature at 25°C. EC50 values of all isolates of Colletotrichum spp. to 2 fungicides as carbendazim and the mixture of carbendazim and diethofencarb was investigated by an agar dilution method. With C. acutatum isolates from pepper belonged to A2 group, the mean of EC50 value to carbendazim and the mixture of carbendazim and diethofencarb was 0.68 and 3.16 μg/ml, respectively. In the case of C. acutatum isolates from boxthorn, which were divided into 2 groups as A1 and A3 group, that to carbendazim was 0.21 at A1 and 0.24 μg/ml at A3, while that to the mixture was 1.52 and 3.35 μg/ml. Isolates of C. gloeosporioides showed the mean of EC50 value was 0.12 μg/ml to carbendazim and 0.92 μg/ml to the mixture. The value of resistant factor was higher in the isolates of C. acutatum obtained in boxthorn than those from pepper.
Keywords:
Anthracnose of pepper and boxthorn, Colletotrichum acutatumColletotrichum gloeosporioides, Resistance to carbendazim키워드:
고추와 구기자 탄저병, carbendazim에 대한 저항성서 론
구기자 탄저병은 Colletotrichum gloeosporioides와 C. dematium 등이 일으키는 것으로 보고되어 있으며, C. gloeosporioides가 C. dematium 보다 발생빈도가 많고 병원성도 강하다(Park와 Kim, 1988). 하지만 Lee (2003)는 구기자 탄저병 병반에서 분리한 Colletotrichum spp. 균주의 형태적, 배양적, 분자생물학적 특징을 조사하여 동정한 결과, 우점종을 C. acutatum으로 발표하였다. 구기자와 마찬가지로 가지과에 속하는 고추 역시 탄저병에 대한 피해가 심한 작물로서, 탄저병을 일으키는 병원균으로 C. gloeosporioides, C. dematium, C. coccodes, C. acutatum, Glomerella cingulata 등 5종이 보고되어 있다(Park와 Kim, 1992). 이러한 고추 탄저병균 역시 과거에 우점종이었던 C. gloeosporioides가 포장에서의 우점종이 C. acutatum으로 변화하였다(Kim et al., 2008).
Colletotrichum속은 주로 열대, 아열대와 온대 지역에 발생하며 곡류, 두류, 채소류, 과수 등 넓은 기주에 침입하여 탄저병을 일으키며(Freeman et al., 1996), 균학적인 형태와 기주 식물에 대한 병원성(Freeman과 Shabi, 1998), 살균제에 대한 반응(Adaskaveg와 Hartin, 1997) 등이 속 내에서도 다양하게 보고되어 있다. 고추와 구기자와 같이 한 종류의 기주 식물을 서로 다른 Colletotrichum의 종이 침입하기도 하고(Adaskaveg와 Hartin, 1997; Zulfiqar et al., 1996), C. acutatum과 같이 아보카도, 아몬드, 딸기, 사과, 복숭아 등 여러 기주를 침입하기도 한다(Adaskaveg와 Hartin, 1997; Bernstein et al., 1995; Freeman과 Shabi, 1998). 뿐만 아니라 Colletotrichum은 종에 따라 침투이행성 살균제인 benomyl에 대한 감수성이 달라서 C. gloeosporioides은 감수성, C. acutatum은 비감수성의 반응을 보인다(Adaskaveg와 Hartin, 1997). Chung 등(2006)도 C. acutatum은 benomyl과 diethofencarb에 대한 반응에서도 모두 비감수성을 보인다고 하였고, C. gloeosporioides는 두 살균제에 대하여 역상관 교차 저항성을 보여 탄저병균 종간에 살균제에 대한 반응의 차이가 있다고 보고하였다.
탄저병균인 Colletotrichum spp.의 전통적 동정 방법에서는 분생포자의 형태와 크기, 강모의 유무, 균핵 형성의 유무, 부착기의 형태 및 기주범위 등을 가지고 탄저병균을 동정하였다(Freeman et al., 1998). 그러나 형태적 특성을 가지고서 병원균을 동정하고자 할 때, 그 특징이 서로 중첩되거나, 배양하는 배지 등에 따라 같은 균주라도 형성되는 분생포자의 크기와 모양이 다를 경우도 있고, 강모의 형성 역시 일관성이 없는 경우가 발생하기 때문에 최근에는 탄저병균이 갖는 다양한 형태·생리적 특징을 조사하거나, 다양한 분자생물학적인 방법을 이용해서 유전자 수준에서 탄저병균을 정확하게 동정하고 있다(Adaskaveg와 Hartin, 1997).
따라서 본 논문에서는 고추와 구기자를 근접한 포장에서 재배하고 있는 충남 청양 지역에서 고추와 구기자에서 탄저병균을 분리하여, 정확한 동정을 하기 위해서 병원균의 ITS 영역의 염기서열을 분석하여 동정함과 동시에, 분생포자의 형태, 온도별 균사생장 정도 등을 조사하였고, 살균제인 carbendazim과 carbendazim/diethofencarb 합제에 대한 병원균의 반응 등을 조사하였다.
재료 및 방법
병원균의 채집 및 분리
2011년 8월 충청남도 청양군의 고추와 구기자 포장에서 탄저병의 전형적인 병반을 보이는 고추와 구기자의 열매를 채집하였다. 병반 부위에서 탄저병균 포자가 형성된 발병조직을 적당한 크기(5 × 5 mm)로 잘라 멸균수 1 ml가 담긴 microtube에 넣고 잘 흔들었다. 살균증류수를 사용하여 1/10로 희석을 한 다음, 포자현탁액에 300 μg/ml의 streptomycin을 첨가하였다. 희석한 포자현탁액에서 100 μl의 현탁액을 취하여 PDA (potato dextrose agar, Difco) 배지에 고르게 접종하고, 25°C에서 1일간 배양하였다. 형성된 단균총을 분리하여 300 μg/ml의 streptomycin이 첨가된 PDA 배지에 접종하고 25°C에서 배양하였다.
분리한 균주들은 새로운 PDA 배지에 옮겨서 25°C 항온기에서 10일간 배양하고 균총의 균사 선단부에서 지름 5 mm의 균사 조각을 떼어내어 CryotubeTM vial (직경 12 mm, 높이 48 mm, Nunc co. Ltd)에 10조각씩 넣고 1 ml의 멸균수를 넣어 상온에서 보관하였다. 또한 장기간 보관을 위해서 5% DMSO (dimetyl sulfoxide)가 첨가된 멸균수에 넣어 -70°C에 보관하였다.
유전자 수준에서 병원균의 동정
PDA 배지에 병원균을 접종하여 25°C에서 1주일간 배양한 후 균사체를 수확하여 12시간 동안 동결건조를 하였다. 동결건조한 시료는 유리봉으로 분쇄한 다음 0.5% SDS-CTAB(2.5 M NaCl, 0.25 M EDTA (pH8.0), 0.5 M Tris-HCl(pH7.5), 1% polyvinylpyrrolidone-10, 1% hexadecyl trimethyl ammonium bromide, 0.5% sodium dodesyl sulfate)를 1.5 ml씩 첨가하고, 65°C에서 1시간 동안 반응시켰다. 반응액은 12,000 g에서 10분간 원심분리를 하였고 상징액을 수거하였다. 상징액에 500 μl의 phenol을 처리하고 하얗게 될 때까지 잘 흔들어준 후에 12,000 g에서 10분간 원심분리를 하였다. 다시 상징액을 수거하여 500 μl의 phenol을 처리하고 동일한 과정을 1회 더 반복하였다. 원심분리 후 수거한 상징액에 동량의 chloroform을 처리한 후, 12,000 g에서 원심분리를 하였다. 상징액은 4°C에서 70% ethanol을 500 μl를 넣고 침전물을 세척하였으며 ethanol을 충분히 건조시킨 후, 50 μl의 살균증류수에 용해시켜 -20°C에서 보관하며 실험에 사용하였다. 또한 DNA를 1.5% agarose gel을 사용하여 1X TAE buffer상에서 100 V/cm3의 전원으로 30분간 전기영동 후 UV illuminator에서 λ DNA를 기준으로 농도를 확인하였고, 확인된 DNA는 다시 0.01 μg/ml으로 정량하여 실험에 사용하였다.
ITS 영역의 DNA를 증폭하기 위해 Kim 등(2008)이 사용한 primer ITS5 (5'-GGA AGT AAA AGT CGT AAC AA-3')와 ITS4 (5'-TCC TCC GCT TAT TGA TAT GC-3')를 사용하여 PCR을 수행하였다. 반응조건은 희석된 DNA 5 μl에 10X KAPA Taq buffer (dye 5 μl), dNTP 5 μl, ITS5 primer(10 pmoles/μl) 3 μl, ITS4 primer (10 pmoles/μl) 3 μl, Taq polymerase (5 units/μl, KAPABIOSYSTEMS) 0.25 μl, 살균증류수 28.75 μl를 첨가하여, 4분간 95°C에서 pre-denaturation 과정을 수행 후, 30초 동안 94°C에서 denaturation, 1분 동안 55°C에서 annealing, 1분 동안 72°C에서 extension 과정을 30회 반복하였으며, 최종적으로 72°C에서 7분 동안 반응을 시킨 후 반응을 종료시켰다. 여기에서 얻어진 PCR 산물들은 TAE buffer (1 M Tris-HCl (pH8.0), 0.25 M EDTA)를 이용하여 제작한 1.5% agarose gel을 사용하여 100 V에서 30분간 전기영동 한 후 UV illuminator를 이용하여 band를 확인하였다. 시료들은 PCR purification kit (GeneAll, Seoul, South Korea)를 사용하여 정제하고 SolGent (Daejeon, South Korea)에 DNA 염기서열 해독을 의뢰하였다.
해독한 염기서열은 PHYDIT ver. 3.1의 clustal X와 chromosome을 이용하여 정리한 후 Neighbor-Joining (NJ)의 방법(Tamura 등, 2004)으로 ITS1-5.8s-ITS2 영역을 이용하여 계통수를 작성하고 1,000회의 bootstrap 분석을 통해 신뢰도를 평가하였다. 실험균주의 분류학적 위치를 비교하기 위해 NCBI GenBank의 염기서열을 획득하여 함께 유연관계도를 작성하였다.
탄저병균의 형태적 특징 조사
본 실험에서 분리한 47균주들을 25°C의 PDA 배지에서 10일간 배양한 후, 배양된 균주들의 균총의 색깔을 조사하였다. 분생포자의 크기 및 형태를 관찰하기 위해 고추와 구기자에서 분리한 균주를 각각 3균주씩 선발하고, 각각의 분생포자를 수확하였다. 선발한 탄저병균은 25°C의 PDA 배지에서 10일간 배양한 후 살균증류수를 붓고 균총의 표면을 멸균한 붓으로 긁어서 분생포자를 수확하였다. 분생포자 현탁액은 4겹의 거즈를 사용하여 여과해서 균사조각을 제거한 후, 광학현미경으로 관찰하며 포자의 형태와 크기를 조사하였다. 각 균주 당 100개의 분생포자의 크기와 모양을 3반복으로 조사하였다.
배양온도에 따른 균사 생장 조사
온도에 따른 균사의 생장속도를 보기 위해 고추와 구기자에서 분리한 Colletotrichum속에 속하는 47개 균주를 PDA 배지에 접종하고, 25°C와 30°C에서 배양하면서 2일마다 균총의 직경을 측정하였다.
살균제에 대한 고추와 구기자 탄저병균의 반응 조사
위의 실험과 동일한 총 47개의 고추와 구기자 탄저병균의 carbendazim (a.i. 95%, Tech.)과, carbendazim/diethofencarb의 합제(a.i. 25%+25%, WP)에 대한 살균제 반응을 조사하였다. 병원균을 PDA 배지에 접종하고 25°C의 항온기에서 7일간 배양한 후 균사 선단 부위에서 직경 5 mm의 균사 조각을 떼어내어 각 약제를 농도별로 첨가한 새로운 PDA 배지에 접종하였다. 살균제를 용해시키기 위한 용매로 carbendazim은 dimethyl sulfoxide(DMSO)를, 그리고 carbendazim과 diethfencarb 합제는 살균증류수를 사용하였다. 두 살균제 모두 PDA 배지에 첨가하여 최종농도가 0.01, 0.1, 1, 10, 100 μg/ml가 되도록 희석하였으며, carbendazim의 경우 PDA 배지 상에서의 DMSO의 최종 농도는 1%가 넘지 않도록 조절하였다. 이 때 PDA 배지에는 세균의 오염을 방지하기 위해서 300 μg/ml의 streptomycin을 첨가하였다. 병원균을 접종한 배지는 25°C에서 7일간 배양한 후 균총의 직경을 측정하였고, 약제를 첨가하지 않은 PDA 배지 상에서의 균총의 직경과 비교하여 균사 생장 억제율(%)을 계산하였다. 각각의 약제가 병원균의 균사생장을 50%와 90%를 억제하는 농도인 EC50값과 EC90값를 구하여 살균제에 대한 각 균주들의 감수성 정도를 비교하였다.
결과 및 고찰
ITS영역 염기서열 분석을 통한 병원균의 종 동정
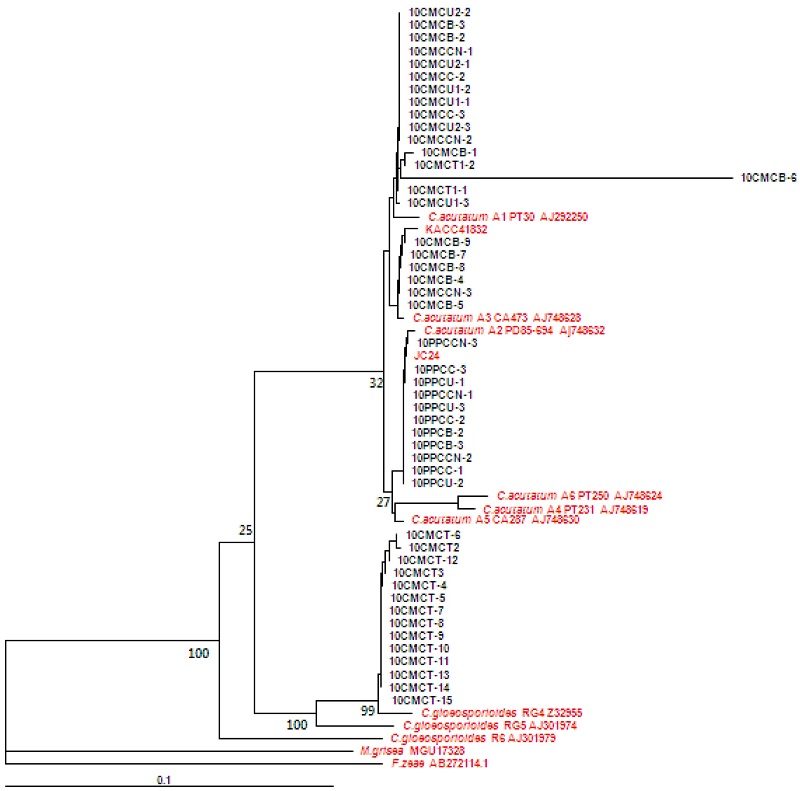
ITS5와 ITS4 primer를 사용하여 ITS 영역을 증폭한 결과, 550 bp의 PCR 산물을 얻을 수 있었다. 증폭한 PCR산물을 클로닝하여 얻은 DNA 염기 서열을 분석하여 병원균의 동정을 수행하였다. 청양 지역의 고추와 구기자에서 총 47개의 Colletotrichum속 균주를 분리하였다. 청양군 운곡면의 구기자시험장에서 채집한 16개의 균주 중에서 10CMCT1-1과 10CMCT1-2를 제외한 나머지 균주는 C. gloeosporioides RG4 Z32955와 같이 그룹을 형성하며 DNA 염기서열이 98% 이상 일치하여 C. gloeosporioides로 동정하였다(Fig. 1). 구기자시험장의 병든 구기자 열매에서 분리한 10CMCT1-1과 10CMCT1-2, 운곡면에서 분리한 10CMCU1-1, 10CMCU1-2, 10CMCU1-3, 10CMCU2-1, 10CMCU2-2, 10CMCU2-3 등 6개 균주, 청양읍에서 분리한 10CMCC2와 10CMCC3, 청남면에서 분리한 10CMCCN1과 10CMCCN2, 비봉면에서 분리한 10CMCB1, 10CMCB2, CMCB3는 C. acutatum의 A1 그룹에 속하는 C. acutatum PT30 AJ292250와 동일한 그룹을 형성하였다. 또한 청남면에서 분리한 10CMCCN3과 비봉면에서 분리한 10CMCB4부터 10CMCB9까지 6개 균주는 A3 그룹에 속하는 C. acutatum CA473 AJ748628과 동일한 그룹을 형성하며, DNA 염기서열은 99.8% 이상의 상동성을 보였다. 청양군 4개 지역에서 채집한 병든 고추에서 분리한 11개의 균주들은 모두 A2 그룹에 속하는 C. acutatum PD85-694 Aj748632와 같은 그룹을 형성하였으며, 상동성은 99.8%이었다. Sreenivasaprasad와 Talhinhas (2005)는 C. acutatum을 형태적인 특징과 유전적 다양성을 조사하여 A1부터 A8까지 8개의 그룹으로 분류하였다. 본 실험에서 분리하여 동정한 고추는 Sreenivasaprasad와 Talhinhas(2005)의 분류와 동일하게 A2 그룹으로 분류되었으나, 동일하게 가지과 작물에 속하는 구기자에서 분리한 탄저병균은 A1과 A3 그룹으로 나누어졌다. 이러한 결과는 구기자에서 분리한 탄저병균의 집단이 고추 탄저병균 집단보다 유전적으로 다양하다는 것을 보여주며, C. acutatum의 경우 고추와 구기자에서 발생하는 집단이 서로 다름을 확인할 수 있었다.
탄저병균 균총의 색깔과 분생포자의 형태 및 크기
고추에서 분리한 C. acutatum의 균주들은 대부분 회백색을 띠고 있는 반면에, 구기자에서 분리한 C. acutatum과 C. gloeosporioides의 균주들은 균총의 중앙 부위는 주황색을 띄지만, 주변은 주황색과 회백색이 혼재되어 있는 모습이었다(Table 1과 Fig. 2). 탄저병균의 균총의 색깔이 병원균의 동정을 위한 기준으로 사용될 수는 없으나, 고추와 구기자 탄저병균의 균총의 색깔이 다르다는 것은 두 병원균 집단에 다양한 차이가 있음을 보여주고 있다. 고추에서 분리된 C. acutatum KACC40690은 PDA 배지에서 배양할 경우 흰색을 나타내기도 하고, 사과에서 분리한 C. acutatum의 경우에는 주황색, 흰색 또는 회색을 띄는 경우도 있는데(Kim et al., 2008), 구기자 탄저병균의 경우는 중앙 부위의 주황색이 균사 선단으로 가면서 회백색과 혼합되는 양상을 보여주고 있었다.

Isolates used in this study, host plnats, and colony color of Colletotrichum spp. obtained from infected fruits of pepper and boxthorn cultivated in Cheongyang
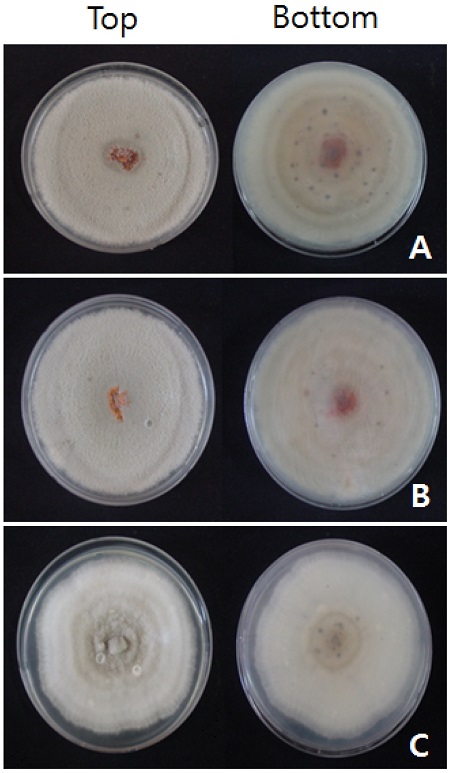
Morphological characteristics of colonies of Colletotrichum gloeosporioides 10CMCT-9 (A) and C. acutatum 10CMCU2-3 (B) isolated from boxthorn, and C. acutatum 10PPCU-2 (C) isolated from pepper, which were inoculated on PDA and incubated at 25°C for 10 days under the dark condition.
구기자에서 분리한 36균주 중에서 C. acutatum 10CMCU1-1, 10CMCC2, 10CMCU2-3 등 3개 균주와, 11개의 고추 균주 중에서 C. acutatum 10PPCU1, 10PPCU2, 10PPCCN1 등 3개 균주를 선발하여 분생포자의 크기와 형태를 조사하였다(Table 2). 구기자에서 분리한 병원균의 분생포자 장경과 단경은 (10.09 ± 2.03) × (4.10 ± 0.71) μm이었으며, 고추에서 분리한 병원균의 장경과 단경은 (10.34 ± 1.84) × (4.56 ± 0.71) μm로 두 그룹 간에 유의성 있는 차이는 없었다. 분생포자의 모양을 조사한 결과, 고추에서 분리한 균주와 구기자에서 분리한 균주 간에 차이가 있었다. 고추에서 분리한 C. acutatum 균주는 Kim 등(2008)의 보고와 같이 양끝이 둥근 원통형 포자의 비율이 평균 95%인 반면, 구기자에서 분리한 C. acutatum 균주는 원통형인 포자의 비율이 75%로 고추에 비하여 낮았다. 구기자 탄저병균의 경우 방추형 포자의 비율은 15.3%, 한 쪽만이 뾰족한 형태를 갖는 포자는 9.7%로, 고추 균주보다 높은 비율로 나타났다.

Size and shape of conidia of Colletotrichun acutatum isolated from infected fruits of pepper and boxthorn in Cheongyang
아몬드에서 분리한 C. acutatum의 분생포자 형태를 관찰하면 최소한 한 쪽 끝이 뾰족한 형태로 나타난다(Adaskaveg와 Forster, 2000). 하지만 고추에서 분리한 C. acutatum은 대부분의 포자의 끝이 둥근 원통형이었으며, 구기자 탄저병균은 75%가 고추 탄저병균과 같은 원통형태이었다. 결국 포자의 끝이 뾰족하다는 C. acutatum의 형태적 특징이 탄저병균 동정의 기준이 되기에는 여러 가지 예외적인 균주들의 출현으로 불가능할 것으로 생각한다.
탄저병균의 온도별 균사 생장
본 실험에서 사용한 47개의 모든 균주는 Colletotrichum의 종에 관계없이 30°C보다는 25°C에서 균사 생장이 더 빨랐다. 고추와 구기자 탄저병균을 25°C의 PDA 배지에서 배양하며 일일 균사생장률을 조사한 결과, 고추에서 분리한 C. acutatum 균주의 일일 평균 균사생장률은 7.1 mm/일이었으며, 구기자에서 분리한 C. acutatum 균주들의 일일 평균 균사생장율은 6.9 mm/일, C. gloeosporioides 균주의 경우에는 6.6 mm/일로 나타나, 분리된 기주와 각 병원균의 종간에 균사생장률에는 차이가 없었다(Table 3). 30°C에서 세 그룹에 속하는 탄저병균의 일일 평균 균사생장률은 2.6 mm/일로 동일하였다. 구기자에서 분리한 C. gloeosporioides 10CMCU1-1 등 4개 균주와 C. acutatum CMCT3 등 4개 균주를 선발하여 고추에서 분리한 C. gloeosporioides KACC 40690과 20, 25, 30°C의 PDA 배지에서 일일 평균 균사생장률을 조사하였다. Fig. 3에서 보는 것과 같이 고추에서 분리한 C. gloeosporioides KACC40690은 청양의 구기자에서 분리한 C. acutatum와 C. gloeosporioides의 8개 균주보다 모든 배양 온도에서 빠르게 생장하였다. 구기자에서 분리한 C. acutatum와 C. gloeosporioides의 총 8개의 균주 모두는 25°C에서 균사가 가장 빠르게 생장하였으며, 배양 온도가 20°C로 낮아지거나, 30°C로 높아질 경우에는 생장이 늦어지는 반면, 고추에서 분리한 C. gloeosporioides KACC40690은 25°C보다도 30°C에서 일일 평균 균사생장율이 11.98 ± 1.53 mm/일로 가장 빨랐다.

Mycelial growth rate of Colletotrichum acutatum and C. gloeosporioides isolated from infected fruits of pepper and boxthorn in Cheongyang
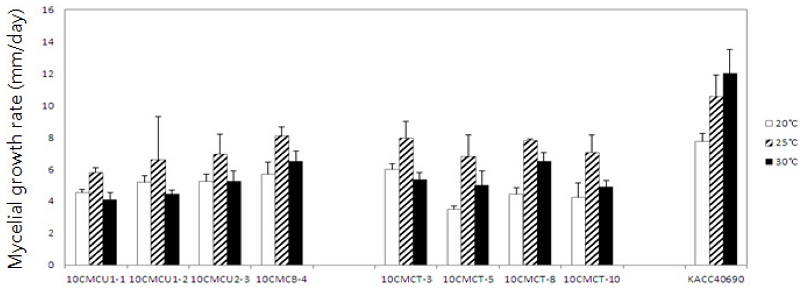
Mycelial growth of Colletotrichum gloeosporioides (10CMCT-3, 10CMCT-5, 10CMCT-8 and 10CMCT-10) and C. acutatum (10CMCU1-1, 10CMCU1-2, 10CMCU2-3 and 10CMCB-4) at each temperature, such as 20, 25, and 30°C. Except for KACC40690 which was isolated from infected pepper fruit and identified as C. gloeosporioides, all isolates were obtained from boxthorn collected in Cheongyang. For calculating mycelial growth rate per one day, everyday was investigated the colony diameter of each isolate on PDA at the indicated temperature.
Adaskaveg와 Forster (2000)는 C. acutatum과 C. gloeosporioides를 비교할 때, C. acutatum의 생장 적온은 25°C인데, 적온에서 배양할 경우도 일일 균사 생장이 10 mm 이하로 느린 생장을 보인다고 하였다. 반면에 C. gloeosporioides는 30°C가 적온이며, 적온에서 배양할 경우 일일 균사생장이 10 mm가 넘게 빠르게 생장하였다. 하지만 구기자에서 분리한 탄저병균 중 C. gloeosporioides는 C. acutatum과 동일하게 생장적온이 25°C로, 고추에서 분리된 C. gloeosporioides KACC40690와는 다른 양상을 보이고 있었다. 이는 구기자에서 탄저병을 일으키는 C. gloeosporioides의 생리적 변화가 일어났을 가능성을 보여주는 결과라고 생각한다. 이러한 생리적 변화는 병원균의 포장 다양성으로 이어질 수 있기 때문에 다양한 형질의 조사가 필요할 것으로 본다.
Carbendazim과 carbendazim/diethofencarb 합제의 균사생장 억제효과
고추에서 분리한 C. acutatum A2에 속하는 균주의 carbendazim에 대한 평균 EC50값은 0.68 μg/ml로 최소와 최대 범위는 0.21-1.39 μg/ml이었고, EC90값은 모두 100 μg/ml 이상이었다(Table 4). 구기자에서 분리한 C. acutatum 균주 중에서 A1 그룹에 속하는 15균주의 평균 EC50값은 0.21 μg/ml (0.01-1.75 μg/ml 사이)이었으며, 10CMCU1-2를 제외한 14균주의 EC90값은 100 μg/ml 이상이었다. 하지만 A3 그룹에 속하는 7균주의 평균 EC50값은 0.42 μg/ml (0.01-1.85 μg/ml)이었다. 구기자에서 분리한 C. gloeosporioides의 평균 EC50값은 10CMCT-13을 제외하면, 0.12 μg/ml(0.02-0.32 μg/ml)였고, EC90값은 10CMCT-12를 제외한 나머지 균주들이 모두 100 μg/ml 이상이었다. 집단 내의 저항성 요인인 Rf값은 고추의 C. acutatum A3 균주들은 6.6이었지만, 구기자의 C. acutatum A1과 A3는 각각 175와 185이었으며, C. gloeosporioides 균주들은 16이었다. carbendazim/diethofencarb 합제에 대한 EC50값과 EC90값을 조사하였다. 고추에서 분리한 C. acutatum A2의 평균 EC50값은 3.16 μg/ml이었고, 구기자에 분리한 C. acutatum A1과 A3의 평균 EC50값은 1.52와 3.35 μg/ml이었다. 구기자에서 분리한 C. gloeosporioides의 평균 EC50값은 0.92 μg/ml로 다른 그룹보다 낮은 EC50값을 나타냈다. Rf값은 고추의 C. acutatum A2 균주들은 3.5 이었지만, 구기자의 C. acutatum A1과 A3은 각각 19.7과 35.0, C. gloeosporioides는 8.8로, 고추에서 분리한 균주들보다 더 높았다. 이러한 결과는 포장에서 주요 작물의 병원균 집단 변화를 예측함과 동시에 화학적 방제를 위해서 필요한 살균제를 선택하는데 도움을 줄 것으로 생각한다.

Effect of carbendazim and mixture of carbendazim and diethofencarb on the mycelial growth of Colletotrichum acutatum and C. gloeosporioides
구기자에서 분리된 탄저병균은 고추와 다르게 C. acutatum과 C. gloeosporioides 두 종류였으며, C. acutatum의 경우 도 A1과 A3 그룹이 같이 존재하는 다양성을 보여주고 있다. 이러한 병원균의 생리·유전적 다양성은 살균제에 대한 반응에도 영향을 미치는 것으로 생각되며, 그 결과 포장에서 병원균의 저항성 요인 값이 고추 탄저병균보다 높게 나타났다. 그런데 저항성 요인 값이 높다는 것은 살균제 저항성 발현 가능성이 높음을 예측할 수 있는 정보이기 때문에, 구기자 포장에서 탄저병 방제를 위해서 사용된 살균제의 관리가 철저히 이루어져야 한다.
Acknowledgments
This study was supported by National Azenda Program (PJ009324) of Rural Development Administration, Republic of Korea.
Literature Cited
- Adaskaveg, J. E., and H. Forster, (2000), Occurrence and management of anthracnose epidemics caused by Colletotrichum species on tree fruit crops in California, In Colletotrichum; host specification, pathology and hostpathogen intraction, Prusky, D., S. Freeman, and M. B. Dickman, p317-336, eds by APS press, St. Paul, Minnesota.
-
Adaskaveg, J. E., and R. J. Hartin, (1997), Characterization of Colletotrichum acutatum isolates causing anthracnose of almond and peach in California, Phytopathology, 87, p979-987.
[https://doi.org/10.1094/PHYTO.1997.87.9.979]

-
Bernstein, B., E. I. Zehr, and R. A. Dean, (1995), Characteristics of Colletotrichum from Peach, Apple, Pecan, and Other Hosts, Plant Dis, 79, p478-482.
[https://doi.org/10.1094/PD-79-0478]

-
Chung, W. H., H. Ishii, K. Nishimura, M. Fukaya, K. Yano, and Y. Kajitani, (2006), Fungicide sensitivity and phylogenetic relationship of anthracnose fungi isolated from various fruit crops in Japan, Plant Dis, 90, p506-512.
[https://doi.org/10.1094/PD-90-0506]

- Freeman, S., T. Katan, and E. Shabi, (1996), Characterization of Colletotrichum gloeosporioides isolates from avocado and almond fruits with molecular and pathogenicity tests, Appl. Environ. Microbiol, 62, p1014-1020.
-
Freeman, S., and E. Shabi, (1998), Cross-infection of subtropical and temperate fruits by Colletotrichum species from various hosts, Physiol. Molecular Plant Pathol, 49, p395-404.
[https://doi.org/10.1006/pmpp.1996.0062]

-
Kim, J. T., S. K. Park, W. Choi, Y. H. Lee, and H. T. Kim, (2008), Characterization of Colletotrichum Isolates Causing Anthracnose of Pepper in Korea, Plant Pathol. J, 24, p17-23.
[https://doi.org/10.5423/PPJ.2008.24.1.017]

- Lee, B. H., (2003), Morphology, pathogenicity and molecular phylogenetic analysis of Colletotrichum spp. associated with anthracnose of Chinese matrimony (Lycium chinense Mill.), MS thesis, chungnam National University, Daejeon, Korea.
- Park, K. S., and C. H. Kim, (1992), Identification, distribution and etiological characteristics of anthracnose fungi of red pepper in Korea, Korean J. Plant Pathol, 8, p61-69, (in Korean).
- Park, S. K., and K. C. Kim, (1988), Virulence of anthracnose fungi to local varieties of Chinese matrimony vine and varietal resistance, Korean J. Plant Pathol, 4, p95-102, (in Korean).
-
Sreenivasaprasad, S., and P. Talhinhas, (2005), Genotypic and phenotypic diversity in Colletotrichum acutatum, a cosmopolitan pathogen causing anthracnose on a wide range of hosts, Molecular Plant Pathology, 6, p361-378.
[https://doi.org/10.1111/j.1364-3703.2005.00291.x]

-
Tamura, K., M. Nei, and S. Kumar, (2004), Prospects for inferring very large phylogenies by using the neighborjoining method, Proc. Natl. Acad. Sci. USA, 101, p11030-11035.
[https://doi.org/10.1073/pnas.0404206101]

-
Zulfiqar, M., R. H. Brlansky, and L. W. Timmer, (1996), Infection of flower and vegetative tissues of citrus by Colletotrichum acutatum and C. gloeosporioides, Mycologia, 88, p121-128.
[https://doi.org/10.2307/3760791]