수출딸기 선별장에서 잿빛곰팡이병원균 밀도조사와 저장온도에 따른 잿빛곰팡이병 발생 연구
Correspondence to: * E-mail: kwak@gnu.ac.kr
초록
국내 딸기는 현재 홍콩, 싱가포르 및 동남아시아 지역으로 수출량이 증대되고 있는 가운데 유통과정에서 환경조건에 따라 품질에 손상이 크게 발생하고 있다. 주로 수출딸기에 품질손상을 일으키는 잿빛곰팡이병은 다른 국가로 이동하는 동안 혹은 수입국에서 소비자에게 판매되기까지의 기간 동안 발생하고 있다. 본 연구는 수출딸기 선별장 공기중 부유중인 잿빛곰팡이병원균의 밀도와 저장중 발병률에 관한 상관관계를 규명하기 위하여 수행되었다. 공기중 병원균의 밀도가 증가함에 따라 저온 저장중 병 발생율이 최대 16%로 나타났다. 상온저장의 경우 상대적으로 공기중 병원균의 밀도가 낮게 조사된 12월 말부터 발병율 100%가 관찰 되었다. 본 연구결과, 선별장의 잿빛곰팡이 병원균 밀도와 저장중 병발생의 상관관계가 구명되었다.
Abstract
Currently, amount of export strawberry has been continuously increased to ship many south Asia countries, including Hong Kong and Singapore. In the distribution process, significant damage to the quality has been caused depending on the environmental conditions. Gray mold disease caused by Botrytis cinerea has been known as major damage to the export strawberry, and the disease was caused during shipping and distribution to the final consumers. This study was performed to assess the relationship between pathogen density in packing shed and disease incidence of gray mold during storage period. Maximum gray mold disease incidence in storage period was up to 16% with low temperature condition (4°C). At room temperature condition, the disease incidence reached up to 100% even densities of the pathogen spore were recorded relatively low in the packing shed. As results of the study, the correlation between pathogen density in the air and disease occurrence clearly clarified.
Keywords:
Gray mold, Packing shed, Spore, Strawberry키워드:
잿빛곰팡이, 선별장, 포자, 딸기서 론
국내 생산 딸기(Fragaria raananassa Duch.) 수출 지역은 아시아권인 홍콩이 25.2%, 동남아권역 싱가포르 38.6% 등이며, 2012년 12월 기준으로 연 2,000톤 이상이 수출되고 있다. 수출딸기는 선박이나 항공을 통해 운송되고 있으며, 운송기간 동안에 저장성이 높은 딸기인 ‘매향’을 주로 재배하고 있다. 전체 수출 딸기의 92% 이상이 경남 진주시 인근에서 재배되고 있다. ‘매향’은 국내에서 육성된 품종으로써 딸기의 신맛과 단맛이 조화를 이루고 향기가 우수하여 해외로부터 품질을 인정받아 수출물량이 증가하고 있다(Kim et al., 2004). 수출 딸기는 포장에서 공동선별장으로 이동된 후 선별장에서 과실의 크기 별로 선별되는 과정 그리고 포장재를 이용한 포장이 이루어지고 있다(Park et al., 2012a, 2012b). 하지만 선별 및 수출 과정 또는 현지 유통판매 과정에서 딸기 물리적 손상이나 잿빛곰팡이에 의한 피해가 50%에 달할 정도로 증가되고 있다(Hwang and Ku, 2004). 이에 대한 방안으로 일반농가에서도 사용이 가능한 저온저장방법(Jeong et al., 1990) 즉 수확 직후 예냉 처리하는 방법을 통해 신선도를 유지하고(Kader, 1992) 있으나 큰 효과를 얻지 못하고 있다.
국내 수출딸기에 발생되는 잿빛곰팡이병원균, Botrytis cinerea는 고추, 오이, 토마토, 인삼부터 딸기에 이르기 까지 총 86종에 이르는 매우 넓은 기주범위를 지니는 병원균으로 알려져 있다(The Korean Society of Plant Pathology, 2009). 딸기에서의 잿빛곰팡이병원균은 수확 후 저장 또는 수출 과정 중에 발생되어 과실을 부패시켜 경제적으로 매우 큰 손실을 일으키고 있는 실정이다(Jarvis, 1977). 잿빛곰팡이병은 포장으로부터 이동되어온 1차 전염원이 분생포자를 통해 전염되며 과실과 꽃받침에 갈색 반점을 형성하고 심한 경우 지제부에 무름 증상이 나타나기도 한다(Braun and Sutton, 1987). 재배 포장에서 발생하는 잿빛곰팡이병의 방제 연구는 수행되었으나(Nam et al., 2011), 선별장의 소독기준이나 선별장의 공기 중에 존재하는 병원균 밀도 파악 및 병원균의 감염여부 등에 대한 연구가 이루어진 바가 없다.
이에 본 연구는 예냉을 통해 잿빛곰팡이병 발생이 현저히 감소(Park et al., 2012b) 한다고 밝혀져 있는 것을 바탕으로 저장온도인 4°C와 상온저장에서의 잿빛곰팡이병 발생빈도를 확인하고자 실시하였다. 또한 공동 선별장에서의 잿빛곰팡이 병원균 포자 밀도변화에 따른 잿빛곰팡이병 발생의 상관관계를 확인하고 이를 통해 공동 선별장 잿빛곰팡이 병원균 밀도 관리 방안에 대한 기초 자료로 이용하고자 수행되었다.
재료 및 방법
선별장에서의 포자채집 및 채집된 포자의 농도 측정
수출딸기 선별장은 경남 진주시 수곡면에 소재하는 선별장을 지정하였다. 선별장의 크기는 30 × 40 미터 넓이로 총 6 라인의 선별대 시설을 갖추고 있다.
선별장의 구역을 입구에 위치한 선별대 중앙과 출구에 위치한 선별대 중앙 그리고 선별장 내부의 선별대 중앙으로 각 3구역으로 나누어 포자를 채집하였다. 포자의 채집은 2013년 11월 28일부터 2014년 4월 16일 까지 2주 간격으로 총 8회 수행되었다.
포자 채집방법은 선별대 위에 포자채집기(UCK Bio-CultureTMUPump)를 위치시킨 후 PDA (Potato Dextrose Broth: 24 g, Agar: 20 g,distilled water /1 L, 진균배양배지) 배지를 채집기 내부에 고정시킨 다음 채집기를 작동시켜 2분간 선별장 내부의 공기를 흡입하였다. 동일한 방법으로 잿빛곰팡이 선택배지인 BSTM (glucose: 2 g, NaNO3: 0.1 g, K2HPO2: 0.1 g, MgSO47H2O: 0.2 g, chlorampenicol: 0.2 g, pentachloronotrobenzene: 0.02 g, Maneb 80: 0.02 g, Rubigan: 0.1 ml, tannic acid: 5 g, agar: 20 g, per 1 L) 배지에서도 실시하였다. 각 배지의 공기 중 부유 포자 채집은 3반복으로 진행 되었다. 공기흡입이 완료된 배지들은 Parafilm으로 밀봉 한 후 28°C에서 7일간 배양한 다음 곰팡이의 Colony 개수를 측정하고 그 값을 CFU Log/L 단위로 나타내었다.
선별장 잿빛곰팡이 병원균, 일반 진균 분리 및 동정
선별장에서 채집된 포자의 농도를 측정한 후 BSTM배지에서 잿빛곰팡이 병원균 포자의 colony를 새로운 배지에 계대배양 하였으며 1차 계대배양 후 단일 colony 형태가 배지에서 배양이 될 때까지 반복적으로 계대배양을 수행하였다. 단일 colony 형태로 배양된 후 배지에 멸균수 5 mL을 분주하여 피펫으로 균사와 포자 그리고 멸균수가 잘 혼합 하였다. 혼합된 Spore stock을 슬라이드글라스에 5 uL를 분주한 후 커버글라스로 덮은 다음 400배의 배율에서 광학 현미경을 통해 포자의 형태를 관찰하였다.
분자생물학적 동정을 위해 5 mL PDB broth배지에 균사를 접종한 후 28°C 8 shaking incubator에서 2일간 배양하였다. 배양된 균사를 배지와 함께 1 mL을 새로운 Eppendorf tube에 옮긴 후 13,000 rpm으로 원심분리기를 작동시켜 균사 pellet을 만든 다음 CTAB buffer를 500 uL 분주하였다. CTAB기법을 통하여 genomic DNA를 정제한 후 진균 동정용으로 사용되고 있는 ITSI, ITSIVprimer를 이용하여 분자생물학적 동정을 실시하였다(White et al., 1990). PCR의 과정은 Taq polymerase 5 Unit, dNTP 1 uL , 2X Buffer 2 uL, 각 10 pmol의 ITSI primer와 ITSIVprimer, 50 ug의 genomic DNA, 그리고 ddH2O를 넣어 20 uL volume으로 PCR을 진행 하였다. PCR 산물 2 uL와 loading buffer 1 uL를 피펫으로 잘 혼합 한 후 1% agarose gel에 넣고 15분간 loading한 후 밴드를 확인 하였으며 sequencing은 솔젠트(SolGent Co., Korea)를 통해 진행하였다.
저장온도에 따른 잿빛곰팡이병 병발생도 측정
경남 진주시 수곡면 공동선별장에서 포장이 완료된 딸기를 30분간 이동한 후 각각 4°C와 상온(21°C)에서 10일간 보관하였다. 저장 10일 경과 후 낱개의 포장단위에 있는 딸기의 개수를 측정하였다. 그리고 나서 잿빛곰팡이병이 발생한 딸기의 개수를 측정하여 총 과실개수에서 병이 걸린 과실을 백분율로 환상하였다. 4°C와 상온에서의 처리구들은 각각 12개의 과실이 포장된 낱개의 포장단위 8개를 각각 반복으로 총 8반복으로 조사하였다.
결과 및 고찰
선별장에서 채집된 포자의 농도 측정 및 동정
진주시 수곡면에 위치한 딸기 선별장의 대기에 존재하는 곰팡이를 PDA와 잿빛곰팡이 포자 선택배지인 BSTM을 이용하여 각각의 배지를 3반복으로 측정한 결과, 채집 시기별로 포자량의 차이가 통계적으로 다르게 나타났다(Fig. 1). 채집된 포자량이 적은 경우 Fig. 1D와 같이 BSTM에서는 6개의 colony가 측정 되었으나 시간이 경과할 수록 Fig. 1E, 1F와 같이 colony가 증가 하였다. BSTM 배지상에서 잿빛곰팡이 포자 colony의 경우 배지의 색이 갈색으로 변하는 것을 기준으로 기록하였다. 진균배양배지인 PDA의 경우 BSTM과 마찬가지로 Fig. 1의 A, B, C순으로 시간이 경과할수록 colony의 수는 증가하였으며 선택배지 보다 colony의 수가 높게 측정 되었다.
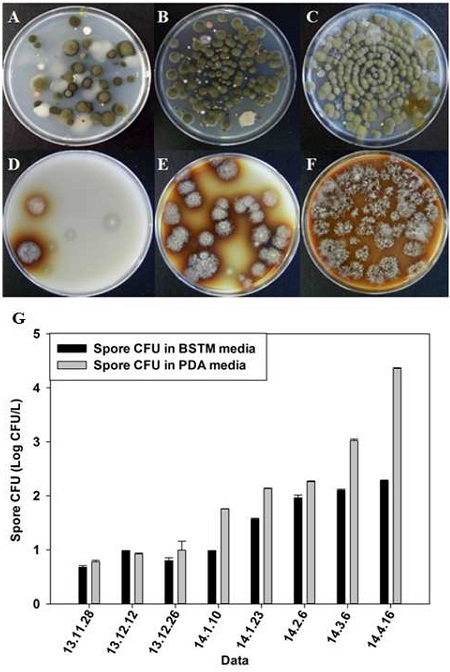
Floating spore densities of gray mold pathogen in packing shed on PDA (A, B, C) media and BSTM media (D, E, F). PDA and BSTM media were incubated at 28°CS for 7 days. Average floating spore densities during survey periods (G).
각각의 배지에서 측정된 Colony를 이용하여 Fig. 1을 통해 밀도를 측정한 결과, 12월까지는 PDA와 BSTM에서 채집된 포자의 양에 큰 차이가 없으나 1월 이후에는 PDA에서 많은 양의 포자가 채집되었다. PDA에서 많은 양의 포자가 채집되는 경우에도 BSTM에서는 잿빛곰팡이 포자만이 채집되었으므로 BSTM이 우수한 잿빛곰팡이 선택배지라고 평가되었다.
선별장에서 잿빛곰팡이의 농도가 시간이 경과함에 따라 증가되는 이유는 몇 가지로 정리할 수 있다. 선별장 내부에서 파지용 딸기를 배출하지 않고 장시간 선별장 내부에 머무르게 하는 점과 선별장으로 유입되는 딸기에 Fig. 2에 나타나듯이 감염된 과실이 유입되는 점으로 보아 선별장에서 시간이 경과할수록 대기 중 병원균 포자의 농도가 지속적으로 축적되어지는 것으로 사료된다.
선별장에서 채집된 잿빛곰팡이 병원균의 동정
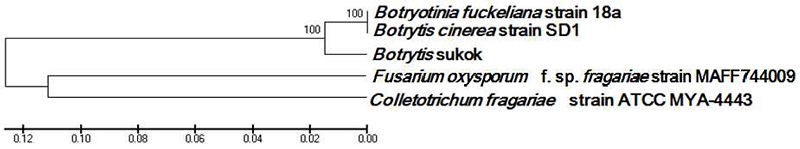
선별장에서 채집된 BSTM 배지로부터 잿빛곰팡이 병원균을 순수하게 분리 하였다. 분리된 균사를 동정하기 위해 CTAB기법을 통해 정제된 DNA를 이용하여 ITS PCR한 결과 500 bp에서 band가 확인되었다(결과 미제시). PCR 산물을 ITS 1 primer와 ITS 4 primer로 염기서열 분석한 결과를 NCBI blast (www.ncbi.nlm.nih.gov/BLAST)를 통해 확인한 결과 Botrytis cinerea와 99% 일치하였다(Back et al., 2014). 또한, 선별장에서 분리된 잿빛곰팡이병원균의 sequence를 MEGA6 program을 통해 유연관계를 확인한 결과 Botrytis sp., B. cinerea와 유연관계가 확인되었다(Fig. 3). 이러한 결과를 바탕으로 선별장에 부유주인 포자중 BSTM에서 분리된 진균은 딸기 잿빛곰팡이의 병원균임이 확인되었다.
선별장 공기 중 부유 진균 동정
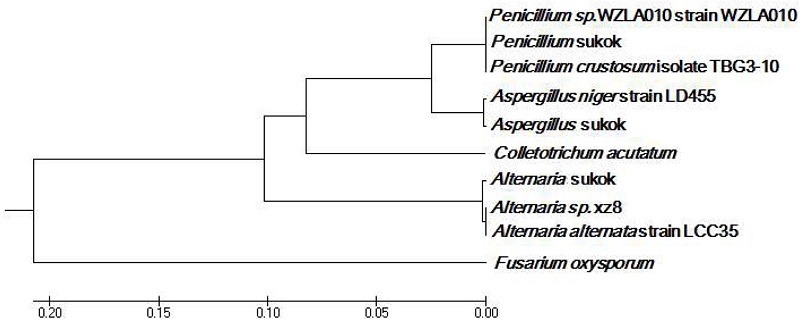
선별장에서 채집된 PDA와 BSTM 배지로부터 colony 형태가 다른 균사를 PDA에 계대배양을 통해 단일 colony형태로 분리 하였다. 단일 colony형태의 균사를 PDB에서 배양한 후 CTAB기법을 통해 정제된 DNA를 ITS PCR한 결과 500 bp에서 band가 확인되었다. PCR산물은 잿빛곰팡이 병원균과 마찬가지로 sequencing을 진행 하였으며 분석된 sequence를 이용하여 NCBI에서 blast한 결과 Penicillium 1종, Aspergillus 1종, Alternaria 2종이 동정되었으며 2개의 sample은 동정이 되지 않았다. 동정된 균의 sequences 유연관계를 분석한 결과 Penicillium속은 Penicillium sp.와 P. crustosum과 일치하였으며, Aspergillus속으로 동정된 진균은 Aspergillus niger와 일치하였다. Alternaria속은 A. alternata와 일치하였으며 각각은 99%의 유사성을 나타내었다(Fig. 4). 선별장의 대기중에는 잿빛곰팡이 병원균뿐 아니라 Penicillium 속, Aspergillus 속, Alternaria 속에 속하는 다양한 곰팡이가 존재한다는 것을 확인하였다.
저장 중 과실에서의 곰팡이 오염 발생율 측정
선별장에서 포장된 딸기를 상온과 저온저장(4°C)에 저장하면서 과실에서 발생되는 잿빛곰팡이병의 발생정도를 측정하였다. 10일간 저장한 결과, 저온저장된 딸기의 경우 포자의 비산이 비교적 소량이였던 11월과 12월는 상대적으로 낮은 발생율을 나타내었다(Fig. 5). 1월과 2월에는 저온 저장한 딸기에서도 잿빛곰팡이의 발생량이 나타나는 것으로 조사되었다. 이와 달리 상온에서 저장한 딸기의 경우 11월부터 딸기 과실에서 잿빛곰팡이의 발생이 확인 되었으며, 12월 후반기부터 조사 종료 시점인 4월 중순까지는 100%로 조사되었다(Fig. 5). 본 실험에서는 저온에서 저장한 딸기의 경우 과실에서의 Fig. 5와 같이 병발생 정도가 최대 16%에 달하였으며, 상온에 저장한 경우 잿빛곰팡이병의 발생정도가 30%에서 100%까지 발생하는 것을 확인하였다. 선별장의 잿빛곰팡이병원균의 부유 밀도와 저장 중 잿빛곰팡이병 발생이 뚜렷한 상관 관계를 나타내는 것으로 조사되었다(Fig. 6). (통계적 처리 방법 등, 그림에 지적한 내용 참고하여 재작성 필요)
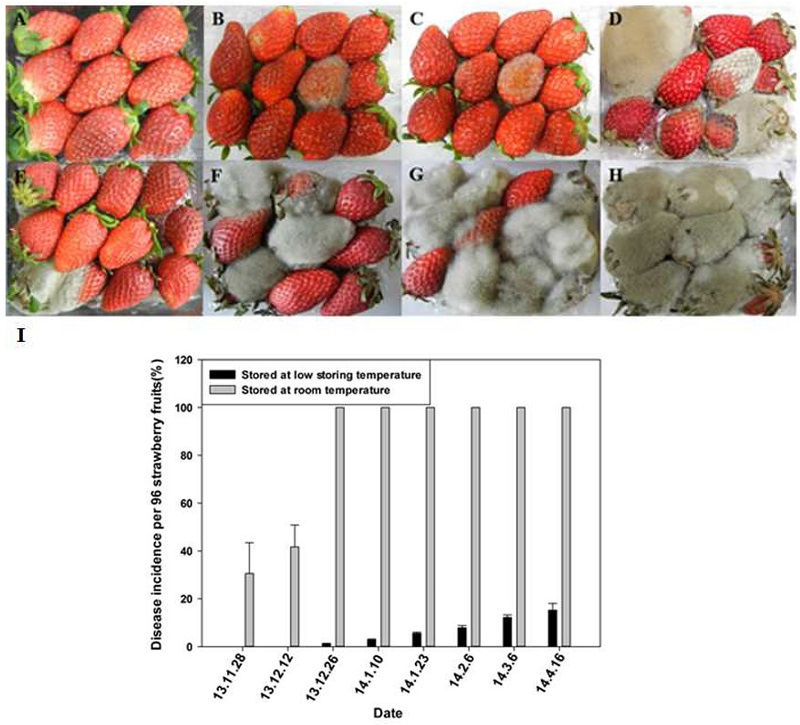
Gray mold disease incidences based on storage temperature conditions. (A, B, C, D) Strawberry packages were stored at low temperature (4°C) for 10 days. (E, F, G, H) The packages were stored at room temperature for 10 days. (I) Decay ratio of gray mold disease in storage strawberry in both temperature conditions.
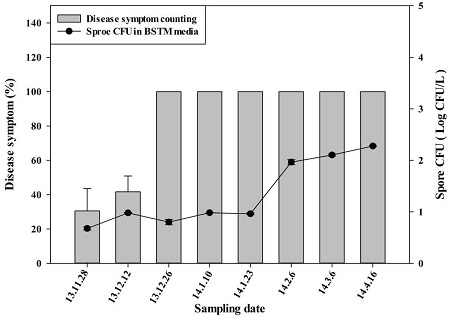
Correlation between B. cinerea spore density in the air and decay disease incidence. The spore densities were detected by BTSM media. the export strawberry packages were incubated at room temperature and then decay ratios were recorded.
저온저장법이 저장, 운송중인 딸기 잿빛곰팡이병의 발생을 감소시킬 수 있는 좋은 대안인 것이 확인되었다. 하지만, 저온 저장중인 딸기에서도 저장 시간이 경과함에 따라 잿빛곰팡이병의 발생이 증가하는 것으로 조사되었다. 선별장에서 부유중인 잿빛곰팡이포자 밀도와 저장 중 병발생과의 상관관계가 확인 되었다. 따라서, 근본적인 대책으로 선별장내부유중인 잿빛곰팡이 병원균의 밀도를 감소시키는 방법을 통하여 수출 딸기의 오염 방지 기술 개발이 필요하다는 것이 본 연구결과를 통하여 도출되었다.
Acknowledgments
본 연구는 농림축산식품부 농림수산식품기술기획평가원 농업생명산업기술개발사업(과제번호 315004-5)의 지원에 의해서 수행되었습니다.
Literature Cited
-
Back, C. -G., S. -Y. Lee, and H. -Y. Jung, (2014), Molecular phylogenetic analysis of Botrytis cinerea occurring in Korea, Kor. J. Mycol, 42, p138-143, (in Korean).
[https://doi.org/10.4489/KJM.2014.42.2.138]

-
Braun, P. G., and J. C. Sutton, (1987), Inoculum sources of Botrytis cinerea in fruit rot of strawberries in Ontario, Can. J. Plant Pathol, 9, p1-5.
[https://doi.org/10.1080/07060668709501903]

- Hwang, Y. S., and J. H. Ku, (2004), Effect of high molecular weight chitosan on the quality and decay of strawberry fruits, J. Agri. Sci, 31, p77-86.
- Jarvis, W. R., (1977), Botryotinia and Botrytis species: Taxonomy, Physiology and Pathogenicity, A guide to the Literature, Monograph No. 15, Ottawa, Canada Department of Agriculture.
- Jeong, J. W., J. H. Jo, D. J. Kwon, and Y. B. Kim, (1990), Studies on the low temperature storage of strawberry pulp and red pepper paste by cryoprotectants, Kor. J. Food Sci. Technol, 22, p434-438.
- Kader, A. A., (1992), Postharvest biology and technology: an overview, p15-20, In: A.A. Kader (ed.), Postharvest technology of horticultural crops, Univ. Calif., Div. Agric. Nat. Resour., Publ, p3311Davis.
- Kim, T. I., W. S. Jang, J. H. Choi, M. H. Nam, W. S. Kim, and S. S. Lee, (2004), Breeding of strawberry ‘Maehyang’ for forcing culture, Kor. J. Hort. Sci. Technol, 22, p434-437, (in Korean).
- Nam, M. H., H. S. Kim, W. K. Lee, M. L. Gleason, and H. G. Kim, (2011), Control efficacy of gray mold on strawberry fruits by timing of chemical and microbial fungicide applications, Kor. J. Hort. Sci. Technol, 29, p151-155.
- Park, J. E., H. M. K, and S. J. Hwang, (2012a), Effect of harvest time, precooling, and storage temperature for keeping the freshness of Maehyang’ strawberry for export, J. Bio-Environ. Control, 21, p404-410, (in Korean).
- Park, J. E., H. M. Kim, and S. J. Hwang, (2012b), Qualitative changes in precooling and storage temperatures on the postharvest management of the fruits in strawberry for export, J. Agricul. Life Sci, 46, p67-74, (in Korean).
- The Korean Society of Plant Pathology, (2000), List of plant diseases in Korea, 5th ed, Seoul, Korean Society of Plant Pathology.
-
White, T. J., T. Bruns, S. Lee, and J. W. Taylor, (1990), Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics, In: MA. Innis, DH. Gelfand, JJ. Sninsky, TJ. White (eds), PCR protocols: a guide to methods and applications, New York, NY, Academic Press, p315-22.
[https://doi.org/10.1016/b978-0-12-372180-8.50042-1]